DiGeorge sendromu - DiGeorge syndrome
| DiGeorge sendromu | |
|---|---|
| Diğer isimler | DiGeorge anomalisi, velokardiyofasiyal sendrom (VCFS), Shprintzen sendromu, konotrunkal anomali yüz sendromu (CTAF), Takao sendromu, Sedlackova sendromu, Cayler kardiyofasiyal sendromu, CATCH22, 22q11.2 delesyon sendromu |
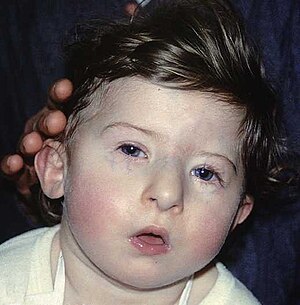 | |
| DiGeorge sendromunun karakteristik yüz özelliklerine sahip bir çocuk | |
| uzmanlık | tıbbi genetik |
| Belirtiler | çeşitli; yaygın olarak doğuştan kalp sorunları , belirli yüz özellikleri, yarık damak |
| komplikasyonlar | Böbrek sorunları , işitme kaybı , otoimmün bozukluklar |
| nedenler | Genetik (tipik olarak yeni mutasyon) |
| teşhis yöntemi | Semptomlara ve genetik testlere dayalı |
| Ayırıcı tanı | Smith-Lemli-Opitz sendromu , Alagille sendromu , VACTERL , Okülo-aurikülo-vertebral spektrum |
| Tedavi | Birçok sağlık uzmanlığını içerir |
| prognoz | Spesifik semptomlara bağlıdır |
| Sıklık | 4.000'de 1 |
22q11.2 delesyon sendromu olarak da bilinen DiGeorge sendromu , 22. kromozomun uzun kolundaki mikrodelesyonun neden olduğu bir sendromdur . Semptomlar değişebilmekle birlikte, genellikle doğuştan kalp sorunları , belirli yüz özellikleri, sık enfeksiyonlar, gelişimsel gecikme , öğrenme sorunları ve yarık damak içerir . İlişkili durumlar arasında böbrek sorunları , şizofreni , işitme kaybı ve romatoid artrit veya Graves hastalığı gibi otoimmün bozukluklar yer alır .
DiGeorge sendromu tipik olarak 22q11.2 olarak bilinen bir yerde 22. kromozomun ortasındaki 30 ila 40 genin silinmesinden kaynaklanır . Vakaların yaklaşık %90'ı , erken gelişim sırasındaki yeni bir mutasyon nedeniyle meydana gelirken, %10'u bir kişinin ebeveynlerinden miras alınır. Öyle baskın otozomal durumunun oluşmasına için tek etkilenen kromozom tabi yani. Tanı, semptomlara dayanarak şüphelenilir ve genetik testlerle doğrulanır .
Tedavisi olmamasına rağmen, tedavi semptomları iyileştirebilir. Bu genellikle, dahil olan potansiyel olarak birçok organ sisteminin işlevini iyileştirme çabalarıyla çok disiplinli bir yaklaşımı içerir . Uzun vadeli sonuçlar, mevcut semptomlara ve kalp ve bağışıklık sistemi problemlerinin ciddiyetine bağlıdır. Tedavi ile yaşam beklentisi normal olabilir.
DiGeorge sendromu yaklaşık 4.000 kişiden 1'inde görülür. Sendrom ilk olarak 1968'de Amerikalı doktor Angelo DiGeorge tarafından tanımlanmıştır . 1981'in sonlarında, altta yatan genetik belirlendi.
Belirti ve bulgular
Bu sendromun özellikleri, aynı ailenin üyeleri arasında bile büyük farklılıklar gösterir ve vücudun birçok bölümünü etkiler. Karakteristik belirti ve semptomlar, doğuştan kalp hastalığı gibi doğum kusurlarını, en sık olarak kapanma ile ilgili nöromüsküler problemlerle ( velofaringeal yetmezlik ), öğrenme güçlüğü , yüz hatlarında hafif farklılıklar ve tekrarlayan enfeksiyonlarla ilişkili damak kusurlarını içerebilir . Enfeksiyonlar nedeniyle sorunlara çocuklarda yaygındır bağışıklık sisteminin 'ın T hücresi - yanıtı aracılı bazı hastalarda bir mevcut olmayan ve ya kaynaklandığını hipoplastik timüs . DiGeorge sendromu, ilk olarak, etkilenmiş bir yenidoğanın, bozuk paratiroid bezleri ve düşük paratiroid hormonu ( parathormon ) seviyeleri nedeniyle hipokalsemiden kaynaklanan kalp kusurları veya kasılmaları olduğunda tespit edilebilir .
Etkilenen bireyler, böbrek anormallikleri ve bebekler olarak önemli beslenme güçlükleri dahil olmak üzere başka türde doğum kusurlarına da sahip olabilirler. Bu hasta popülasyonunda gastrointestinal sorunlar da çok yaygındır. Sindirim motilitesi sorunları kabızlığa neden olabilir. Gibi hastalıkları hipotiroidizm ve hipoparatiroidizm veya trombositopeni (düşük trombosit seviyeleri) ve psikiyatrik hastalıklar sıklıkla geç olarak ortaya çıkan özellikleri vardır.
Kromozomal bölge 22q11.2'deki mikrodelesyonlar, 20 ila 30 kat artmış şizofreni riski ile ilişkilidir . Çalışmalar, genel popülasyondaki 22q11.2DS'nin toplam tahmini %0.025 riski ile karşılaştırıldığında, şizofrenide %0.5 ila %2.0 arasında değişen ve ortalama yaklaşık %1.0 olan çeşitli 22q11.2DS oranları sağlar.
Belirgin özellikler, 22q11.2DS'yi tanımlamak için anımsatıcı CATCH-22 kullanılarak özetlenebilir ; 22, kromozomal anormalliği gösteren 22, aşağıdaki gibi 22. kromozomda bulunur:
- Kardiyak anormallik (yaygın olarak kesintiye uğramış aortik ark , truncus arteriosus ve Fallot tetralojisi )
- Anormal yüzler
- Timik aplazi
- Yarık dudak
- Hipokalsemi/hipoparatiroidizm
Bireyler, ilişkili özelliklerin sayısında ve hafiften çok ciddiye kadar değişen birçok olası özelliğe sahip olabilir. Yaygın olduğu gösterilen semptomlar şunları içerir:
- Konjenital kalp hastalığı (bireylerin %40'ı), özellikle konotrunkal malformasyonlar ( kesilmiş aortik ark (%50), persistan trunkus arteriosus (%34), Fallot tetralojisi ve ventriküler septal defekt )
- Siyanoz (oksijen açısından zengin kanın zayıf dolaşımı nedeniyle mavimsi cilt)
- Damak anomalileri (%50), özellikle velofaringeal yetersizlik , submukozal yarık damak ve yarık damak ; hipertelorizm dahil karakteristik yüz özellikleri ( Kafkas bireylerinin çoğunda bulunur )
- Bilişsel eksiklikler , dikkat eksikliği bozuklukları dahil olmak üzere öğrenme güçlükleri (%90)
- Hipokalsemi (%50)(hipoparatiroidizme bağlı)
- Önemli beslenme sorunları (%30)
- Böbrek anomalileri (%37)
- İşitme kaybı (her ikisi de iletken ve sensorinöral ) ( kranyofasiyal sendrom işitme kaybı )
- Laringotrakeoözofageal anomaliler
- Büyüme hormonu eksikliği
- Otoimmün bozukluklar
- Azalan T hücre sayılarına bağlı bağışıklık bozuklukları
- Şizofreni
- Nöbetler ( hipokalsemili veya hipokalsemisiz )
- İskelet anormallikleri
- Psikolojik bozukluklar
Bu sendrom eksik penetrans ile karakterizedir . Bu nedenle, farklı hastalar arasında klinik ifadede belirgin bir değişkenlik vardır. Bu genellikle erken teşhisi zorlaştırır.
Bilişsel bozukluklar
DiGeorge sendromlu çocukların nöropsikolojik testlerde belirli bir profili vardır. Genellikle sınırın altında normal bir IQ'ya sahiptirler ve çoğu birey sözel alanlarda sözel olmayan alanlardan daha yüksek puanlara sahiptir. Bazıları ana akım okullara devam edebilirken, diğerleri evde eğitim veya özel sınıflarda eğitim görmektedir. Erken çocukluk döneminde hipokalseminin şiddeti, otizm benzeri davranışsal zorluklarla ilişkilidir.
DiGeorge sendromlu yetişkinler, şizofreni geliştirmek için özellikle yüksek riskli bir gruptur. Yaklaşık %30'unda en az bir psikoz atağı vardır ve yaklaşık dörtte biri yetişkinliğe kadar şizofreni geliştirir .
DiGeorge sendromlu bireylerin erken başlangıçlı Parkinson hastalığı (PD) geliştirme riski de daha yüksektir . Parkinson semptomlarına neden olabilen antipsikotiklerin kullanımı nedeniyle Parkinson teşhisi 10 yıla kadar gecikebilir .
Konuşma ve dil
Mevcut araştırmalar, benzersiz bir konuşma ve dil bozuklukları profilini gösteriyor, 22q11.2DS ile ilişkili. Çocuklar genellikle sözel olmayan IQ puanlarına kıyasla konuşma ve dil değerlendirmelerinde daha düşük performans gösterirler. Yaygın sorunlar arasında hipernasalite, dil gecikmeleri ve konuşma sesi hataları bulunur.
Hipernasalite , sözlü konuşma seslerinin üretimi sırasında burundan hava kaçtığında oluşur ve bu da anlaşılabilirliğin azalmasına neden olur . Bu, konuşma ve dil profilinde yaygın bir özelliktir çünkü çocukların %69'unda damak anomalisi vardır. Yumuşak damak perdesinin yapısı havanın burun boşluğuna gitmesini engellemeyecek şekilde ise hipernazal konuşmaya neden olur . Bu fenomene velofaringeal yetersizlik (VPI) denir . İşitme kaybı aynı zamanda artan hipernazaliteye de katkıda bulunabilir çünkü işitme bozukluğu olan çocuklar sözlü konuşma çıktılarını kendi kendilerine izlemekte zorlanabilirler. VPI için mevcut tedavi seçenekleri protez ve ameliyatı içerir.
Dil gelişiminin başlangıcında kelime hazinesi edinme ve konuşulan dili formüle etme zorlukları ( ifade edici dil eksiklikleri) de 22q11.2 silme ile ilişkili konuşma ve dil profilinin bir parçasıdır. Okul öncesi çağındaki çocuklar için kelime kazanımı genellikle ciddi şekilde gecikir. Son zamanlarda yapılan bazı araştırmalarda, çocukların kelime dağarcığı çok kısıtlıydı veya 2-3 yaşlarında hala sözlü değillerdi. Okul çağındaki çocuklar, olgunlaştıkça ifade edici dilde ilerleme kaydederler, ancak birçoğu, anlatıları sözlü olarak hatırlama ve daha uzun ve daha karmaşık cümleler üretme gibi dil görevleriyle sunulduğunda gecikmeler yaşamaya ve zorluk göstermeye devam eder. Konuşulan dili anlama, muhafaza etme veya işleme yeteneği olan alıcı dil de genellikle ifade edici dil bozuklukları ile aynı şiddette olmasa da bozulabilir.
Artikülasyon hataları, DiGeorge sendromlu çocuklarda yaygın olarak bulunur. Bu hatalar, sınırlı bir fonemik (konuşma sesi) envanterini ve anlaşılabilirliğin azalmasına neden olan telafi edici artikülasyon stratejilerinin kullanımını içerir. Phonemic Tipik olarak oluşan stok ön ya da ağız boşluğu arka yapılan ses oluşur: / p /, / a /, / m /, / n / ve gırtlak durur. Ağız ortasında yapılan ses tamamen yoktur. Bu çocuk popülasyonu tarafından yapılan telafi edici artikülasyon hataları şunları içerir: gırtlak durmaları , nazal yer değiştirmeler, faringeal frikatifler, linguapalatal ıslık sesleri, ünsüz sesler üzerinde azaltılmış basınç veya bu semptomların bir kombinasyonu. Bu hatalardan gırtlak durmaları en yüksek görülme sıklığına sahiptir. Damağın yapısal anormallikleri nedeniyle sınırlı bir fonemik envanterin ve telafi edici artikülasyon stratejilerinin kullanımının mevcut olduğu düşünülmektedir . Bu popülasyon tarafından sergilenen konuşma bozuklukları, genç yaşlarda daha şiddetlidir ve çocuk olgunlaştıkça kademeli bir iyileşme eğilimi gösterir.
Genetik
DiGeorge sendromu, kromozom 22, bölge 1, bant 1, alt bant 2'nin (22q11.2) uzun kolunun (q) bir kısmının heterozigot olarak silinmesinden kaynaklanır . Hastaların yaklaşık% 80-90 3'ün bir silme bilgisi Mb ve% 8 1,5 MB bir silme sahiptir. Silme işleminden etkilenen gen sayısı yaklaşık 30 ila 50 olarak belirtilmiştir. Çok nadiren, benzer klinik özelliklere sahip hastalarda, kromozom 10'un kısa kolunda delesyonlar olabilir. Bozukluk, otozomal dominant bir kalıtım modeline sahiptir.
1995 ile 2013 yılları arasında teşhis konan 749 kişi üzerinde yapılan bir Fransız araştırması, mutasyonun hastaların %15'inde kalıtsal olduğunu ve bunun %85,5'inin anneden geldiğini buldu. Diğer çalışmalar kalıtım oranlarının %6-10 olduğunu bulmuştur. Çoğu vaka, de novo (ailede yeni) silme işleminin bir sonucudur . Bunun nedeni, 22q11 bölgesinin sperm veya yumurta oluşumu sırasında yeniden düzenlenmelere oldukça yatkın bir yapıya sahip olmasıdır.
Sendromun ilişkili tüm özelliklerine neden olan kesin mekanizma bilinmemektedir. Silinen bölgedeki 30-50 genden bazılarının, bazı belirti ve semptomların gelişiminde muhtemelen rol oynadığı tespit edilmiştir.
TBX1
Haploinsufficiency ait TBX1 gen (T-box transkripsiyon faktörü TBX1) gözlenen bazı semptomlarının nedeni olduğu düşünülmektedir. Bu gendeki nokta mutasyonları , DiGeorge sendromlu bireylerde de gözlenmiştir. TBX1, embriyonik gelişim sırasında doku ve organ oluşumunda önemli rolü olan T-box gen ailesinin bir parçasıdır ve migrasyon sonrası nöral krest hücrelerinin farklılaşmasının düzenlenmesinde rol oynayabilir . Nöral krest, kafatası kemikleri, yüz ve damak mezenşimi , kalbin çıkış yolu ve timus ve paratiroid stroması dahil olmak üzere DiGeorge sendromunda etkilenen yapıların çoğunu oluşturur . Faringeal arkların gelişimi sırasında FGF18 ekspresyonu kaybı olduğunda , nöral krest hücre ölümü görülür. Ne FGF18 ne de TBX1 nöral krest hücrelerinde eksprese edilmese de, TBX1'in FGF18 ekspresyonunun düzenlenmesinde rolü olabilir ve bu hücrelerin faringeal bölgede farklılaşmasının doğru olmasını sağlar. Bu nedenle, DiGeorge sendromundaki bazı semptomlardan TBX1 disfonksiyonu sorumlu olabilir.
Fare modellerinde yapılan araştırmalar, Tbx1'in silinmesinin insanlarda görülenlere benzer çeşitli kusurlara yol açtığını ve esas olarak büyük arterlerin ve timusun gelişimini etkilediğini göstermiştir .
Tbx1 eksikliği olan farelerin büyük arterlerinde görülen anormallikler, erken gelişim sırasında aort arklarının anormal oluşumu ve yeniden şekillenmesinin bir sonucudur . Aortik arkların doğru oluşumu ve yeniden şekillenmesi için Tbx1'in rolü, Tbx1'in kardiyovasküler gelişim ve DiGeorge sendromunda görülen fenotipler için anahtar rolünü öne süren çeşitli fare modellerinde kapsamlı bir şekilde incelenmiştir.
DGCR8
Farelerde, DGCR8 geninin haploins yetmezliği , microRNA miR-338 ve 22q11.2 delesyon fenotiplerinin yanlış düzenlenmesiyle ilişkilendirilmiştir .
TANGO2
Kromozom 22 açık okuma çerçevesi 25 (C22orf25) olarak da bilinen taşıma ve golgi organizasyon 2 homologu ( TANGO2 ), insanlarda TANGO2 geni tarafından kodlanan bir proteindir.
C22orf25'i kodlayan gen, kromozom 22'de ve q11.21 konumunda bulunur, bu nedenle genellikle 22q11.2 delesyon sendromu ile ilişkilidir. Ancak TANGO2 bozukluğunun otozomal çekinik olması her durumda ortaya çıkmaz.
TANGO2 genindeki mutasyonlar, mitokondriyal β-oksidasyonda kusurlara ve endoplazmik retikulum stresinde artışa ve Golgi hacim yoğunluğunda azalmaya neden olabilir . Bu mutasyonlar, erken başlangıçlı hipoglisemi , hiperamonyemi , rabdomiyoliz , kardiyak aritmiler ve daha sonra bilişsel bozulmaya dönüşen ensefalopati ile sonuçlanır .
Parkinson hastalığı genleri
22q11.2DS, daha yüksek erken başlangıçlı Parkinson hastalığı (PD) riski ile ilişkilendirilmiştir . Görülen nöropatoloji, LRRK2 ile ilişkili PD'ye benzer . 22q11.2DS'li bireylerde etkilenen genlerin hiçbiri daha önce PD ile bağlantılı değildi, ancak muhtemel aday olan birkaç tane var. Bu beyin microDNA biyogenezine için önemli olan DGCR8 içerir SRPT5 bir proteini kodlayan ile etkileşime PARK2 protein, COMT dopamin seviyesini düzenleyen katılır ve mikroRNA miR-185 PD lokuslar LRRK2 bilinen hedef düşünülmektedir.
Teşhis

DiGeorge sendromunun teşhisi, potansiyel semptomların sayısı ve bireyler arasındaki fenotiplerdeki farklılıklar nedeniyle zor olabilir. Bir veya daha fazla delesyon belirtisi olan hastalarda şüphelenilir. Bu durumlarda 22q11.2DS teşhisi, kromozom 22, bölge 1, bant 1, alt bant 2'nin uzun kolunun (q) bir kısmının silinmesinin gözlemlenmesiyle doğrulanır. Genetik analiz normalde floresan in situ hibridizasyon kullanılarak yapılır. (FISH), standart karyotiplemenin (örneğin G-bantlama ) gözden kaçırdığı mikrodelesyonları saptayabilir . Daha yeni analiz yöntemleri , her ikisi de FISH tarafından tespit edilmeyen 22q11.2'de atipik silmeleri tespit edebilen Multipleks ligasyona bağlı prob amplifikasyon testi (MLPA) ve kantitatif polimeraz zincir reaksiyonu (qPCR) içerir. qPCR analizi ayrıca 3 ila 14 gün arasında değişebilen FISH'den daha hızlıdır.
22q kromozomu üzerindeki 37 noktada kopya sayısı varyasyonunu tespit etmek için geliştirilen yeni bir yüksek tanımlı MLPA probu üzerinde 2008 yılında yapılan bir araştırma, normal 22q11.2 delesyonlarını tespit etmede bunun FISH kadar güvenilir olduğunu bulmuştur. Ayrıca FISH kullanılarak kolayca gözden kaçan daha küçük atipik silmeleri de tespit edebildi. Bu faktörler, daha düşük maliyet ve daha kolay test ile birlikte bu MLPA probunun klinik testlerde FISH'in yerini alabileceği anlamına gelir.
Boncuklar üzerinde BAC'leri kullanan genetik testler, doğum öncesi testler sırasında 22q11.2DS ile tutarlı silmeleri tespit etmede başarılı olmuştur. Dizi karşılaştırmalı genomik hibridizasyon (dizi-CGH), tüm genomu silme veya çoğaltma için taramak için bir çipte kabartmalı çok sayıda prob kullanır. 22q11.2'nin doğum sonrası ve doğum öncesi tanısında kullanılabilir.
DiGeorge sendromu semptomları olan bireylerin %5'inden azında normal rutin sitogenetik çalışmalar ve negatif FISH testi vardır. Bu durumlarda, atipik silmeler nedendir. Bazı 22q11.2 delesyon sendromu vakaları, diğer kromozomlarda, özellikle de 10p14 kromozom bölgesinde bir delesyonda kusurlara sahiptir.
Tedavi
DiGeorge sendromu için bilinen bir tedavi yoktur. Bazı bireysel özellikler standart tedaviler kullanılarak tedavi edilebilir. Anahtar, ilişkili özelliklerin her birini tanımlamak ve her birini mevcut en iyi tedavileri kullanarak yönetmektir.
Örneğin çocuklarda kan transfüzyonu ve canlı aşılarla bağışıklama konusunda özel önlemler alınması gerektiğinden bağışıklık sorunlarının erken teşhis edilmesi önemlidir. Timus transplantasyonu , nadir görülen, "tam" DiGeorge sendromunda timusun yokluğunu gidermek için kullanılabilir. Bakteriyel enfeksiyonlar antibiyotiklerle tedavi edilir . Konjenital kalp anormallikleri için genellikle kalp cerrahisi gerekir. Hipokalsemiye neden olan hipoparatiroidizm genellikle ömür boyu D vitamini ve kalsiyum takviyesi gerektirir. Çok sistemli bakım sağlayan özel klinikler, DiGeorge sendromlu bireylerin tüm sağlık ihtiyaçlarının değerlendirilmesine ve hastaların dikkatli bir şekilde izlenmesine olanak tanır. Bu tür bir sistemin bir örneği , çocuklara 22q11 delesyon sendromu ile sürekli destek, tıbbi bakım ve bir sağlık ekibinden bilgi sağlayan SickKids Hastanesi Toronto, Kanada'daki 22q Silme Kliniğidir .
Metirozin ( metiltirozin ), DiGeorge sendromu için etiket dışı bir tedavi olarak kullanılır.
epidemiyoloji
DiGeorge sendromunun 2000'de bir ile 4000 canlı doğumda birini etkilediği tahmin edilmektedir. Bu tahmin, büyük doğum kusurlarına dayanmaktadır ve eksik bir tahmin olabilir, çünkü delesyonu olan bazı kişilerde çok az semptom vardır ve resmi olarak teşhis edilmemiş olabilir. Genetik delesyon sendromu nedeniyle zihinsel engelliliğin en yaygın nedenlerinden biridir .
Etkilenen insan sayısının birden fazla nedenden dolayı artması bekleniyor: (1) cerrahi ve tıbbi gelişmeler, artan sayıda insan sendromla ilişkili kalp kusurlarından kurtuluyor. Bu bireyler sırayla çocuk sahibi olurlar. DiGeorge sendromlu bir kişinin etkilenmiş bir çocuğa sahip olma şansı her hamilelik için %50'dir; (2) Çocukları etkilemiş, ancak kendi genetik koşullarından habersiz olan ebeveynler, şimdi genetik testlerin kullanıma sunulmasıyla teşhis edilmektedir; (3) FISH (floresan in situ hibridizasyon) gibi moleküler genetik tekniklerin sınırlamaları vardır ve 22q11.2 delesyonlarının hepsini tespit edememiştir. Daha yeni teknolojiler bu atipik silmeleri tespit edebildi.
İsim
DiGeorge sendromunun belirti ve semptomları o kadar çeşitlidir ki, özelliklerinin farklı gruplandırmaları bir zamanlar ayrı koşullar olarak kabul edildi. Bu orijinal sınıflandırmalar velokardiyofasiyal sendrom, Shprintzen sendromu, DiGeorge dizisi/sendromu, Sedlackova sendromu ve konotrunkal anomali yüz sendromunu içeriyordu. Artık hepsinin tek bir sendromun sunumları olduğu anlaşılıyor.
ICD-10 2015 versiyonu, iki kod kullanarak DiGeorge sendromundan bahseder: D82.1 (Di George sendromu) ve Q93.81 (Velo-kardiyo-yüz sendromu). ICD-11 Beta Taslağı, sendromu “LD50.P1 CATCH 22 fenotipi” başlığı altında tartışır. Ancak bu sendroma 22. kromozomun küçük bir parçasının silinmesi neden olduğu için , bazıları “22q11.2 delesyon sendromu (22q11) adını önermektedir. .2DS)" kullanılabilir. Bazı uzmanlar, hem DiGeorge hem de velokardiyofasiyal sendromların adının CATCH-22 olarak değiştirilmesini destekler. Uluslararası 22q11.2 Vakfı, "Aynı Ad Kampanyası" aracılığıyla 22q11.2 delesyon sendromu adını savunur.
Ayrıca bakınız
Referanslar
Bu makale, ABD Ulusal Tıp Kütüphanesinden alınan kamu malı metni içermektedir .
Dış bağlantılar
| sınıflandırma | |
|---|---|
| Dış kaynaklar |
- DiGeorge sendromu de Curlie
- McDonald-McGinn DM, Emanuel BS, Zackai EH (16 Aralık 2005). "22q11.2 Silme Sendromu" . Pagon RA, Bird TD, Dolan CR, Stephens K (ed.). Geneİncelemeler . Washington Üniversitesi, Seattle. PMID 20301696 . NBK1523.
- Firth HV (17 Şubat 2009). "22q11.2 Çoğaltma" . Pagon RA, Bird TD, Dolan CR, Stephens K (ed.). Geneİncelemeler . Washington Üniversitesi, Seattle. PMID 20301749 . NBK3823.


