Duchenne kas distrofisi - Duchenne muscular dystrophy
| Duchenne kas distrofisi | |
|---|---|
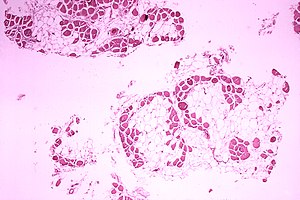 | |
| Mikroskopik geniş değiştirme gösteren Duchenne kas distrofisi olan bir kişinin, çapraz kesit baldır kas görüntü kas lifleri ile yağ hücreleri . | |
| Telaffuz | |
| uzmanlık | Pediatrik nöroloji , nöromüsküler tıp , tıbbi genetik . |
| Belirtiler | Kas güçsüzlüğü , ayağa kalkmada güçlük, skolyoz |
| Her zamanki başlangıç | 4 yaş civarında |
| nedenler | Genetik ( X'e bağlı resesif ) |
| teşhis yöntemi | Genetik test |
| Tedavi | Farmakolojik tedavi, fizik tedavi , diş telleri , konuşma terapisi, mesleki terapi, cerrahi, yardımlı ventilasyon |
| prognoz | yaşam beklentisi 26 |
| Sıklık | Erkeklerde 3.500-6.000'de 1; kadınlarda, 50.000.000'de 1 |
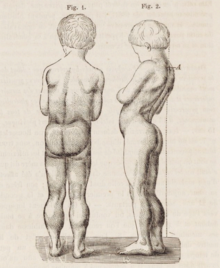
Duchenne müsküler distrofisi ( DMD ), esas olarak erkekleri etkileyen ciddi bir müsküler distrofi türüdür. Kas zayıflığı genellikle dört yaş civarında başlar ve hızla kötüleşir. Kas kaybı tipik olarak önce uyluklarda ve pelviste, ardından kollarda meydana gelir. Bu, ayakta durmakta sorun yaşamanıza neden olabilir. Çoğu, 12 yaşına kadar yürüyemez. Etkilenen kaslar, artan yağ içeriği nedeniyle daha büyük görünebilir . Skolyoz da yaygındır. Bazıları zihinsel engelli olabilir . Kusurlu genin tek bir kopyasına sahip olan dişiler hafif semptomlar gösterebilir.
Bozukluk X'e bağlı resesiftir . Vakaların yaklaşık üçte ikisi bir kişinin annesinden miras alınırken, vakaların üçte biri yeni bir mutasyondan kaynaklanmaktadır . Bu bir mutasyon neden olur geni için protein distrofin . Distrofin, kas lifinin hücre zarını korumak için önemlidir . Genetik testler genellikle tanıyı doğumda yapabilir. Ayrıca, bu etkilenen yüksek düzeyde kreatin kinaz kendi içinde kan .
Bilinen bir tedavisi olmamasına rağmen, fizik tedavi , diş telleri ve düzeltici cerrahi bazı semptomlara yardımcı olabilir. Solunum kasları zayıf olanlarda yardımlı ventilasyon gerekebilir . Kullanılan ilaçlar arasında kas dejenerasyonunu yavaşlatmak için steroidler , nöbetleri ve bazı kas aktivitelerini kontrol etmek için antikonvülsanlar ve ölmekte olan kas hücrelerine verilen hasarı geciktirmek için immünosupresanlar bulunur . Bir tedavi olarak gen tedavisi , insanlarda çalışmanın erken aşamalarındadır. Gen terapisini kullanan küçük bir ilk çalışma, bazı çocukların kas gücünü artırdı, ancak 2020 itibariyle uzun vadeli etkiler bilinmiyor.
DMD, doğumda yaklaşık 3.500 ila 6.000 erkekten birini etkiler. En sık görülen müsküler distrofi türüdür. Yaşam süresi 26 olduğu; ancak, mükemmel bir özenle, bazıları 30'lu veya 40'lı yaşlarına kadar yaşayabilir. Hastalık kızlarda çok daha nadirdir ve yaklaşık 50.000.000 canlı kadın doğumunda bir görülür.
Belirti ve bulgular
DMD , kas lifi düzensizliği, ölüm ve bağ dokusu veya yağ ile yer değiştirme nedeniyle ilerleyici kas güçsüzlüğüne neden olur . Önce istemli kaslar etkilenir, özellikle kalçalar , pelvik bölge , uyluklar , baldırlar . Sonunda omuzlara ve boyuna ilerler , ardından kollar , solunum kasları ve diğer alanlar gelir. Yorgunluk yaygındır.
Belirtiler genellikle beş yaşından önce ortaya çıkar ve bir erkek çocuğunun ilk adımlarını attığı andan itibaren bile gözlemlenebilir. Motor becerilerde , yürüme, adım atma veya koşmada garip bir şekilde sonuçlanabilecek genel bir zorluk vardır . Kısmen Aşil tendonunun kısalması nedeniyle ve diz ekstansör zayıflığını telafi ettiği için ayak parmakları üzerinde yürüme eğilimindedirler . Düşmeler sık olabilir. Çocuğun yürümesi giderek zorlaşıyor; yürüme yeteneği genellikle 13 yaşından önce tamamen parçalanır. DMD'den etkilenen erkeklerin çoğu, 21 yaşına kadar esasen "boyundan aşağısı felç olur". Kardiyomiyopati , özellikle dilate kardiyomiyopati , 18 yaşındakilerin yarısında görülür. Konjestif kalp yetmezliği veya aritmi (düzensiz kalp atışı) gelişimi sadece ara sıradır. Hastalığın geç evrelerinde, pnömoni ile sonuçlanabilecek solunum bozukluğu ve yutma bozukluğu meydana gelebilir .
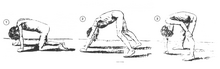
DMD'nin klasik bir işareti, pozitif bir Gowers işaretiyle kendini gösterdiği gibi, yalan söyleme veya oturma pozisyonundan kalkmada zorluktur . Bir çocuk yüzüstü yatarak kalkmaya çalıştığında, üst ekstremitelerini kullanarak pelvik kas zayıflığını telafi eder: önce kolları ve dizleri üzerinde durmak için ayağa kalkarak ve sonra dik durmak için ellerini bacaklarının üzerinde "yürüterek". DMD'nin bir başka karakteristik işareti, dil, baldır, kalça ve omuz kaslarının (4 veya 5 yaş civarında) psödohipertrofisidir (büyümesi). Kas dokusu sonunda yağ ve bağ dokusu ile değiştirilir, dolayısıyla psödohipertrofi terimi. Kas lifi bozuklukları ve kas kontraktürleri kas lifleri kısaltılması nedeniyle Aşil tendonu ve hamstring olan bozmaktadır işlevselliği oluşabilir fibroz de bağ doku . Lomber hiperlordoz , skolyoz , anterior pelvik tilt ve göğüs deformiteleri gibi iskelet deformiteleri oluşabilir . Lomber hiperlordozun, tümü değişen duruş ve yürüyüşe neden olan gluteal ve kuadrisep kas zayıflığına yanıt olarak telafi edici bir mekanizma olduğu düşünülmektedir (örneğin: kısıtlı kalça ekstansiyonu).
DMD'nin kas-iskelet sistemi dışı belirtileri ortaya çıkar. Nöro-davranışsal bozukluklar (örneğin, DEHB ), öğrenme bozuklukları ( disleksi ) ve belirli bilişsel becerilerde (özellikle kısa süreli sözel bellek) ilerleyici olmayan zayıflıklar için daha yüksek bir risk vardır ve bunların yokluğun veya işlevsizliğin sonucu olduğuna inanılmaktadır. beyindeki distrofin.
Neden
DMD, X kromozomunun kısa kolunda bulunan Xp21 lokusunda distrofin geninin mutasyonundan kaynaklanır . Distrofin , her bir kas lifinin aktin hücre iskeletini , birçok alt birim içeren bir protein kompleksi aracılığıyla alttaki bazal laminaya ( hücre dışı matris ) bağlamaktan sorumludur . Distrofinin yokluğu, fazla kalsiyumun sarkolemmaya (hücre zarı) nüfuz etmesine izin verir . Kalsiyum ve sinyal yollarındaki değişiklikler, suyun mitokondriye girmesine neden olur ve daha sonra patlar.
İskelet kası distrofisinde, mitokondriyal disfonksiyon, stres kaynaklı sitozolik kalsiyum sinyallerinin amplifikasyonuna ve stres kaynaklı reaktif-oksijen türlerinin üretiminin amplifikasyonuna yol açar . Birkaç yolu içeren ve net olarak anlaşılmayan karmaşık bir basamaklama işleminde , hücre içinde artan oksidatif stres sarkolemmaya zarar verir ve sonunda hücrenin ölümüyle sonuçlanır. Kas lifleri nekroza uğrar ve nihayetinde yağ ve bağ dokusu ile değiştirilir .
DMD, X'e bağlı çekinik bir düzende devralınır . Erkekler etkilenirken dişiler tipik olarak genetik özelliğin taşıyıcılarıdır . Dişi bir taşıyıcı, etkilenmiş bir oğlu olana kadar mutasyon taşıdığından habersiz olacaktır. Taşıyıcı bir annenin oğlunun, kusurlu geni annesinden miras alma olasılığı %50'dir. Taşıyıcı bir annenin kızının taşıyıcı olma olasılığı %50 ve genin iki normal kopyasına sahip olma olasılığı %50'dir. Her durumda, etkilenmemiş bir baba ya oğluna normal bir Y ya da kızına normal bir X verir. DMD gibi X'e bağlı resesif bir durumun kadın taşıyıcıları, X inaktivasyon paternlerine bağlı olarak semptomlar gösterebilir . DMD'nin 3.600 erkek bebekte bir görülme sıklığı vardır. Distrofin genindeki mutasyonlar ya kalıtsal olabilir ya da germ hattı iletimi sırasında kendiliğinden ortaya çıkabilir.
DMD kadınlarda son derece nadirdir (yaklaşık 50.000.000 kadın doğumunda 1). Anne babası ve taşıyıcı anne olan kadınlarda, X kromozomu eksik olanlarda veya inaktif X kromozomu olanlarda (nadir nedenlerin en yaygını) ortaya çıkabilir. Taşıyıcı bir annenin ve etkilenmiş bir babanın kızı etkilenecek veya eşit olasılıkla bir taşıyıcı olacaktır, çünkü etkilenen X kromozomunu her zaman babasından miras alacaktır ve etkilenen X kromozomunu annesinden de miras alma şansı %50'dir. .
Kan-beyin bariyerinin bozulmasının, DMD'nin gelişiminde kayda değer bir özellik olduğu görülmüştür.
Teşhis
Ailesinde bozukluk öyküsü olan kişiler için genetik danışmanlık önerilir. DMD, gebelik sırasında yapılan genetik çalışmalarla yaklaşık %95 doğrulukla tespit edilebilir. Kan dolaşımındaki kreatin kinaz (CPK-MM) seviyeleri son derece yüksektir. Bir elektromiyografi (EMG), zayıflığın sinirlerdeki hasardan ziyade kas dokusunun tahrip edilmesinden kaynaklandığını gösterir .
DNA testi
Distrofin geninin kasa özgü izoformu 79 ekzondan oluşur ve DNA testi ( kan testi ) ve analiz genellikle etkilenen ekzon veya ekzonların spesifik mutasyon tipini tanımlayabilir. DNA testi çoğu durumda tanıyı doğrular.
kas biyopsisi
DNA testi mutasyonu bulamazsa, kas biyopsisi testi yapılabilir. Biyopsi iğnesi kullanılarak küçük bir kas dokusu örneği çıkarılır. DMD için biyopsi örneğinde gerçekleştirilen anahtar testler , distrofin için immünohistokimya , immünositokimya ve immünoblotlamadır ve deneyimli bir nöromüsküler patolog tarafından yorumlanmalıdır. Bu testler, proteinin varlığı veya yokluğu hakkında bilgi sağlar. Proteinin yokluğu, DMD için pozitif bir testtir. Distrofinin mevcut olduğu durumlarda testler, distrofinin miktarını ve moleküler boyutunu göstererek DMD'yi daha hafif distrofinopati fenotiplerinden ayırmaya yardımcı olur . Geçtiğimiz birkaç yıl içinde, duruma neden olan birçok mutasyonun daha fazlasını tespit eden DNA testleri geliştirildi ve DMD'nin varlığını doğrulamak için kas biyopsisi gerekli değildir.
doğum öncesi testler
Anne bilinen veya şüphelenilen bir taşıyıcı olduğunda doğum öncesi test düşünülebilir.
Doğum öncesi testler, doğmamış çocuğun en yaygın mutasyonlardan birine sahip olup olmadığını söyleyebilir. DMD'den birçok mutasyon sorumludur ve bazıları tanımlanmamıştır, bu nedenle annede şüphelenilen mutasyon tanımlanmadıysa genetik testler yanlış negatif olabilir.
İnvaziv testlerden önce fetal cinsiyetin belirlenmesi önemlidir; Erkekler bazen bu X'e bağlı hastalıktan etkilenirken, kadın DMD'si oldukça nadirdir. Bu, 16 haftada ultrason taramasıyla veya daha yakın bir zamanda ücretsiz fetal DNA (cffDNA) testiyle elde edilebilir. Koryon villus örneklemesi (CVS) 11–14 haftada yapılabilir ve %1'lik bir düşük riski vardır. Amniyosentez 15 hafta sonra yapılabilir ve %0.5 düşük yapma riski vardır. İnvaziv olmayan doğum öncesi testler 10-12 hafta civarında yapılabilir. Genetik test sonuçlarının net olmadığı durumlarda bir diğer seçenek ise fetal kas biyopsisidir.
Tedavi

DMD için bir tedavi bilinmemektedir ve düzenleyici makamlar tarafından devam eden bir tıbbi ihtiyaç kabul edilmiştir . Gen tedavisi bir miktar başarı göstermiştir.
Tedavi genellikle spesifik anketler kullanılarak ölçülebilen yaşam kalitesini en üst düzeye çıkarmak için semptomların başlangıcını kontrol etmeyi amaçlar ve şunları içerir:
- Prednizolon ve deflazakort gibi kortikosteroidler , 2 yıla kadar kas gücü ve işlevinde kısa süreli iyileşmelere yol açar. Bunun için kanıtlar sağlam olmasa da, kortikosteroidlerin yürümeyi uzatmaya yardımcı olduğu da bildirilmiştir.
- Randomize kontrol denemeleri, β 2 agonistlerinin kas gücünü artırdığını, ancak hastalığın ilerlemesini değiştirmediğini göstermiştir. β 2 agonistlerle ilgili çoğu RCT için takip süresi sadece 12 ay civarındadır, bu nedenle sonuçlar bu zaman çerçevesinin ötesinde tahmin edilemez.
- Yüzme gibi hafif, sarsıcı olmayan fiziksel aktiviteler teşvik edilir. Hareketsizlik ( yatak istirahati gibi ) kas hastalığını kötüleştirebilir.
- Fizik tedavi, kas gücünü, esnekliğini ve işlevini korumaya yardımcı olur.
- Ortopedik aletler (diş telleri ve tekerlekli sandalyeler gibi) hareketliliği ve kendi kendine bakım yeteneğini geliştirebilir. Uyku sırasında ayak bileğini yerinde tutan, vücuda oturan çıkarılabilir bacak destekleri, kontraktürlerin başlamasını geciktirebilir .
- Hastalık ilerledikçe uygun solunum desteği önemlidir.
- Kalp sorunları kalp pili gerektirebilir .
Bir Morfolino antisens oligo olan eteplirsen ilacı , distrofin ekson 51 atlamasına uygun mutasyonların tedavisi için Amerika Birleşik Devletleri'nde onaylanmıştır. Eteplirsen klinik bir fayda sağlayamadığı için ABD onayı tartışmalı olmuştur; Avrupa İlaç Ajansı tarafından onaylanmamıştır.
İlaç ataluren (Translarna) Avrupa Birliği'nde kullanımı onaylanmıştır.
Duyarlılık karşıtı oligonükleotid golodirsen (Vyondys 53) distrofin transkript ekson 53 atlama yararlanabilir vakaların tedavisi için, 2019 yılında Amerika Birleşik Devletleri'nde tıbbi kullanım için onaylanmıştır.
Morfolino duyarlılık karşıtı oligonükleotid viltolarsen (Viltepso) 53 atlamayı ekson mükellef olduğu DMD geninin bir teyit mutasyonu olan kişilerde Duchenne müsküler distrofi (DMD) tedavisi için, Ağustos 2020 yılında Amerika Birleşik Devletleri'nde tıbbi kullanım için onaylanmıştır. Amerika Birleşik Devletleri'nde bu tür mutasyona sahip kişiler için onaylanmış ikinci hedefli tedavidir. DMD'li kişilerin yaklaşık %8'i, ekson 53 atlamasına uygun bir mutasyona sahiptir.
Casimersen , Şubat 2021'de Amerika Birleşik Devletleri'nde tıbbi kullanım için onaylandı ve ekson 45 atlamaya uygun, DMD geninin doğrulanmış bir mutasyonuna sahip kişiler için FDA onaylı ilk hedefli tedavidir.
DMD için kapsamlı multidisipliner bakım kılavuzları, Hastalık Kontrol ve Önleme Merkezleri tarafından geliştirildi ve 2010 yılında The Lancet Neurology'de iki bölüm halinde yayınlandı. 2018'de bir güncelleme yayınlandı.
Fizik Tedavi
Fiziksel terapistler, hastaların maksimum fiziksel potansiyellerine ulaşmalarını sağlamakla ilgilenir. Amaçları:
- Uygun olduğunda bir esneme ve egzersiz programı geliştirerek kontraktür ve deformite gelişimini en aza indirin
- Destekleyici ve dayanıklı tıbbi ekipman önererek fiziksel nitelikteki diğer ikincil komplikasyonları tahmin edin ve en aza indirin
- solunum fonksiyonunu izleyin ve solunum egzersizlerine yardımcı olacak teknikler ve sekresyonları temizleme yöntemleri hakkında tavsiyelerde bulunun
Solunum yardımı
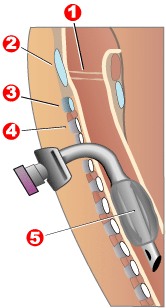
1 – Vokal kıvrımlar
2 – Tiroid kıkırdak
3 – Krikoid kıkırdak
4 – Trakeal halkalar
5 – Balon manşet
Kişiye her nefeste ayarlanabilir bir hacim (miktar) hava veren modern "hacim ventilatörleri /solunum cihazları", müsküler distrofiye bağlı solunum problemleri olan kişilerin tedavisinde değerlidir. Ventilatör, havanın doğrudan iletildiği invaziv bir endotrakeal veya trakeotomi tüpü gerektirebilir , ancak bazı insanlar için bir yüz maskesi veya ağızlık yoluyla invaziv olmayan uygulama yeterlidir. Pozitif hava yolu basıncı makineleri, özellikle iki seviyeli olanlar, bazen bu şekilde kullanılır. Solunum ekipmanı, taşınabilirlik için harici pilli bir elektrikli tekerlekli sandalyenin altındaki veya arkasındaki bir ventilatör tepsisine kolayca sığabilir.
Ventilatör tedavisi, solunum kaslarının çökmeye başlayabildiği onlu yaşların ortalarından sonlarına kadar başlayabilir. Vital kapasite normalin %40'ının altına düşmüşse, kişinin solunum sıkıntısı yaşamasının (hipoventilasyon) en muhtemel olduğu uyku saatleri sırasında bir volüm ventilatörü/solunum cihazı kullanılabilir. Uyku sırasında hipoventilasyon , bir oksimetre çalışması ve bir kılcal kan gazı ile kapsamlı bir uyku bozukluğu öyküsü ile belirlenir (bakınız solunum fonksiyon testi ). Öksürüğe yardımcı bir cihaz, akciğerlerin pozitif hava basıncıyla hiperinflasyonu ve ardından mukusu yukarı kaldırmak için negatif basınçla akciğerlerdeki aşırı mukusun giderilmesine yardımcı olabilir. Hayati kapasite normalin yüzde 30'unun altına düşmeye devam ederse, daha fazla yardım için gün içinde bir volüm ventilatörüne/solunum cihazına da ihtiyaç duyulabilir. Kişi gün içinde gerektiğinde ventilatör/solunum cihazını kullanma süresini kademeli olarak artıracaktır. Ancak solunum cihazına ihtiyaç duymayan 20'li yaşlarında hastalığı olan insanlar da var.
prognoz
Duchenne müsküler distrofisi, sonunda tüm gönüllü kasları etkileyen ve daha sonraki aşamalarda kalp ve solunum kaslarını tutan, nadir görülen ilerleyici bir hastalıktır. Yaşam beklentisinin 25-26 civarında olduğu tahmin edilmektedir, ancak bu değişmektedir. Mükemmel tıbbi bakımla erkekler genellikle 30'lu yaşlarına kadar yaşarlar. Paris, Maine'den David Hatch , hastalığa sahip dünyanın en yaşlı insanı olabilir; o 58 yaşında.
DMD'li kişilerde en yaygın doğrudan ölüm nedeni solunum yetmezliğidir . Mekanik ventilasyon ve trakeotomi prosedürleri gibi tedaviden kaynaklanan komplikasyonlar da bir endişe kaynağıdır. Bir sonraki önde gelen ölüm nedeni, dilate kardiyomiyopatinin neden olduğu kalp yetmezliği gibi kalple ilgili durumlardır . Solunum desteği ile ortalama hayatta kalma yaşı 40'a ulaşabilir. Nadir durumlarda, DMD'li kişilerin tekerlekli sandalyelerde ve yataklarda uygun konumlandırma ve ventilatör desteği kullanımı ( trakeostomi yoluyla) ile kırklı yaşlarına veya ellili yaşlarının başlarına kadar hayatta kaldıkları görülmüştür. veya ağızlık), hava yolu temizliği ve kalp ilaçları. Daha sonraki yaşam bakımı için gerekli desteklerin erken planlanması, DMD'li kişiler için daha uzun ömürlü olduğunu göstermiştir.
Tuhaf bir şekilde, Duchenne kas distrofisinin mdx fare modelinde, distrofin eksikliği, artan kalsiyum seviyeleri ve iskelet kası miyonekrozu ile ilişkilidir. İçsel laringeal kasları (ILMS) korunmakta olup miyonekroz uğramaz. ILM'ler, diğer kaslara kıyasla kalsiyum değişiklikleriyle daha iyi başa çıkma kabiliyetini düşündüren bir kalsiyum düzenleme sistemi profiline sahiptir ve bu, benzersiz patofizyolojik özellikleri için mekanik bir içgörü sağlayabilir. ILM, çeşitli klinik senaryolarda kas kaybının önlenmesi ve tedavisi için yeni stratejilerin geliştirilmesini kolaylaştırabilir. Ek olarak, Duchenne müsküler distrofisi olan hastalarda plazma lipoprotein seviyeleri de yükselmiştir, bu da hastalarda birincil bir dislipidemi durumu anlamına gelir.
epidemiyoloji
DMD, en yaygın kas distrofisi türüdür; doğumda yaklaşık 5.000 erkekten birini etkiler.
ABD'de, 2010 yılında yapılan bir araştırma, Hispanik olmayan Beyazlar ve Hispanik olmayan Siyahlara kıyasla, DMD yaşı beş ila elli dört arasında değişen Hispanik olanların daha yüksek bir miktarını gösterdi.
Tarih
Hastalık ilk olarak 1834'te Napolili doktor Giovanni Semmola ve 1836'da Gaetano Conte tarafından tanımlanmıştır. Bununla birlikte, DMD adını Paraplegie hypertrophique adlı kitabının 1861 baskısında yazan Fransız nörolog Guillaume-Benjamin-Amand Duchenne'den (1806-1875) almıştır. de l'enfance de Reason serebral , bu duruma sahip bir çocuğun vakasını anlattı ve detaylandırdı. Bir yıl sonra, Album de Photographyies pathologiques'inde hastasının fotoğraflarını sundu . 1868'de, etkilenen diğer 13 çocuğun hesabını verdi. Duchenne, mikroskopik inceleme için canlı bir hastadan doku almak için biyopsi yapan ilk kişiydi.
Önemli vakalar
Alfredo ("Dino", "Alfredino") Ferrari (Ocak 1932'de Modena'da doğdu ), Enzo Ferrari'nin oğlu, 1955'in sonunda F2 modeli için 1.5 L DOHC V6 motorunu tasarladı. Ancak Dino, motorun üretildiğini hiç görmedi: 30 Haziran 1956'da Modena'da 24 yaşında, adaşı Dino ve Fiat Dino yapılmadan önce öldü .
Rapçi Darius Weems hastalığa sahipti ve ününü farkındalık yaratmak ve tedavi için fon sağlamak için kullandı. 27 yaşında öldü (kardeşi de 19 yaşında ölümüne kadar hastalıktan acı çekti). Darius Batıya Gidiyor filmi, Weems'in büyüme yolculuğunu ve hastalığa sahip olmayı kabullenmeyi belgeliyor.
Jonathan Evison'ın 2012'de yayınlanan The Revised Fundamentals of Caremaking adlı romanı, hastalığa yakalanmış genç bir adamı tasvir ediyordu . 2016'da Netflix , romana dayanan bir film olan The Fundamentals of Caring'i yayınladı .
Araştırma
Mevcut araştırmalar, ekson atlama , kök hücre replasman tedavisi, analog yukarı regülasyonu, gen replasmanı ve hastalığın ilerlemesini yavaşlatmak için destekleyici bakımı içerir.
Distrofin veya utrofin yapma kabiliyetini geri kazandıran ilaçları bulmak için çabalar devam etmektedir. Diğer çabalar arasında kalsiyum iyonlarının kas hücrelerine girişini engellemeye çalışmak yer alır.
Ekson atlama
DNA'nın yapısal analogları olan antisens oligonükleotitler (oligolar), DMD'li kişilerin %10'u için potansiyel bir tedavinin temelidir. Bileşikler, protein üretimi için RNA'ya kopyalandığında distrofin geninin hatalı kısımlarının atlanmasına izin vererek, proteinin hala kesilmiş fakat daha işlevsel bir versiyonunun üretilmesine izin verir. Anlamsız bastırma tedavisi olarak da bilinir.
İki tür antisens oligo, 2'-0-metil fosforotiyoat oligoları ( drisapersen gibi ) ve Morfolino oligoları ( eteplirsen gibi ), geçici yarar kanıtlarına sahiptir ve üzerinde çalışılmaktadır. Eteplirsen, ekson 51'i atlamayı hedefliyor. "Örnek olarak, ekson 51'i atlamak, tüm erkek çocukların ~% 15'inin okuma çerçevesini geri yükler. silinen tüm DMD erkeklerinin %70'inden fazlası ile ilgilenir." Bu, vakaların yaklaşık yüzde 1.5'ini temsil ediyor.
Olan kişiler Becker müsküler distrofi DMD daha hafif olduğunu, normal distrofin daha kısa olmasına rağmen işlevseldir distrofin bir form var. 1990 yılında İngiltere ve ark. hafif Becker müsküler distrofisi olan bir hastada distrofin için kodlama bölgesinin %46'sından yoksun olduğunu fark etti. Distrofinin bu işlevsel, ancak kesik formu, daha kısa distrofinin hala terapötik olarak faydalı olabileceği fikrini doğurdu. Aynı zamanda, Kole ve ark. antisens oligonükleotidler (AON'ler) ile ön mRNA'yı hedefleyerek modifiye eklemeye sahipti. Kole, beta-talasemi hastalarından alınan hücrelerde yanlış eklemeyi düzeltmek için ekleme hedefli AON'leri kullanarak başarı gösterdi Wilton'ın grubu, kas distrofisi için ekzon atlama testini yaptı.
Gen tedavisi
Araştırmacılar, Duchenne kas distrofisine (DMD) yol açan bir mutasyonu düzeltmek için bir gen düzenleme yöntemi üzerinde çalışıyorlar. Araştırmacılar , DNA'daki distrofin genindeki bir mutasyonu kesin olarak kaldırabilen ve vücudun DNA onarım mekanizmalarının onu genin normal bir kopyasıyla değiştirmesine izin veren CRISPR/Cas9 aracılı genom düzenleme adı verilen bir teknik kullandılar . Bunun diğer gen terapisi tekniklerine göre yararı, bir gendeki "kusuru" geçici olarak "işlevsel" bir gen eklemek yerine kalıcı olarak düzeltebilmesidir.
CRISPR/Cas9 sistemi aracılığıyla genom düzenleme şu anda insanlarda mümkün değildir. Bununla birlikte, teknolojideki gelişmeler sayesinde, gelecekte DMD için tedaviler geliştirmek için bu tekniği kullanmak mümkün olabilir. 2007'de araştırmacılar, Duchenne MD için dünyanın ilk klinik (viral aracılı) gen tedavisi denemesini yaptılar.
Biostrofin , Duchenne musküler distrofi ve Becker musküler distrofi tedavisinde gen tedavisi için bir dağıtım vektörüdür .
Referanslar
daha fazla okuma
- Birnkrant DJ, Bushby K, Bann CM, Apkon SD, Blackwell A, Brumbaugh D, et al. (Mart 2018). "Duchenne kas distrofisinin teşhisi ve yönetimi, bölüm 1: teşhis ve nöromüsküler, rehabilitasyon, endokrin ve gastrointestinal ve beslenme yönetimi" . Lancet Nörol . 17 (3): 251–267. doi : 10.1016/S1474-4422(18)30024-3 . PMC 5869704 . PMID 29395989 .
- Birnkrant DJ, Bushby K, Bann CM, Alman BA, Apkon SD, Blackwell A, et al. (Nisan 2018). "Duchenne kas distrofisinin teşhisi ve yönetimi, bölüm 2: solunum, kalp, kemik sağlığı ve ortopedik yönetim" . Lancet Nörol . 17 (4): 347-361. doi : 10.1016/S1474-4422(18)30025-5 . PMC 5889091 . PMID 29395990 .
Dış bağlantılar
- Musküler Distrofiler de Curlie
- CDC'nin Doğum Kusurları ve Gelişimsel Engelliler Ulusal Merkezi (daha önce aşağıda "Duchenne/Becker Musküler Distrofi, NCBDDD" olarak listelenmiştir) CDC'de
- Genler ve Hastalık Sayfa at NCBI'deki
| sınıflandırma | |
|---|---|
| Dış kaynaklar |