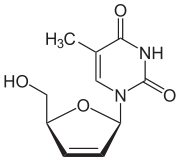
Stavudin - Stavudine
 | |
 | |
| Klinik veriler | |
|---|---|
| Ticari isimler | Zerit |
| Diğer isimler | 2 ′, 3′-didehidro-2 ′, 3′-dideoksitimidin |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a694033 |
| Lisans verileri | |
| Gebelik kategorisi |
|
Yönetim yolları |
Ağızla |
| ATC kodu | |
| Hukuki durum | |
| Hukuki durum | |
| Farmakokinetik veriler | |
| Biyoyararlanım | >% 80 |
| Protein bağlama | İhmal edilebilir |
| Metabolizma | Böbrek eliminasyonu (~% 40) |
| Eliminasyon yarı ömrü | 0.8-1.5 saat (yetişkinlerde) |
| Tanımlayıcılar | |
| |
| CAS numarası | |
| PubChem Müşteri Kimliği | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| NIAID ChemDB | |
| CompTox Kontrol Paneli ( EPA ) | |
| ECHA Bilgi Kartı |
100.169.180 |
| Kimyasal ve fiziksel veriler | |
| Formül | C 10 H 12 N 2 O 4 |
| Molar kütle | 224.216 g · mol −1 |
| 3B modeli ( JSmol ) | |
| |
| |
| (Doğrulayın) | |
Diğerlerinin yanı sıra Zerit markası altında satılan Stavudin ( d4T ), HIV / AIDS'i önlemek ve tedavi etmek için kullanılan bir antiretroviral ilaçtır . Genellikle diğer antiretroviraller ile kullanılması tavsiye edilir. Bir iğne batması yaralanması veya diğer potansiyel maruziyetten sonra önleme için kullanılabilir . Ancak bu birinci basamak bir tedavi değildir. Ağız yoluyla verilir.
Yaygın yan etkiler arasında baş ağrısı , ishal, kusma, döküntü ve periferik sinir sorunları bulunur. Şiddetli yan etkiler arasında yüksek kan laktat , pankreatit ve genişlemiş karaciğer bulunur . Genellikle hamilelikte tavsiye edilmez . Stavudin, nükleozid analog ters transkriptaz inhibitörü (NRTI) ilaç sınıfındadır.
Stavudin ilk olarak 1966'da tanımlandı ve 1994'te Amerika Birleşik Devletleri'nde kullanım için onaylandı. Jenerik bir ilaç olarak mevcuttur.
Tıbbi kullanımlar
Stavudin, HIV-1 enfeksiyonunun tedavisinde kullanılır , ancak bir tedavi değildir. Normalde ilk tedavi olarak tavsiye edilmez. Stavudin, virüsle ya işte (örneğin iğne batması) ya da enfekte kan ya da diğer vücut sıvılarına maruz kalma yoluyla temas ettikten sonra HIV-1 enfeksiyonu geliştirme riskini de azaltabilir. Enfeksiyonun daha iyi kontrolü ve HIV komplikasyonlarının azaltılması için her zaman diğer HIV ilaçlarıyla birlikte kullanılır.
Dünya Sağlık Örgütü (WHO), yüksek toksisite seviyeleri nedeniyle stavudinin aşamalı olarak kaldırılmasını önermektedir. İlaç kullanılması gerekiyorsa, yan etkilerin oluşumunu azaltmak için düşük dozaj kullanılması önerilir; ancak, 2015 Cochrane incelemesi , yüksek ve düşük doz rejimleri arasında net bir avantaj bulamamıştır.
Hamilelik ve emzirme
Hayvan çalışmalarında stavudinin fetüsü etkilediği gösterilmiştir, ancak insan çalışmalarından hiçbir veri bulunmamaktadır. Bu nedenle gebe kadınlara, yalnızca potansiyel faydalar fetüse yönelik potansiyel zarardan ağır basarsa stavudin verilmelidir. Ek olarak , stavudin ve didanozinin diğer antiviral ajanlarla kombinasyon tedavisi alan hamile kadınlarda ölümcül laktik asidoz vakaları bildirilmiştir .
Hastalık Kontrol ve Önleme Merkezleri , HIV-enfekte annelerin anne sütü ile HIV bulaşma riskini önlemek amacıyla, bebeklerini emzirmek öneririz. İnsan anne sütü için veri bulunmamakla birlikte, stavudinin hayvan anne sütüne geçtiğine dair kanıtlar da vardır.
Çocuk
Stavudin, doğumdan ergenliğe kadar HIV ile enfekte olan çocuklarda kullanım için güvenlidir. Olumsuz etkiler ve güvenlik profili yetişkinlerle aynıdır.
Yaşlı
65 yaş ve üstü HIV ile enfekte yetişkinlerde stavudin kullanımına ilişkin veri bulunmamaktadır. Bununla birlikte, 65 yaşın üzerindeki 12.000 kişinin% 30'unda periferik nöropati gelişti . Ek olarak, yaşlıların böbrek fonksiyonlarının azalması daha olası olduğundan, toksik yan etkilere sahip olma olasılıkları daha yüksektir.
Olumsuz olaylar
Yaygın yan etkiler
- Mide bulantısı
- Kusma
- İshal
- Baş ağrısı
- Mide bulantısı
Ciddi yan etkiler
- Periferik nöropati
- Laktik asit
- Pankreatit
- Hepatotoksisite
- Hepatomegali ile steatoz
- Lipoatrofi / lipodistrofi (yağın yeniden dağılımı / birikimi)
Bu ciddi yan etkilerin gelişmesi için bireyler izlenmektedir. Periferik nöropati gelişiminin doza bağlı olduğu gösterilmiştir ve ilaç kesilirse çözülebilir. İlerlemiş HIV-1 hastalığı, periferik nöropati öyküsü olan veya nöropati ile ilişkili diğer ilaçları kullanan kişiler bu yan etkiyi daha sık geliştirir.
Stavudinin laboratuar testinde genotoksik olduğu gösterilmiştir , ancak klinik dozlarda kanserojen etkileri yoktur. Yüksek dozlarda uygulandığında hiperlaktatemi, kemik mineral yoğunluğu (BMD) kaybı, ekstremite yağında azalma ve trigliseritlerde artış bulundu. Aynı zamanda lipodistrofi'ye neden olma olasılığı en yüksek antiviral ilaçlardan biridir ve bu nedenle gelişmiş ülkelerdeki çoğu hasta için artık uygun bir tedavi olarak kabul edilmemektedir.
HLA-B * 4001, Tayland'da yapılan bir çalışmaya göre, stavudinin süresini önlemek veya kısaltmak için hangi hastaların stavudine bağlı lipodistrofi geliştireceğini tahmin etmek için genetik bir işaret olarak kullanılabilir.
Hindistan gibi kaynakların zayıf olduğu ortamlarda hala birinci basamak tedavide ilk seçenek olarak kullanılmaktadır. Sadece periferik nöropati veya gebelik gelişmesi durumunda, bir sonraki seçenek olan zidovudin ile değiştirilir . Daha önce tedavi görmemiş hastalarda doz titrasyonunun güvenliği ve etkinliği bildirilmemiştir. Yalnızca, sürekli virolojik baskılanması olan hastalarda bildirilmiştir. Bu bulgular, yüksek viral yüke sahip ART denenmemiş hastalarda kullanılan Stavudin için genelleştirilmemiştir.
30 Kasım 2009 Pazartesi günü, Dünya Sağlık Örgütü "[WHO], ülkelerin uzun vadeli, geri döndürülemez yan etkileri nedeniyle Stavudin veya d4T kullanımını aşamalı olarak kaldırmalarını tavsiye etmektedir. Düşük maliyeti ve yaygın bulunabilirliği nedeniyle gelişmekte olan ülkelerde alternatif tedavi. Zidovudin (AZT) veya tenofovir (TDF) daha az toksik ve eşit derecede etkili alternatifler olarak önerilmektedir. "
Hareket mekanizması
Stavudine nükleosıttır analoğu ve timidin . Hücresel kinazlar tarafından aktif bir trifosfata fosforile edilir . Stavudin trifosfat , doğal substrat olan timidin trifosfat ile rekabet ederek HIV'in ters transkriptazını inhibe eder . Ters transkriptaz , virüsün genetik materyalini konakçının DNA'sına yerleştirmek için RNA'sının bir DNA kopyasını yapmak için kullandığı enzimdir. Stavudin trifosfat, DNA sarmalına dahil edildikten sonra DNA replikasyonunun sona ermesine neden olur .
Farmakokinetik
Emilim: Stavudin hızlı absorpsiyona ve iyi bir oral biyoyararlanıma sahiptir (F = 0.86).
Dağılım: Stavudin kandaki proteinlere bağlanmaz.
Metabolizma: Stavudinin klirensi, karaciğer metabolizmasından minimal düzeyde etkilenir. Oksidasyon ve glukuronidasyon , küçük metabolitler üretir.
Eliminasyon: Stavudin çoğunlukla idrarda ve çoğunlukla değişmemiş haliyle atılır.
İlaç etkileşimleri
Stavudinin hücre içi fosforilasyonunu inhibe edebileceği için eş zamanlı zidovudin kullanımı önerilmez . Diğer anti-HIV ilaçları bu özelliğe sahip değildir.
Stavudin, proteine bağlı değildir ve majör sitokrom P450 izoformlarını inhibe etmez. Bu nedenle, bu yollarla metabolize edilen ilaçlarla veya proteine bağlı ilaçlarla önemli ilaç etkileşimleri olası değildir.
Tarih
Stavudine ilk olarak 1960'larda Jerome Horwitz tarafından yaratıldı ve orijinal olarak D4T olarak adlandırıldı. 1980'lerde AIDS salgını meydana geldiğinde, William Prusoff ve Dr. Tai-Shun Lin, Stavudine'nin anti-HIV özelliklerini keşfettiler. İlaç şirketi Bristol-Myers Squibb , ilacı Zerit ticari adı altında üretmektedir.
Ayrıca, ajansın Stavudine'i onaylanmadan önce hastalara sunmasına izin veren ABD Gıda ve İlaç Dairesi (FDA) tarafından 1992 yılında paralel izleme statüsü verilen ilk ilaçtır . Stavudine, FDA'nın hızlandırılmış onay süreci kapsamında sunuldu. Bu süreç boyunca, stavudıne etkinliği üzerindeki etkisi ölçüldü belirteç , CD4 yerine klinik uç noktalarının,. FDA, CD4 hücre sayısındaki artışın, ilacın AIDS ve HIV enfeksiyonuna karşı ne kadar etkili olacağının bir göstergesi olduğu sonucuna vardı. Stavudin, 27 Haziran 1994'te FDA tarafından AIDS ve HIV enfeksiyonunun tedavisi için onaylanan dördüncü ilaçtı. Onaylandıktan sonra bile, ilacın klinik yararını değerlendirmek için çalışmalar sürdürüldü. Klinik faydalara dair herhangi bir gösterge yoksa hızlandırılmış onay geri çekilebilir.
2018 yılında Mylan Pharmaceuticals, stavudin 20 mg, 30 mg ve 40 mg kapsül üretimini durdurdu.
Referanslar
Dış bağlantılar
- "Stavudine" . İlaç Bilgi Portalı . ABD Ulusal Tıp Kütüphanesi.
