Ataluren - Ataluren
 | |
 | |
| Klinik veriler | |
|---|---|
| Ticari isimler | Translarna |
| Diğer isimler | PTC124 |
| AHFS / Drugs.com | Uluslararası İlaç İsimleri |
| Lisans verileri | |
Yönetim yolları |
Ağızla |
| ATC kodu | |
| Hukuki durum | |
| Hukuki durum | |
| tanımlayıcılar | |
| |
| CAS numarası | |
| PubChem Müşteri Kimliği | |
| IUPHAR/BPS | |
| İlaç Bankası | |
| Kimyasal Örümcek | |
| ÜNİİ | |
| fıçı | |
| chebi | |
| CHEMBL | |
| CompTox Panosu ( EPA ) | |
| ECHA Bilgi Kartı |
100.132.097 |
| Kimyasal ve fiziksel veriler | |
| formül | C 15 H 9 F N 2 O 3 |
| Molar kütle | 284.246 g·mol -1 |
| 3B model ( JSmol ) | |
| |
| |
|
| |
Translarna markası altında satılan Ataluren , Duchenne kas distrofisi tedavisi için bir ilaçtır . PTC Therapeutics tarafından tasarlanmıştır .
tıbbi kullanım
Ataluren, Avrupa Birliği'nde , distrofin geninde saçma bir mutasyona sahip olan , yürüyebilen ve beş yaşından büyük Duchenne müsküler distrofisi olan kişileri tedavi etmek için kullanılmaktadır .
Kontrendikasyonlar
Hamile veya emziren kişiler ataluren almamalıdır.
Yan etkiler
Klinik çalışmalarda ataluren alan kişilerin %10'undan fazlası kusma yaşamıştır; %5'ten fazlası ishal, mide bulantısı, baş ağrısı, üst karın ağrısı ve şişkinlik yaşadı; İnsanların %1 ila %5'i iştah azalması ve kilo kaybı, yüksek trigliserit seviyeleri , yüksek tansiyon, öksürük, burun kanaması, karın rahatsızlığı, kabızlık, kızarıklık, kollarında, bacaklarında ve göğüs kaslarında ağrı, idrarlarında kan yaşadı. , idrar kaçırma ve ateş.
Etkileşimler
Ataluren alan birine aminoglikozidler , etki mekanizmasına müdahale ettikleri için verilmemelidir. Dikkat neden ilaçlar kullanılmalıdır UGT1A9 veya substratları olduğu OAT1 , OAT3 veya OATP1B3 .
Farmakoloji
Çok sayıda çalışma atalurenin biyolojik hedefini belirlemede başarısız olsa da, ateşböceği lusiferazını bağladığı ve stabilize ettiği keşfedildi, böylece okuma testi üzerinde yanlış bir pozitif etki yarattığı mekanizmayı açıkladı.
Ataluren'in, aşağı akış transkripsiyon , mRNA işleme üzerinde belirgin bir etkisi olmayan anlamsız kodonların bulunduğu bölgeye belirli yakın akraba tRNA'nın yerleştirilmesini teşvik ederek ribozomları erken durdurma kodonlarına ("okuma" olarak adlandırılan bir etki) karşı daha az duyarlı hale getirdiği düşünülmektedir. mRNA'nın veya elde edilen proteinin stabilitesi, böylece mutasyona uğramamış endojen ürüne benzer fonksiyonel bir protein meydana getirir. Durma kodonu 'UGA' için özellikle iyi çalışıyor gibi görünüyor.
Çalışmalar, ataluren tedavisinin, Duchenne kas distrofisi için erken durdurma kodon mutasyonunu içeren insan ve fare birincil kas hücrelerinde tam uzunluktaki distrofin proteininin ekspresyonunu arttırdığını ve çizgili kas fonksiyonunu kurtardığını göstermiştir. Kistik fibroz için erken durdurma kodon mutasyonuna sahip farelerde yapılan çalışmalar, artan CFTR protein üretimi ve fonksiyonunu göstermiştir. Bu çalışmayı genişleterek, maya ve insan hücreleriyle yapılan mekanik bir çalışma, CFTR proteininde spesifik kodon pozisyonlarında spesifik amino asit ikameleriyle sonuçlanan ataluren aracılı standart olmayan kodon-antikodon baz eşleşmelerinin ayrıntılarını aydınlatmıştır.
Ataluren'in onayına ilişkin Avrupa İlaç Ajansı incelemesi, "mevcut klinik olmayan verilerin, önerilen etki mekanizmasını desteklemek ve atalurenin erken durdurma kodonları için seçiciliğine ilişkin daha önceki endişeleri hafifletmek için yeterli kabul edildiği" sonucuna varmıştır.
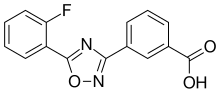
Kimya
Ataluren bir oksadiazoldür ; kimyasal adı 3-[5-(2-Fluorofenil)-1,2,4-oksadiazol-3-il]benzoik asittir.
Tarih
Ataluren, PTC Therapeutics'teki bilim adamları tarafından, Lee Sweeney'nin Pennsylvania Üniversitesi'ndeki laboratuvarıyla işbirliği içinde keşfedildi ve başlangıçta Parent Project Musküler Distrofi tarafından finanse edildi. Ekip , mutasyona uğramış genler tarafından ifade edilen protein miktarını artıran bileşikleri tanımlamak için bir kimyasal kütüphanenin fenotipik taramasını kullandı ve ardından bu ilacı oluşturmak için ekrandaki isabetlerden birini optimize etti. Birçok hücre tabanlı taramanın sonuçlarında olduğu gibi, atalurenin biyolojik hedefi bilinmemektedir.
Faz I klinik denemeleri 2004 yılında başlamıştır.
2010 yılında, PTC Therapeutics, Duchenne musküler distrofi için faz 2b klinik denemesinin ön sonuçlarını yayınladı ve katılımcılar, 48 haftalık denemeden sonra altı dakikalık yürüme mesafesinde önemli bir gelişme göstermedi. Bu başarısızlık , ilacı takip etmek için Genzyme ile 100 milyon dolarlık bir anlaşmanın feshedilmesiyle sonuçlandı .
Mayıs 2014'te ataluren , Avrupa İlaç Ajansı'nın (EMA) Beşeri Tıbbi Ürünler Komitesi'nden (CHMP) olumlu bir görüş aldı ve Ağustos 2014'te saçma mutasyon Duchenne kas distrofisi olan kişileri tedavi etmek için Avrupa Komisyonu'ndan pazar izni aldı; doğrulayıcı bir faz III klinik deney gerekliydi. Aralık ayına kadar Almanya, Fransa, İtalya, Danimarka, İspanya ve diğer bir dizi Avrupa Birliği ülkesinde piyasadaydı.
Şubat 2016'da FDA , ataluren'in birincil son noktasını kaçırdığı bir klinik araştırmaya dayanan ataluren için PTC Therapeutics yeni ilaç başvurusunu kabul etmeyi reddetti ; PTC temyize gitti ve FDA Ekim 2016'da tekrar reddetti.
Temmuz 2016'da NHS İngiltere, Translarna için beş yıllık bir MAA aracılığıyla İngiltere'deki Translarna'ya geri ödemeli hasta erişimi sağlayan bir Yönetilen Erişim Anlaşması (MAA) kabul etti. Bu, Nisan 2016'da Ulusal Sağlık ve Bakım Mükemmelliği Enstitüsü'nün (NICE) olumlu bir tavsiyesinin ardından geldi ve PTC ve NHS İngiltere'nin MAA şartlarını tamamlamasına tabi oldu. NICE, son kılavuzunu iki ay içinde takip eden hastalar için MAA'nın uygulanmasıyla Temmuz ayında yayınladı.
Mart 2017'de PTC, Faz III denemelerinde etkinlik eksikliği nedeniyle kistik fibroz için ataluren gelişimini sonlandırdı.
Ayrıca bakınız
- Biostrofin , rimeporid ve eteplirsen , Duchenne musküler distrofisine karşı diğer ilaçlar
- Ivacaftor ve lumacaftor , Vertex Pharmaceuticals tarafından geliştirilmekte olan kistik fibrozise karşı diğer ilaçlar
Referanslar
Dış bağlantılar
- "Ataluren" . İlaç Bilgi Portalı . ABD Ulusal Tıp Kütüphanesi.
