hERG - hERG
hERG ( s uman e Ther-a-go-go - R sevinçli G bir gen (olup en) KCNH2 ) olup olarak bilinen bir protein için kodlama K v 11.1 , alfa alt-birimi , bir bir potasyum iyon kanalı . Bu iyon kanalı (bazen basitçe 'hERG' olarak adlandırılır) en iyi kalbin elektriksel aktivitesine katkısıyla bilinir : hERG kanalı , kalbin atışını koordine etmeye yardımcı olan kardiyak aksiyon potansiyelindeki repolarize edici I Kr akımına aracılık eder .
Bu kanalın hücre zarı boyunca elektrik akımını iletme yeteneği, ilaçların uygulanması veya bazı ailelerde nadir görülen mutasyonlar tarafından engellendiğinde veya tehlikeye girdiğinde, uzun QT sendromu adı verilen potansiyel olarak ölümcül bir hastalığa neden olabilir . Tersine, bu kanallardan akımı artıran genetik mutasyonlar, ilgili kalıtsal kalp ritmi bozukluğu Kısa QT sendromuna yol açabilir . Piyasadaki klinik olarak başarılı bir dizi ilaç, hERG'yi inhibe etme, QT'yi uzatma ve potansiyel olarak ölümcül kalp atış düzensizliğine ( torsades de pointes adı verilen ventriküler taşiaritmi ) yol açma eğilimine sahiptir . Bu, hERG inhibisyonunu, ilaç geliştirme sırasında kaçınılması gereken önemli bir anti-hedef haline getirmiştir .
hERG ayrıca sinir sisteminin bazı hücrelerinin işlevlerini modüle etmekle ve lösemik hücrelerde kanser benzeri özellikleri oluşturmak ve sürdürmekle de ilişkilendirilmiştir.
İşlev
hERG, potasyum (K + ) iyonlarını kalbin kas hücrelerinden ( kardiyak miyositler ) dışarı ileten iyon kanalı proteinlerinden birinin ('hızlı' gecikmeli doğrultucu akımı ( I Kr )) büyük bölümünü oluşturur ve bu akım, Kardiyak aksiyon potansiyeli sırasında hücre zarının dinlenme durumuna ( repolarizasyon ) dönüşün doğru şekilde zamanlanmasında kritik öneme sahiptir . Bazen ilaçların farmakolojik etkilerinden bahsederken "hERG kanalları" ve I Kr terimleri birbirinin yerine kullanılır, ancak teknik anlamda "hERG kanalları" yalnızca laboratuvardaki bilim adamları tarafından yapılabilir; Resmi terimlerle, hERG'yi içeren vücutta doğal olarak oluşan kanallara, o hücre tipinde ölçülen elektrik akımının adıyla atıfta bulunulur, bu nedenle, örneğin kalpte, doğru ad I Kr'dir . Terminoloji bu fark ileten kanalları olup olmadığı konusunda tartışma daha açık hale I Kr diğer alt-birimleri (örneğin, beta alt-birimlerinin) içerir veya kanallar farklı türde (karışımını ihtiva edip izoform ) hERG, ancak ilk olarak keşfedilen bir form hERG deneysel önce (yani, hERG yoksun hücreler içine aktarılır ve heterolog ekspresyonu), kalp 'hızlı' rektifayer akım (gecikmiş özelliklerinin bir potasyum iyon kanalı oluşturulur ve bu kanal bir çok imzaya sahip I Kr dahil), bir Kr ' Membranın repolarizasyonuna yanıt olarak kanalın 'paradoksal yeniden canlanan akım' üretmesiyle sonuçlanan içe doğru düzeltme.
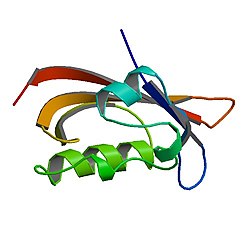
Yapı
hERG için X-ışını kristalografisine dayalı ayrıntılı bir atomik yapı henüz mevcut değildir, ancak yapılar son zamanlarda elektron mikroskobu ile çözülmüştür. Laboratuvarda heterolog olarak eksprese edilen hERG potasyum kanalı, kanalın plazma membranındaki gözenekini oluşturan 4 özdeş alfa alt birimini içerir . Her bir hERG alt birimi, S1-S6 olarak numaralandırılmış 6 transmembran alfa sarmalından , S5 ve S6 arasında yer alan bir gözenek sarmalından ve sitoplazmik olarak yerleştirilmiş N- ve C-terminallerinden oluşur . S4 sarmalı , her 3. pozisyonda pozitif yüklü bir arginin veya lizin amino asit kalıntısı içerir ve iletken ve iletken olmayan durumlar arasındaki konformasyonları değiştirerek kanalın voltaj değişikliklerine yanıt vermesine izin veren voltaja duyarlı bir sensör olarak hareket ettiği düşünülmektedir. 'geçit'). S5 ve S6 sarmalları arasında, hücre dışı bir döngü ("taret" olarak bilinir) ve hücre dışı olarak başlayıp biten, ancak plazma zarına dönen "gözenek halkası" vardır; bir kanaldaki hERG alt birimlerinin her biri için gözenek döngüsü, iyon ileten gözenekle karşı karşıyadır ve diğer 3 alt birimin karşılık gelen döngülerine bitişiktir ve birlikte, kanal gözeneğinin seçicilik filtre bölgesini oluştururlar. Seçicilik dizisi, SVGFG, bakteriyel KcsA kanallarında bulunana çok benzer . hERG için tam bir kristal yapı henüz mevcut olmasa da, sitoplazmik N-terminali için deaktivasyon hızını yavaşlatan bir PAS alanı (aminoasit 26-135) içerdiği gösterilen bir yapı bulunmuştur .
Genetik
Bu kanaldaki fonksiyon kaybı mutasyonları uzun QT sendromuna (LQT2) yol açabilirken, fonksiyon kazancı mutasyonları kısa QT sendromuna yol açabilir . Her iki klinik bozukluk da , kardiyak aksiyon potansiyelinin repolarizasyon bozuklukları nedeniyle potansiyel olarak ölümcül kardiyak aritmiler (örneğin, torsades de pointes ) riskine yol açabilen iyon kanalı işlev bozukluğundan ( kanalopatiler olarak adlandırılır ) kaynaklanır. Uzun QT sendromu için, kısa QT sendromundan çok daha fazla hERG mutasyonu tanımlanmıştır.
İlaç etkileşimleri
Bu kanal aynı zamanda ilaç bağlanmasına ve hücre dışı potasyum seviyelerinin azalmasına karşı da duyarlıdır, bunların her ikisi de kanal fonksiyonunun azalmasına ve ilaca bağlı (edinilmiş) uzun QT sendromuna neden olabilir . QT uzamasına neden olabilen ilaçlar arasında en yaygın olanları antiaritmikler (özellikle Sınıf 1A ve Sınıf III), antipsikotik ajanlar ve bazı antibiyotikleri (kinolonlar ve makrolidler dahil) içerir.
Kardiyak yan etkiler için başka potansiyel hedefler olmasına rağmen, edinilmiş QT uzaması ile ilişkili ilaçların büyük çoğunluğunun hERG potasyum kanalı ile etkileşime girdiği bilinmektedir. Bu fenomenin ana nedenlerinden biri, hERG kanalının daha büyük iç vestibülüdür, bu nedenle birçok farklı ilaç sınıfına bu potasyum kanalını bağlamak ve bloke etmek için daha fazla alan sağlar.
hERG içeren kanallar amiodaron tarafından bloke edilir .
İlaç geliştirme konuları
QT aralığını uzatan ilaçların belgelenmiş potansiyeli nedeniyle, Amerika Birleşik Devletleri Gıda ve İlaç İdaresi, klinik öncesi ilaç geliştirme sırasında kardiyak güvenlik profilinin oluşturulması için öneriler yayınladı: ICH S7B. CHMP/ICH/423/02 olarak yayınlanan, CHMP tarafından Mayıs 2005'te kabul edilen, insan farmasötikleri tarafından gecikmiş ventriküler repolarizasyon (QT aralığı uzaması) potansiyelinin klinik olmayan değerlendirmesi. Klinik öncesi hERG çalışmaları GLP ortamında gerçekleştirilmelidir .
adlandırma
hERG geni ilk olarak Jeff Warmke ve Barry Ganetzky, ardından her ikisi de Wisconsin-Madison Üniversitesi'nde bir makalede adlandırılmış ve tanımlanmıştır . hERG geni, Drosophila sineğinde bulunan Ether-à-go-go geninin insan homologudur ; Ether-à-go-go , 1960'larda William D. Kaplan ve William E. Trout, III tarafından Duarte, California'daki City of Hope Hastanesindeyken seçildi . Ether-à-go genindeki mutasyonlara sahip sinekler eter ile uyuşturulduğunda , West Hollywood, California'daki o zamanlar popüler olan Whiskey A Go-Go gece kulübündeki dans gibi bacakları titremeye başlar .
Etkileşimler
HERG'nin YWHAE tarafından kodlanan 14-3-3 epsilon proteini ile etkileşime girdiği gösterilmiştir .
Ayrıca bakınız
Referanslar
daha fazla okuma
- Vincent GM (1998). "Uzun QT sendromunun moleküler genetiği: bayılma ve ani ölüme neden olan genler". Annu. Rev. Med . 49 : 263–74. doi : 10.1146/annurev.med.49.1.263 . PMID 9509262 .
- Ackerman MJ (1998). "Uzun QT sendromu: kalbin iyon kanalı hastalıkları" . Mayo Kliniği. Proc . 73 (3): 250–69. doi : 10.4065/73.3.250 . PMID 9511785 .
- Taglialatela M, Castaldo P, Pannaccione A, Giorgio G, Annunziato L (1998). "Farmakolojik hedefler olarak insan eter-a-gogo ile ilgili gen (HERG) K+ kanalları: şimdiki ve gelecekteki çıkarımlar". Biyokimya. farmakol . 55 (11): 1741–6. doi : 10.1016/S0006-2952(98)00002-1 . PMID 9714291 .
- Bjerregaard P, Gussak I (2005). "Kısa QT sendromu: mekanizmalar, tanı ve tedavi". Nat Clin Pract Cardiovasc Med . 2 (2): 84–7. doi : 10.1038/ncpcardio0097 . PMID 16265378 . S2CID 10125533 .
- Gutman GA, Chandy KG, Grissmer S, Lazdunski M, McKinnon D, Pardo LA, Robertson GA, Rudy B, Sanguinetti MC, Stühmer W, Wang X (2005). "Uluslararası Farmakoloji Birliği. LIII. Voltaj kapılı potasyum kanallarının isimlendirilmesi ve moleküler ilişkileri". farmakol. Rev . 57 (4): 473–508. doi : 10.1124/pr.57.4.10 . PMID 16382104 . S2CID 219195192 .