Sodyum tiyosülfat - Sodium thiosulfate

|
|
|
|

|
|
| İsimler | |
|---|---|
|
IUPAC adı
sodyum tiyosülfat
|
|
| Diğer isimler
Sodyum
hiposülfit Soda hiposülfit |
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| chebi | |
| CHEMBL | |
| Kimyasal Örümcek | |
| ECHA Bilgi Kartı |
100.028.970 |
| E numarası | E539 (asitlik düzenleyiciler, ...) |
|
PubChem Müşteri Kimliği
|
|
| RTECS numarası | |
| ÜNİİ | |
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikler | |
|
Na 2S 2Ö 3 |
|
| Molar kütle | 158.11 g/mol (susuz) 248.18 g/mol (pentahidrat) |
| Dış görünüş | Beyaz kristaller |
| Koku | Kokusuz |
| Yoğunluk | 1.667 g / cc 3. |
| Erime noktası | 48,3 °C (118,9 °F; 321.4 K) (pentahidrat) |
| Kaynama noktası | 100 °C (212 °F; 373 K) (pentahidrat, - 5H 2 O ayrışması) |
| 20,1 g/100 mL (20 °C) 231 g/100 mL (100 °C) |
|
| çözünürlük | alkolde ihmal edilebilir |
|
Kırılma indisi ( n D )
|
1.489 |
| Yapı | |
| monoklinik | |
| Tehlikeler | |
| Güvenlik Bilgi Formu | Harici MSDS |
| R cümleleri (modası geçmiş) | R21 R36 R37 R38 |
| NFPA 704 (ateş elması) | |
| Alevlenme noktası | Yanıcı değil |
| Bağıntılı bileşikler | |
|
Diğer katyonlar
|
Tiyosülfürik asit Lityum tiyosülfat Potasyum tiyosülfat |
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
|
|
|
| Bilgi kutusu referansları | |
Sodyum tiyosülfat ( sodyum tiyosülfat ) bir bir inorganik bileşik formülü ile Na 2 S 2 O 3 . x H 2 O. Tipik olarak beyaz veya renksiz pentahidrat , Na 2 S 2 O 3 ·5 H 2 O olarak mevcuttur . Katı, suda iyi çözünen efloresan (suyu kolayca kaybeder) kristalli bir maddedir.
Sodyum tiyosülfat altın madenciliği , su arıtma , analitik kimya , gümüş bazlı fotoğraf filmi ve baskılarının geliştirilmesi ve tıpta kullanılır . Tiosülfat sodyum tıbbi kullanımları tedavisini içerir siyanür zehirlenmesine ve pityriasis . Bir sağlık sisteminde ihtiyaç duyulan en güvenli ve en etkili ilaçlar olan Dünya Sağlık Örgütü'nün Temel İlaçlar Listesi'nde yer almaktadır .
kullanır
Sodyum tiyosülfat ağırlıklı olarak endüstride kullanılmaktadır. Örneğin, boyaları çözünür löko formlarına dönüştürmek için kullanılır. Aynı zamanda "yün, pamuk, ipek, ...sabunlar, yapıştırıcılar, kil, kum, boksit ve... yemeklik yağlar, yemeklik yağlar ve jelatini" ağartmak için de kullanılır.
Tıbbi kullanımlar
Siyanür zehirlenmesinin tedavisinde sodyum tiyosülfat kullanılmaktadır . Diğer kullanımlar arasında saçkıran ve tinea versicolor'un topikal tedavisi ve hemodiyaliz ve kemoterapinin bazı yan etkilerinin tedavisi yer alır .
fotoğraf işleme
Gümüş halojenürler , örneğin, AgBr , fotografik emülsiyonların tipik bileşenleri, sulu tiyosülfat ile muamele edildikten sonra çözülür. Fotoğrafik bir sabitleyici olarak bu uygulama, John Herschel tarafından keşfedilmiştir . Bu her ikisi için kullanılan filmin ve fotoğraf kağıdı işleme; sodyum tiyosülfat, fotoğrafik bir sabitleyici olarak bilinir ve genellikle orijinal kimyasal adı olan soda hiposülfitinden 'hipo' olarak adlandırılır. Amonyum tiyosülfat , bu uygulama için tipik olarak sodyum tiyosülfat'a tercih edilir.
Klorlu suyun nötralize edilmesi
Akvaryumlarda, yüzme havuzlarında ve kaplıcalarda (örn. süper klorlamanın ardından ) kullanım için klor seviyelerinin düşürülmesi dahil olmak üzere musluk suyunu klordan arındırmak için ve nehirlere salınmadan önce çöken geri yıkama suyunu arıtmak için su arıtma tesislerinde kullanılır. İndirgeme reaksiyonu, iyot indirgeme reaksiyonuna benzer.
Olarak pH değeri test ağartıcı maddeler, sodyum tiosülfat ağartıcının renk giderici etkisini etkisiz hale getirir ve sıvı göstergelerle ağartma çözeltilerinin pH test etmek için bir olanak sağlar. İlgili reaksiyon iyot reaksiyonuna benzer: tiyosülfat hipokloriti ( ağartıcıdaki aktif bileşen ) azaltır ve bunu yaparken sülfata oksitlenir. Tam reaksiyon:
- 4 NaClO + Na
2S
2Ö
3 + 2 NaOH → 4 NaCl + 2 Na
2BU YÜZDEN
4 + H
2Ö
Benzer şekilde, sodyum tiyosülfat brom ile reaksiyona girerek çözeltiden serbest bromu uzaklaştırır. Sodyum tiyosülfat çözeltileri, kimya laboratuvarlarında brom ile çalışırken ve brom, iyot veya diğer güçlü oksitleyicilerin güvenli bir şekilde atılması için yaygın olarak bir önlem olarak kullanılır.
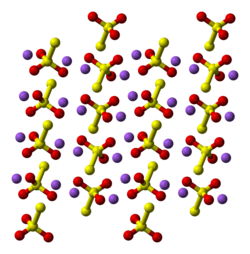
Yapı
Pentahidratın iki polimorfu bilinmektedir. Susuz tuz birkaç polimorf halinde bulunur. Katı halde, tiyosülfat anyonu tetrahedral şekildedir ve kavramsal olarak oksijen atomlarından birinin bir sülfat anyonundaki bir kükürt atomu ile değiştirilmesiyle türetilir . SS mesafesi, terminal kükürtün önemli bir negatif yüke sahip olduğunu ve SO etkileşimlerinin daha fazla çift bağ karakterine sahip olduğunu ima eden tek bir bağı belirtir.
Üretme
Endüstriyel ölçekte, sodyum tiyosülfat esas olarak sodyum sülfür veya kükürt boya imalatının sıvı atık ürünlerinden üretilir.
Laboratuvarda, bu tuz, sulu bir sodyum sülfit çözeltisinin kükürt ile ısıtılmasıyla veya sulu sodyum hidroksit ve kükürtün aşağıdaki denkleme göre kaynatılmasıyla hazırlanabilir :
- 6 NaOH + 4 S → 2 Na
2S + Na
2S
2Ö
3 + 3 Saat
2Ö
Temel reaksiyonlar
300 °C'ye ısıtıldığında, sodyum sülfat ve sodyum polisülfide ayrışır :
- 4 Na
2S
2Ö
3 → 3 Na
2BU YÜZDEN
4 + Hayır
2S
5
Tiyosülfat tuzları, asitlerle muamele üzerine karakteristik olarak ayrışır. İlk protonasyon sülfürde meydana gelir. Protonasyon -78 °C'de dietil eter içinde gerçekleştirildiğinde , H 2 S 2 O 3 ( tiyosülfürik asit ) elde edilebilir. Bu pKa ile biraz güçlü bir asittir bir sırasıyla 0.6 ve birinci ve ikinci dissosiyasyon için 1.7, ve s.
Normal koşullar altında, bu tuzun fazlalık çözeltilerinin seyreltik asitlerle bile asitleştirilmesi, tamamen kükürt , kükürt dioksit ve suya ayrışma ile sonuçlanır :
- Na
2S
2Ö
3 + 2 HCl → 2 NaCl + "S" + SO
2 + H
2Ö
Bu reaksiyon " saat reaksiyonu " olarak bilinir , çünkü kükürt belirli bir konsantrasyona ulaştığında çözelti renksizden soluk sarıya döner. Bu reaksiyon, kolloidal kükürt üretmek için kullanılmıştır. Bu işlem, kimya derslerinde reaksiyon hızı kavramını göstermek için kullanılır .
koordinasyon kimyası
Tiyosülfat, yumuşak metal iyonları için güçlü bir liganddır . Tipik bir kompleksi [Pd (S 2 O 3 ) 2 ( etilendiamin )] 2- , bir çift bulunmaktadır, tiyosülfat ligandları S-birleşimiyle birleştirilmiştir. Sodyum tiyosülfat ve amonyum tiyosülfat , altının ekstraksiyonu için siyanüre alternatif liksivanlar olarak önerilmiştir . Bu yaklaşımın avantajı, (i) tiyosülfat çok daha az toksik siyanür ve (ii) olan türleri cevher daha are refrakter için altın siyanür (örneğin , karbonlu ya da Carlin tipi maden ) tiyosülfat ile filtre edilebilir. Bu alternatif işlemle ilgili bazı problemler, yüksek tiyosülfat tüketimini ve [Au(S)'den beri uygun bir geri kazanım tekniğinin eksikliğini içerir.
2Ö
3)
2] 3- değildir adsorbe için aktive edilmiş karbon cevheri çamurundan karmaşık altın ayrı altın siyanür kullanılan standart yöntemdir.
iyodometri
Analitik kimyada, en önemli kullanım için gelir tiyosülfat anyon reaksiyona girdiği stoikiometrik ile iyodin indirgeyerek, sulu çözelti içinde iyodür olarak tiyosülfat oksidize edilir tetratiyonat :
- 2 saat
2Ö2−
3 + ben
2 → S
4Ö2−
6 + 2 ben-
Bu reaksiyonun nicel doğası nedeniyle ve Na nedeniyle
2S
2Ö
3· 5H 2 O mükemmel bir raf ömrüne sahiptir, bu şekilde kullanılan bir titrant olarak iyodometri . Na
2S
2Ö
3·5H 2 O da iyot saati deneylerinin bir bileşenidir .
Bu özel kullanım, Winkler'in çözünmüş oksijen testindeki uzun bir dizi reaksiyon yoluyla suyun oksijen içeriğini ölçmek için ayarlanabilir . Ayrıca çözeltideki ( örneğin hidrojen peroksit ) belirli bileşiklerin konsantrasyonlarının hacimsel olarak tahmininde ve ticari ağartma tozu ve sudaki klor içeriğinin tahmininde de kullanılır.
Alüminyum katyon reaksiyonu
Sodyum tiyosülfat analitik kimyada kullanılır . Alüminyum katyonları içeren bir numune ile ısıtıldığında beyaz bir çökelti üretebilir:
- 2 Al 3+ + 3 S
2Ö2−
3 + 3 Saat
2O → 3 SO
2 + 3S + 2 Al(OH)
3
Organik Kimya
Sodyum tiyosülfatın alkilasyonu, Bunte tuzları olarak adlandırılan S -alkiltiyosülfatları verir . Alkiltiyosülfatlar hidrolize duyarlıdır ve tiyol verir. Bu reaksiyon, tiyoglikolik asidin bir sentezi ile gösterilmiştir :
- CLCH
2CO
2H + Na
2S
2Ö
3 → Na[O
3S
2CH
2CO
2H] + NaCl - Na[O
3S
2CH
2CO
2H] + H
2O → HSCH
2CO
2H + NaHSO
4

