Elektrokimyasal gradyan - Electrochemical gradient
Bir elektrokimyasal gradyan a, gradyan arasında elektrokimyasal potansiyel genellikle için, iyon bir boyunca hareket edebilir membran . Gradyan, kimyasal gradyan veya bir zar boyunca çözünen konsantrasyonundaki farklılık ve bir zar boyunca elektrik gradyan veya yük farkı olmak üzere iki kısımdan oluşur . Geçirgen bir zar boyunca eşit olmayan konsantrasyonlarda bir iyon olduğunda, iyon basit difüzyon yoluyla zar boyunca daha yüksek konsantrasyon alanından daha düşük konsantrasyon alanına doğru hareket edecektir . İyonlar ayrıca bir zar boyunca bir elektrik potansiyeli oluşturan bir elektrik yükü de taşırlar . Zar boyunca eşit olmayan bir yük dağılımı varsa, o zaman elektrik potansiyelindeki fark, yükler zarın her iki tarafında dengelenene kadar iyon difüzyonunu tahrik eden bir kuvvet üretir.
Tanım
Elektrokimyasal gradyan, elektrokimyasal potansiyelin gradyanıdır:
- , ile birlikte
- iyon türlerinin kimyasal potansiyeli
- iyon türlerinin değerliliği
- F, Faraday sabiti
- yerel elektrik potansiyeli
genel bakış
Elektrokimyasal potansiyel, elektroanalitik kimyada ve piller ve yakıt hücreleri gibi endüstriyel uygulamalarda önemlidir . Enerjinin korunabileceği birçok değiştirilebilir potansiyel enerji formundan birini temsil eder .
Biyolojik süreçlerde, bir iyonun difüzyon veya bir zar boyunca aktif taşıma yoluyla hareket ettiği yön , elektrokimyasal gradyan tarafından belirlenir. Olarak mitokondri ve kloroplast proton gradyanlar üretmek için kullanılan kemiosmotik potansiyel olarak da bilinen bir proton itici gücü . Bu potansiyel enerji , sırasıyla oksidatif fosforilasyon veya fotofosforilasyon ile ATP sentezi için kullanılır .
Bir elektrokimyasal gradyan iki bileşene sahiptir. İlk olarak, elektrik bileşeni, lipid zarı boyunca bir yük farkından kaynaklanır. İkincisi, bir kimyasal bileşen, zar boyunca farklı bir iyon konsantrasyonundan kaynaklanır . Bu iki faktörün kombinasyonu, bir iyonun bir zar boyunca hareketi için termodinamik olarak uygun yönü belirler.
Bir elektrokimyasal gradyan, bir hidroelektrik barajdaki su basıncına benzer . Membran içindeki sodyum-potasyum pompası gibi zar taşıma proteinleri , suyun potansiyel enerjisini diğer fiziksel veya kimyasal enerji biçimlerine dönüştüren türbinlere eşdeğerdir ve zardan geçen iyonlar, suyun dibinde sona eren suya eşdeğerdir. barajın. Ayrıca, barajın üstündeki göle su pompalamak için enerji kullanılabilir. Benzer şekilde, hücrelerdeki kimyasal enerji, elektrokimyasal gradyanlar oluşturmak için kullanılabilir.
Kimya
Terim tipik olarak, bir pil elektrotunda bir elektron transferini içeren bir kimyasal reaksiyonun yer alacağı bağlamlarda uygulanır . Bir pilde, iyonların hareketinden kaynaklanan bir elektrokimyasal potansiyel, elektrotların reaksiyon enerjisini dengeler. Bir pil reaksiyonunun üretebileceği maksimum voltaj bazen o reaksiyonun standart elektrokimyasal potansiyeli olarak adlandırılır (ayrıca bkz. Elektrot potansiyeli ve Standart elektrot potansiyelleri tablosu ). Spesifik olarak elektrik yüklü çözünen maddelerin hareketiyle ilgili durumlarda, potansiyel genellikle volt birimlerinde ifade edilir . Bakınız: Konsantrasyon hücresi .
biyolojik bağlam
Bir hücre zarı boyunca iyon hareketi yoluyla bir transmembran elektrik potansiyelinin üretilmesi, sinir iletimi, kas kasılması , hormon salgılanması ve duyusal süreçler gibi biyolojik süreçleri yönlendirir . Geleneksel olarak, tipik bir hayvan hücresi, hücrenin içinde dışarıya göre -50 mV ila -70 mV arasında bir transmembran elektrik potansiyeline sahiptir.
Elektrokimyasal gradyanlar, mitokondride oksidatif fosforilasyonda proton gradyanlarının oluşturulmasında da rol oynar. Son adımı hücresel solunum olan elektron taşıma zinciri . Mitokondrinin iç zarına gömülü dört kompleks elektron taşıma zincirini oluşturur. Bununla birlikte, sadece, III I kompleksleri ve bunlardan IV pompa protonları matris için arası boşlukta (IMS). Toplamda, matristen IMS'ye yer değiştiren ve 200mV'den fazla bir elektrokimyasal potansiyel üreten on proton vardır. Bu , ADP'ye inorganik bir fosfat ekleyerek ATP üreten ATP sentaz yoluyla proton akışını matrise geri döndürür . Bu nedenle, mitokondride enerji üretimi için bir proton elektrokimyasal gradyanının oluşturulması çok önemlidir. Elektron taşıma zinciri için toplam denklem:
NADH + 11 H + (matris) + 1/2 O 2 → NAD + + 10 H + (IMS) + H 2 O.
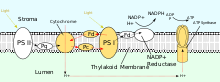
Elektron taşıma zincirine benzer şekilde, fotosentez pompa protonlarının ışığa bağlı reaksiyonları , ATP sentaz tarafından ATP sentezini yürütmek için kloroplastların tilakoid lümenine pompalanır . Proton gradyanı, siklik olmayan veya siklik fotofosforilasyon yoluyla üretilebilir. Siklik olmayan fotofosforilasyonun katılan proteinler, fotosistem II (PSII), plastiquinone ve b sitokrom 6 kompleks f direkt olarak bir proton derecesi üreten katkıda bulunur. PSII tarafından emilen her dört foton için, lümene sekiz proton pompalanır. Fotofosforilasyon için toplam denklem:
2 NADP + + 6 H + (stroma) + 2 H 2 O → 2 NADPH + 8 H + (lümen) + O 2 .
Diğer birkaç taşıyıcı ve iyon kanalı, bir proton elektrokimyasal gradyanının oluşturulmasında rol oynar. Bir TPK olan 3 , bir potasyum kanalı Ca aktive edilir 2+ ve K yürüten + için tilakoid lümenden stroma sağlanmasına yardımcı olur , pH gradyanı. Öte yandan, elektro-nötr K + akış önleyici (KEA 3 ), K +' yı thylakoid lümenine ve H +' yı stromaya aktararak elektrik alanı oluşturmaya yardımcı olur .
iyon gradyanları
İyonlar yüklü olduğundan basit difüzyonla zardan geçemezler. İyonları zar boyunca iki farklı mekanizma ile taşıyabilir: aktif veya pasif taşıma. İyonların aktif taşınmasına bir örnek Na + -K + -ATPase'dir (NKA). NKA , ATP'nin ADP ve bir inorganik fosfata hidrolizini katalize eder ve hidrolize edilen her ATP molekülü için hücre dışına üç Na + , hücre içinde iki K + taşınır. Bu, hücrenin içini dışarıdan daha negatif hale getirir ve daha spesifik olarak , yaklaşık -60mV'lik bir zar potansiyeli V zarı oluşturur. Pasif taşımanın bir örneği, Na + , K + , Ca 2+ ve Cl − kanallarından geçen iyon akışlarıdır . Bu iyonlar, konsantrasyon gradyanlarını aşağı doğru hareket etme eğilimindedir. Örneğin, Na, çok miktarda olduğundan + hücre dışında, Na + , Na akacaktır + hücresine kanalı. Hücre içindeki elektrik potansiyeli negatif olduğundan, pozitif iyon akışı zarı depolarize eder ve bu da transmembran elektrik potansiyelini sıfıra yaklaştırır. Bununla birlikte, kimyasal gradyanın etkisi elektrik gradyanının etkisinden daha büyük olduğu sürece , Na + konsantrasyon gradyanında aşağı doğru hareket etmeye devam edecektir. Her iki gradyanın etkisi eşit olduğunda ( bu yaklaşık +70mV'lik bir zar potansiyelinde Na + için ), Na + akışı durur çünkü itici kuvvet (ΔG) sıfırdır. İtici gücün denklemi:
Bu denklemde, R, temsil ettiği gaz sabiti , T temsil mutlak sıcaklık , z iyonik yük ve F temsil Faraday sabit .
Hücresel iyon konsantrasyonları aşağıdaki tabloda verilmiştir. X- net negatif yüklü proteinleri temsil eder.
| İyon | Memeli | kalamar akson | S. cerevisiae | E. koli | Deniz suyu | ||
|---|---|---|---|---|---|---|---|
| Hücre | Kan | Hücre | Kan | ||||
| K + | 100 - 140 | 4-5 | 400 | 10 - 20 | 300 | 30 - 300 | 10 |
| Hayır + | 5-15 | 145 | 50 | 440 | 30 | 10 | 500 |
| mg 2+ | 10 0,5 - 0,8 |
1 - 1.5 | 50 | 30 - 100 0.01 - 1 |
50 | ||
| Ca 2+ | 10 -4 | 2,2 - 2,6 1,3 - 1,5 |
10 −4 - 3×10 −4 | 10 | 2 | 3 10 -4 |
10 |
| Cl - | 4 | 110 | 40 - 150 | 560 | 10 - 200 | 500 | |
| X - | 138 | 9 | 300 - 400 | 5-10 | |||
| HCO 3 - | 12 | 29 | |||||
| pH | 7.1 - 7.3 | 7,35 ila 7,45 (normal arteriyel kan pH'ı)
6,9 - 7,8 (genel aralık) |
7,2 - 7,8 | 8.1 - 8.2 | |||
Proton gradyanları
Özellikle proton gradyanları, birçok hücre tipinde bir enerji depolama biçimi olarak önemlidir. Gradyan genellikle ATP sentazını, flagellar rotasyonu veya metabolitlerin taşınmasını sağlamak için kullanılır . Bu bölüm, ilgili hücrelerinde proton gradyanlarını oluşturmaya yardımcı olan üç sürece odaklanacaktır: bakteriorhodopsin ve döngüsel olmayan fotofosforilasyon ve oksidatif fosforilasyon.
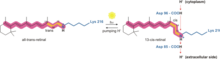
Bakteriyelhodopsin
Bakteriorhodopsinin Archaea'da bir proton gradyanı oluşturma yolu bir proton pompasından geçer . Proton pompası, membranın düşük H + konsantrasyonuna sahip tarafından yüksek H + konsantrasyonuna sahip tarafına protonları sürmek için proton taşıyıcılarına dayanır . Bakteriorhodopsin'de, proton pompası, 568 nm dalga boyundaki fotonların absorpsiyonu ile aktive edilir ve bu , K durumunu oluşturan retinadaki Schiff bazının (SB) izomerizasyonuna yol açar . Bu, SB'yi Asp85 ve Asp212'den uzaklaştırarak SB'den Asp85'e H + transferinin M1 durumunu oluşturmasına neden olur . Protein daha sonra Glu204'ü Glu204'ten dış ortama bir proton salan Glu194'ten ayırarak M2 durumuna geçer. SB, N durumunu oluşturan Asp96 tarafından yeniden protonlanır. Onun beri ikinci proton Asp96 geldiği önemlidir protonu giderilmiş devlet dengesiz olup, hızla gelen bir proton ile reprotonated sitozolün . Asp85 ve Asp96'nın protonasyonu, O durumunu oluşturan SB'nin yeniden izomerizasyonuna neden olur. Son olarak, Asp85 protonunu Glu204'e bıraktığında bakteriorhodopsin dinlenme durumuna geri döner.
fotofosforilasyon
PSII ayrıca kloroplastlarda proton gradyanlarının oluşumunu yönlendirmek için ışığa güvenir , ancak PSII bu amaca ulaşmak için vektörel redoks kimyasını kullanır. Protonların protein içinde fiziksel olarak taşınması yerine, hücre dışı tarafta protonların bağlanmasını gerektiren reaksiyonlar meydana gelirken, hücre içi tarafta protonların salınmasını gerektiren reaksiyonlar meydana gelecektir. 680 nm dalga boylu foton emilimine iki elektron uyarmak için kullanılan P 680 , bir daha yüksek enerji seviyesine . Bu daha yüksek enerjili elektronlar, proteine bağlı plastokinona (PQ A ) ve daha sonra bağlanmamış plastokinona (PQ B ) aktarılır . Bu, plastokinonu (PQ) , stromadan iki proton kazandıktan sonra PSII'den salınan plastokinole (PQH 2 ) indirger . P 680'deki elektronlar , oksijen gelişen kompleks (OEC) yoluyla suyun oksitlenmesiyle yenilenir . O salınmasında Bu sonuçlar 2 ve H + lümenine. Toplam reaksiyon gösterilir:
PSII serbest bırakıldıktan sonra, PQH 2 b sitokrom doğru hareket 6 daha sonra PQH iki elektron transfer kompleksi f 2 için plastosiyanin iki ayrı reaksiyonlarda. Meydana gelen süreç, elektron taşıma zincirinin Kompleks III'teki Q döngüsüne benzer. Birinci reaksiyonda, PQH 2 lümen tarafında kompleksine bağlanan ve bir elektron transfer edilir demir-sülfür merkezi sonra aktarır sitokrom f sonra plastosiyanindeki aktarır. İkinci elektron heme b L'ye aktarılır, bu daha sonra onu heme b H'ye aktarır ve daha sonra onu PQ'ya aktarır. İkinci reaksiyonda, ikinci PQH 2 başka plastosiyanindeki ve PQ için bir elektron eklenmesi, okside olur. Her iki reaksiyon birlikte dört protonu lümene aktarır.
Oksidatif fosforilasyon
Elektron taşıma zinciri, içinde kompleks I (CI) katalize azalma ve ubikinon ile (UQ) üzerinden ubikuinolden (UQH 2 iki transferi ile) elektron düşük gelen nikotinamid adenin dinükleotid IMS mitokondrial matris dört proton yer değiştirir (NADH) :
Kompleks III (CIII), Q döngüsünü katalize eder . UQH iki elektronun transferini içeren birinci aşama 2 oksitlenmiş iki molekülü ile CI ile indirgenmiş sitokrom c Q o sitesi. İkinci aşamada, iki veya daha fazla elektron UQH için UQ azaltmak 2 Q ise, en i sitesi. Toplam reaksiyon gösterilir:
Kompleks IV (CIV), CIII tarafından indirgenmiş sitokrom c'den tam oksijenin yarısına iki elektron transferini katalize eder. Oksidatif fosforilasyonda bir tam oksijenin kullanılması, dört elektronun transferini gerektirir. Oksijen daha sonra su oluşturmak için matristen dört proton tüketirken, diğer dört proton IMS'ye pompalanır. Toplam reaksiyon gösterilir:
Ayrıca bakınız
Referanslar
- Campbell ve Reece (2005). Biyoloji . Pearson Benjamin Cummings. ISBN'si 978-0-8053-7146-8.
- Stephen T. Abedon, Ohio Eyalet Üniversitesi'nde Biyoloji 113 için "Bölüm 8'den önemli kelimeler ve kavramlar, Campbell & Reece, 2002 (1/14/2005)"