oksaziridin - Oxaziridine

|
|

|
|

|
|
| İsimler | |
|---|---|
|
Tercih edilen IUPAC adı
oksaziridin |
|
|
Sistematik IUPAC adı
1-Oksa-2-azasiklopropan |
|
| Diğer isimler
Oksaaziridin
Oksazasiklopropan |
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| Kimyasal Örümcek | |
|
PubChem Müşteri Kimliği
|
|
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikleri | |
| Cı , H 3 K O | |
| Molar kütle | 45.041 g·mol -1 |
|
Aksi belirtilmediği sürece, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
| Bilgi kutusu referansları | |
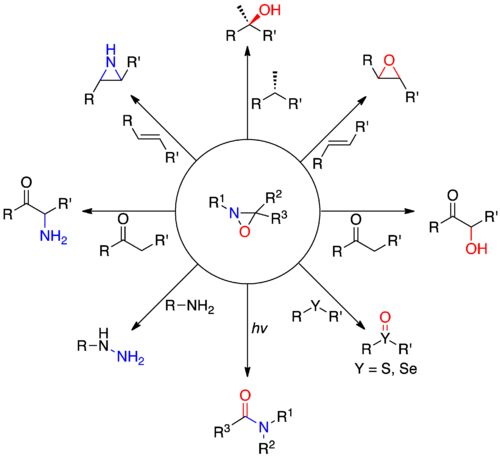
Bir oksaziridin , oksijen, nitrojen ve karbon içeren üç üyeli bir heterosikl içeren organik bir moleküldür . En büyük uygulamalarında oksaziridinler, hidrazinin endüstriyel üretiminde ara maddelerdir . Oksaziridin türevleri ayrıca organik kimyada enolatların alfa hidroksilasyonu, olefinlerin epoksidasyonu ve aziridinasyonu ve diğer heteroatom transfer reaksiyonları dahil olmak üzere çeşitli oksidasyonlar için özel reaktifler olarak kullanılır. Oksaziridinler ayrıca amidlere öncü olarak hizmet eder ve ikame edilmiş beş üyeli heterosikller oluşturmak için çeşitli heterokümülenlerle [3+2] siklo ilavelerine katılır. Kiral oksaziridin türevleri, diğer substratların yanı sıra prokiral enolatlara asimetrik oksijen transferini etkiler. Bazı oksaziridinler ayrıca nitrojenin tersine çevrilmesine karşı yüksek bir bariyer özelliğine sahiptir ve nitrojen merkezinde kiralite olasılığına izin verir.
Tarih
Oksaziridin türevleri ilk olarak 1950'lerin ortalarında Emmons ve ardından Krimm ve Horner ve Jürgens tarafından rapor edildi. Oksijen ve nitrojen , yüksek elektronegatiflikleri nedeniyle tipik olarak nükleofiller gibi davranırken , oksaziridinler her iki heteroatomun elektrofilik transferine izin verir . Bu olağandışı reaktivite, oldukça gergin üç üyeli halkanın ve nispeten zayıf NO bağının varlığından kaynaklanmaktadır. Azot ikame küçük olduğunda nükleofiller aziridin nitrojende saldırı (R eğilimi 1 = H) ve oksijen atomu, nitrojen ikame büyük olduğunda sterik kütleye . Oksaziridin sisteminin dışı elektronik de dahil olmak üzere, oksijen ve azot transfer reaksiyonlarının bir dizi yapmak için kullanılabilir, ancak bunlarla sınırlı değildir: bir α-hidroksilasyon enolatlar , epoksidasyonu alkenlerin, seçici oksidasyonu sülfitlerin ve selenürler , aminasyon ve N -nucleophiles ve N- asilamidasyon.
Peroksit işlemi endüstriyel üretimi için hidrazin oksidasyonu yoluyla amonyak ile hidrojen peroksit ketonların mevcudiyetinde 1970'lerin başında geliştirilmiştir.
Kiral kamforsülfoniloksaziridinlerin, kemoterapi ajanı olarak pazarlanan taksol gibi kompleks ürünlerin sentezinde faydalı olduğu kanıtlanmıştır. Hem Holton Taxol toplam sentezi hem de Wender Taxol toplam sentezi , kamforsülfoniloksaziridin ile asimetrik a-hidroksilasyon özelliğine sahiptir.
sentez
NH, N-alkil, N-ariloksaziridinler
NH, N-alkil ve N-aryloxaziridines sentezi için iki temel yaklaşım, oksitlenmesi iminler ile perasitler (A) ve aminasyon karboniller (B).
Ek olarak, kiral iminlerin oksidasyonu ve iminlerin kiral perasitlerle oksidasyonu, enantiopür oksaziridinler verebilir. Bazı oksaziridinler, 100 ila 130 kJ/mol'lük bir inversiyon bariyeri nedeniyle oda sıcaklığında konfigürasyon olarak kararlı nitrojen atomlarının benzersiz özelliğine sahiptir. Stereokimyanın tamamen konfigürasyonsal olarak kararlı nitrojene bağlı olduğu enantiopür oksaziridinler rapor edilmektedir.
N- sülfoniloksaziridinler
1970'lerin sonlarında ve 1980'lerin başında Franklin A. Davis , yalnızca oksijen transfer reaktifleri olarak hareket eden ve bugün en baskın olarak kullanılan oksaziridin sınıfı olan ilk N- sülfoniloksaziridinleri sentezledi . Orijinal olarak mCPBA ve faz transfer katalizörü benziltrimetilamonyum klorür ile sentezlenmiş olsa da, oksidan olarak okson kullanılarak geliştirilmiş bir sentez artık en yaygın olanıdır.
Günümüzde her biri biraz farklı özelliklere ve reaktiviteye sahip birçok N-sülfoniloksaziridin kullanılmaktadır. Bu reaktifler aşağıdaki tabloda özetlenmiştir.
perflorlu oksaziridinler
Yüksek elektron çeken perfloroalkil sübstitüentleri ile oksaziridinler, dioksiranlarınkine tipik oksaziridinlere göre daha benzer reaktivite sergiler . Özellikle, perfloroalkiloksaziridinler, yüksek seçicilikle belirli CH bağlarını hidroksiller. Perflorlu oksaziridinler, bir perflorlu iminin perflorometil florokarbonil perokside ve bir metal floride bir HF süpürücü olarak işlev görmesine tabi tutulmasıyla sentezlenebilir.
Reaksiyonlar
Hidrazin üretimi
Oksaziridinler, hidrazin üretimi için peroksit işleminde ara maddelerdir . Amonyağın oksaziridini vermek üzere metil etil keton varlığında oksitlendiği bir adımı içeren bu yöntemle yılda milyonlarca kilogram hidrazin üretilir :
- Me (Et), C = O + NH 3 + H 2 O 2 → Me (Et), CONH + H 2 O
Sonraki adımlarda, oksaziridin, hidrazin yolunda hemen olan hidrazon'a dönüştürülür:
- Me (Et), CONH + NH 3 → Me (Et), C = NNH 2 + H 2 O
oksijen transferi
Enolatların α-Hidroksilasyonu
α-Hidroksiketonlar veya asilolinler , birçok doğal üründe bulunan önemli bir sentetik motiftir . α-Hidroksiketonlar, α-diketonların indirgenmesi, ayrılan grup için bir hidroksil ikamesi ve bir enolatın doğrudan oksidasyonu dahil olmak üzere birçok yolla sentezlenmiştir. Oksodiperoksimolibdenum(piridin)-(heksametilfosforik triamid) (MoOPH) ve N- sülfoniloksaziridinler, bu işlemde uygulanan en yaygın elektrofilik oksijen kaynaklarıdır. N- sülfoniloksaziridinleri kullanmanın bir avantajı, MoOPH ve diğer oksidanlara göre neredeyse her zaman daha yüksek kiral indüksiyonun gözlenmesidir. Elektrofil olarak N- sülfoniloksaziridin ile Evans'ın kiral yardımcısı ile a-hidroksilasyon için yüksek verim (%77-91) ve dr (95:5 – 99:1) rapor edilmiştir. Kiral indüksiyon, SAMP ve RAMP dahil olmak üzere şiral yardımcı maddelere sahip diğer birçok kiral keton ve keton ile gösterilmiştir .
Prokiral enolatların kamforsülfoniloksaziridin türevleri ile asimetrik hidroksilasyonu üzerine, orta ila yüksek enantiyomerik fazlalık elde eden kapsamlı çalışmalar rapor edilmiştir . Bu stereokimyasal ürünü, R sterik kütle açık geçiş durumunu içerir haklı genel olarak kabul edilen, önerilen geçiş durum 1 yaklaşımın yüzünü belirler.
Bazı hidroksilasyonların seçiciliği, yukarıdaki tabloda oksaziridinler 3b ve 3c olarak oksaziridin halkasına alfa koordinasyon gruplarının eklenmesiyle bazı durumlarda büyük ölçüde iyileştirilebilir . Bu gibi durumlarda reaksiyon, metal oksianyon stabilize kapalı bir geçiş durumunun ilerler önerilmektedir şelasyon kafur iskelet üzerinde sülfat ve koordinasyon grubunu ihtiva etmektedir.
Oksaziridinlerle a-hidroksilasyon, toplam sentezde yaygın olarak uygulanmıştır. Hem Holton Taxol toplam sentezinde hem de Wender Taxol toplam sentezinde önemli bir adımdır . Ek olarak, Forsyth, C3-C14 (sübstitüe edilmiş 1,7-Dioxaspiro[5.5]undec-3-ene) Okadaik asit Sisteminin sentezindeki dönüşümü uyguladı .
alkenlerin epoksidasyonu
Alkenlerin epoksidasyonu yaygın bir reaksiyondur çünkü epoksitler bir dizi faydalı yolla türevlendirilebilir. Klasik olarak, laboratuvar epoksidasyonu mCPBA veya diğer perasitler ile gerçekleştirilir. Oksaziridinlerin, aside son derece duyarlı epoksitlerin oluşumu için faydalı olduğu bulunmuştur. (-)-Chaetominin, aşağıda görüldüğü gibi geç aşama transformasyonu olarak oksaziridin epoksidasyonu yoluyla sentezlendi.
Yüksek sentetik faydanın bir başka dönüşümü asimetrik epoksidasyondur . Bir dizi asimetrik epoksidasyon mevcuttur: Sharpless epoksidasyonu , Jacobsen-Katsuki epoksidasyonu ve Juliá-Colonna epoksidasyonu . Bu yöntemler, seçiciliği sağlamak için belirli işlevsellik gerektirir. Sharpless epoksidasyonu alilik alkollere özgüdür, Jacobsen epoksidasyonu cis- disübstitüe aril alkenleri gerektirir ve Juliá epoksidasyonu α-β doymamış ketonları gerektirir . Kiral oksaziridinler , birçok işlevsiz alken üzerinde stereospesifik olarak etki eder . Hatta oksaziridin kiral biriminde stereospesifik epoksidasyonu katalitik olarak etkilemek mümkündür. Enantiometik fazlalık seviyeleri büyük ölçekli sentez için pratik hale gelmeden önce bu reaksiyonlarla ilgili daha fazla araştırma yapılması gerekebilir. Lusinichi et al. aşağıda görülen stokiyometrik oksidan olarak okson kullanan bir kiral oksaziridinyum tuzu ile asimetrik epoksidasyonu araştırmışlardır.
Aktifleştirilmemiş hidrokarbonların hidroksilasyonu
Perflorlu oksaziridinlerin, kayda değer bir bölgesel ve diastereospesifiklikle aktifleştirilmemiş hidrokarbonları hidroksillediği bilinmektedir. Bu çok arzu edilen bir dönüşümdür ve benzer tepkisellik ve özgüllük, özellikle oksidanın metalik olmayan doğası göz önüne alındığında, nadiren rekabet eder. Perflorlu oksaziridinler, üçüncül hidrojenlere karşı yüksek seçicilik gösterir . Birincil karbonların hidroksilasyonu ve iki oksitlenebilir bölgeye sahip bir bileşiğin dihidroksilasyonu hiç gözlenmedi. Stereokimyanın tutulması çok yüksektir, genellikle %95 ila 98'dir. (Stereokimyanın tutulması, bir florür tuzunun eklenmesiyle daha da arttırılabilir).
azot transferi
Sübstitüe edilmemiş veya asillenmiş nitrojenlere sahip oksaziridinler, bu reaktivite önemli ölçüde daha az dikkat çekmiş olsa da, nitrojen atomu transfer edebilir.
Aminasyonu N -nucleophiles
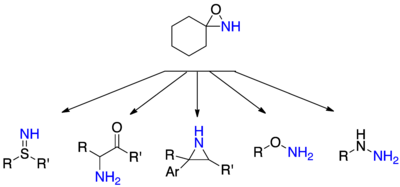
N- sübstitüe edilmemiş oksaziridinler ile nükleofillerin aminasyonu, olası nükleofiller ve karşılık gelen ürünler açısından oldukça çok yönlüdür. Hidrazinler , ikincil veya üçüncül aminlerin aminasyonundan türetilebilir, hidroksilamin ve tiyohidroksaminler, karşılık gelen alkollerinden ve tiyollerinden oluşturulabilir, sülfimitler tiyoeterlerden oluşturulabilir ve a-aminoketonlar, karşılık gelen enolatların saldırısı ile oluşturulabilir.
N- asilamidasyon
Asillenmiş aminlerin transferi, ikame edilmemiş aminlerinkinden daha zordur, ancak oksaziridinler tarafından amin transferinden farklı olarak, açillenmiş aminleri doğrudan transfer eden alternatif yöntemler yoktur. Asilamin transferi öncelikle nükleofiller olarak aminler ve hidrazinler kullanılarak gerçekleştirilmiştir. Literatürde bazıları olmasına rağmen, karbon nükleofillere çok az sayıda asillenmiş nitrojen transferi başarıyla gerçekleştirilmiştir.
yeniden düzenlemeler
Oksaziridinlerin, UV ışığı ile ışınlandığında veya Cu I gibi tek bir elektron transfer reaktifi varlığında radikal bir mekanizma yoluyla yeniden düzenleme reaksiyonlarına girdiği bulunmuştur . spirosiklik oksaziridinler karşılık gelen laktama halka açılımlarına uğrarlar . Göç eden ikame edici, nitrojen üzerindeki yalnız çifte trans grubunun her zaman baskın göç ürünü olacağı bir stereoelektronik etki ile belirlenir . Bu etkinin ışığında, yeniden düzenlemeyi yönlendirmek için yüksek inversiyon bariyeri nedeniyle kiral nitrojenden yararlanmak mümkündür. Bu fenomen, aşağıdaki yeniden düzenlemelerde gözlemlenen seçiciliklerle gösterilmektedir. Soldaki yeniden düzenlemede sadece termodinamik açıdan elverişsiz ürün gözlenirken, sağdaki reaksiyonda daha az kararlı radikal ara üründen türetilen ürün tercih edilir.
Aubé , NIH tarafından erektil disfonksiyon ve seçici serotonin geri alım inhibitörlerinin neden olduğu cinsel sorunların tedavisinde muhtemelen etkili olarak sınıflandırılan doğal bir ilaç olan (+)- yohimbin sentezinde anahtar adım olarak bu yeniden düzenlemeden yararlanıyor .
Ayrıca, oksaziridinlerin termal olarak nitronlara yeniden düzenleneceği de dikkate değerdir . Elde edilen nitronun Cis-trans seçiciliği zayıftır, ancak verimler iyi ila mükemmel arasındadır. Bazı oksaziridinlerin bir nitron ara ürünü yoluyla zamanla rasemize olduğu düşünülmektedir.
Heterokümülenlerle siklus yüklemeleri
Oksaziridinler , aşağıdaki şekilde gösterildiği gibi, bir dizi benzersiz beş üyeli heterosikl elde etmek için hetero kümülenlerle siklo ekleme reaksiyonlarına girer . Bu reaktivite, gergin üç üyeli halka ve zayıf NO bağından kaynaklanmaktadır.