Lityum kobalt oksit - Lithium cobalt oxide
 |
|
|
|
| İsimler | |
|---|---|
|
IUPAC adı
lityum kobalt(III) oksit
|
|
| Diğer isimler
lityum kobaltit
|
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| Kimyasal Örümcek | |
| ECHA Bilgi Kartı |
100.032.135 |
| AT Numarası | |
|
PubChem Müşteri Kimliği
|
|
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikleri | |
|
LiCoO 2 |
|
| Molar kütle | 97.87 g mol -1 |
| Görünüm | koyu mavi veya mavimsi gri kristal katı |
| Tehlikeler | |
| Ana tehlikeler | zararlı |
| GHS piktogramları |
 
|
| GHS Sinyal kelimesi | Tehlike |
| H317 , H350 , H360 | |
| P201 , P202 , P261 , P272 , P280 , P281 , + 352 P302 , P308 + 313 , P321 , P333 + 313 , başvurunuz P363 , P405 , P501 | |
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
|
|
|
| Bilgi kutusu referansları | |
Lityum kobalt oksit , de denir lityum cobaltate veya lityum kobaltit , a, kimyasal bileşik , formül ile LiCoO
2. Kobalt atomu, +3 oksidasyon durumunda resmi nedenle olan IUPAC adı lityum kobalt (III) oksit .
Lityum kobalt oksit koyu mavi ya da gri-mavi kristalli bir katıdır, ve yaygın olarak pozitif kullanılan elektrotlar arasında lityum iyon pil .
yapı
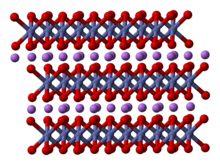
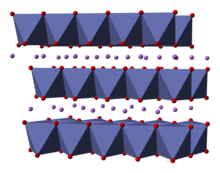
LiCoO'nun yapısı
2x-ışını kırınımı , elektron mikroskobu , nötron tozu kırınımı ve EXAFS dahil olmak üzere çok sayıda teknikle çalışılmıştır .
Katı, monovalent lityum katyonlarının katmanlarından oluşur ( Li+
) iki yüzü levha düzlemine paralel olan, kenar paylaşan oktahedra olarak düzenlenmiş, kobalt ve oksijen atomlarının genişletilmiş anyonik tabakaları arasında uzanan . Kobalt atomları resmi olarak üç değerlikli oksidasyon durumundadır ( Co3+
) ve iki oksijen atomu tabakası ( O2–
).
Her katmanda (kobalt, oksijen veya lityum), atomlar düzenli bir üçgen kafes içinde düzenlenir. Kafesler, lityum atomları kobalt atomlarından en uzak olacak şekilde dengelenir ve yapı, her üç kobalt (veya lityum) katmanında düzlemlere dik yönde tekrar eder. Nokta grubu simetri içinde Hermann-Mauguin üç kat bir birim hücre gösteren, gösterim uygun olmayan dönme simetrisi ve bir ayna düzlemine. Üç katlı dönme ekseni (katmanlara normal olan) uygunsuz olarak adlandırılır, çünkü oksijen üçgenleri (her bir oktahedronun zıt taraflarında bulunur) hizasızdır.
Hazırlık
Tamamen indirgenmiş lityum kobalt oksit, lityum karbonat Li'nin stoikiometrik bir karışımını ısıtarak hazırlanabilir.
2CO
3ve kobalt (II, III) oksit Co
3Ö
4veya metalik kobalt 600–800 °C'de, ardından ürünü 900 °C'de saatlerce oksijen atmosferi altında tavlama .
Katot kullanımına daha uygun nanometre boyutundaki partiküller, hidratlı kobalt oksalat β- CoC'nin kalsinasyonu ile de elde edilebilir.
2Ö
4· 2 Saat
2O , 750-900 °C'ye kadar lityum hidroksit LiOH ile yaklaşık 8 um uzunluğunda ve 0,4 um genişliğinde çubuk benzeri kristaller şeklinde .
Üçüncü bir yöntem , su çözeltisi içinde eşit molar miktarlarda lityum asetat , kobalt asetat ve sitrik asit kullanır . 80 °C'de ısıtma, karışımı viskoz şeffaf bir jele dönüştürür. Kurutulmuş jel daha sonra öğütülür ve kademeli olarak 550 °C'ye ısıtılır.
Şarj edilebilir pillerde kullanın
Bir alt katkı elektrot olarak lityum kobalt oksit faydası bir tarafından 1980 yılında keşfedildi Oxford University liderliğindeki araştırma grubu John B. Goodenough ve Tokyo Üniversitesi 'nin Koichi Mizushima .
Bileşik şimdi bazı şarj edilebilir katod olarak kullanılır lityum iyon bataryalar arasında değişen tanecik boyutlarına sahip, nanometre için mikrometre . Şarj sırasında, kobalt kısmen +4 durumuna oksitlenir, bazı lityum iyonları elektrolite hareket eder ve sonuçta bir dizi Li bileşiği oluşur.
xCoO
20 < x < 1 ile
LiCoO ile üretilen piller
2katotlar çok kararlı kapasitelere sahiptir, ancak nikel-kobalt-alüminyum (NCA) oksitlere dayalı katotlara göre daha düşük kapasite ve güce sahiptir. Termal kararlılıkla ilgili sorunlar LiCoO için daha iyidir
2önemli ölçüde olmasa da diğer nikel açısından zengin kimyalardan daha katotlar. Bu, LiCoO'yu
2yüksek sıcaklıkta çalıştırma (>130 °C) veya aşırı şarj gibi kötüye kullanım durumlarında termal kaçaklara duyarlı piller . Yüksek sıcaklıklarda, LiCoO
2 Ayrışma oksijen üretir ve bu oksijen daha sonra hücrenin organik elektroliti ile reaksiyona girer. Bu, bitişik hücrelere yayılabilen veya yakındaki yanıcı malzemeleri ateşleyebilen bu yüksek derecede ekzotermik reaksiyonun büyüklüğünden dolayı bir güvenlik sorunudur. Genel olarak, bu birçok lityum iyon pil katodu için görülür.


