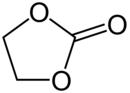
etilen karbonat - Ethylene carbonate
|
|
|||
| İsimler | |||
|---|---|---|---|
|
Tercih edilen IUPAC adı
1,3-Dioksolan-2-bir |
|||
| Diğer isimler
etilen glikol karbonat
|
|||
| tanımlayıcılar | |||
|
3B model ( JSmol )
|
|||
| Kimyasal Örümcek | |||
| ECHA Bilgi Kartı |
100.002.283 |
||
|
PubChem Müşteri Kimliği
|
|||
| ÜNİİ | |||
|
CompTox Panosu ( EPA )
|
|||
|
|||
|
|||
| Özellikler | |||
| Cı- 3 H 4 O 3 | |||
| Molar kütle | 88.062 g·mol -1 | ||
| Dış görünüş | Beyaz ila sarı katı | ||
| Yoğunluk | 1,3210 g / cc 3. | ||
| Erime noktası | 34 - 37 °C (93 - 99 °F; 307 - 310 K) | ||
| Kaynama noktası | 243.0 °C (469.4 °F; 516.1 K) | ||
| Çözünür | |||
| Tehlikeler | |||
| Güvenlik Bilgi Formu | Harici MSDS | ||
|
AB sınıflandırması (DSD) (eski)
|
tahriş edici ( XI ) | ||
| R cümleleri (modası geçmiş) | R41 | ||
| S-ifadeleri (modası geçmiş) | S26 S39 | ||
| Alevlenme noktası | 150 °C (302 °F; 423 K) | ||
| 465 °C (869 °F; 738 K) | |||
|
Aksi belirtilmediği sürece, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|||
|
|
|||
| Bilgi kutusu referansları | |||
Etilen karbonat (bazen kısaltılmış AT ) olan organik bileşiğin formülü ile (CH 2 O) 2 CO. Bu olarak sınıflandırılır siklik karbonat ester ve etilen glikol ve karbonik asit . Oda sıcaklığında (25 °C) etilen karbonat şeffaf kristalli bir katıdır, pratik olarak kokusuz ve renksizdir ve suda biraz çözünür. Sıvı halde (en 34-37 °C) renksiz, kokusuz bir sıvıdır.
Üretim ve reaksiyonlar
Etilen karbonat, etilen oksit ve karbon dioksit arasındaki reaksiyonla üretilir . Reaksiyon, çeşitli katyonlar ve kompleksler tarafından katalize edilir:
- (CH 2 ) 2 O + CO 2 → (CH 2 O) 2 CO
Laboratuarda etilen karbonat, 150 °C sıcaklıkta ve 3 kPa basınçta katalizör olarak çinko oksit kullanılarak üre ve etilen glikolün reaksiyonundan da üretilebilir :
- (NH 2 ) 2 CO + HO−CH 2 CH 2 −OH → (CH 2 O) 2 CO + 2 NH 3
Etilen karbonat (ve propilen karbonat ) dönüştürülebilir dimetil karbonat (faydalı bir solvent ve hafif bir metilleyici madde ile) transesterifikasyon ile metanol :
- Cı- 2 , H 4 CO 3 + 2CH 3 OH → CH 3 OCO 2 CH 3 + HOC 2 H 4 OH
Dimetil karbonat, aynı zamanda, yüksek yüzey alanlı (termal olarak pul pul dökülmüş) grafit karbon nitrür (gC 3 N 4) malzemeleri tarafından katalize edilen etilen karbonat ve metanolün transesterifikasyonu yoluyla da yapılabilir . Bu yöntem metal veya halojenür kontaminasyonu olasılığını azaltır ve 393 K sıcaklıkta %60'a kadar verim sağlayabilir.
Dimetil karbonatın kendisi de benzer şekilde bir fosgen ikamesi olan difenil karbonata transesterifiye edilebilir :
- CH 3 OCO 2 CH 3 + 2 PhOH → PhoCO 2 Ph + 2 MeOH
Uygulamalar
Etilen karbonat olarak kullanılan polar bir çözücü , bir ile moleküler dipol momentinin 4.9 D , sadece 0.1 D göre daha düşük propilen karbonat .
Bu yüksek olarak kullanılabilir geçirgenlik bileşeni elektrolit içinde lityum pilleri ve lityum iyon pil . Viskoziteyi ve erime noktasını düşürmek için bu elektrolitlere dietil karbonat , etil metil karbonat, dimetil karbonat ve metil asetat gibi diğer bileşenler eklenebilir .
Tipik bir sodyum interkalasyon tipi pil, etilen karbonat ve dietil karbonat (EC/DEC) içinde floroetilen karbonat (FEC) (%99), metalik Na (%99.9) ve 1.0 M sodyum perklorat (NaClO4) solüsyonlarından oluşan bir elektrolit kullanır. , 1:1 v/v pil sınıfı, FEC ile karıştırılmış (ağırlıkça %10). Etilen ve dietil karbonatların bir karışımı kullanıldığında, florlu karbonatlar 2 volta kadar daha yüksek potansiyeller sağlar.
Etilen karbonat ayrıca plastikleştirici olarak ve polimerlerde ve organik sentezde kullanılan vinilen karbonatın öncüsü olarak kullanılır .
Oksalil klorür ticari olarak etilen karbonattan üretilir. Fotoklorlama, tetrakloroetilen karbonatı verir:
- C 2 H 4 O 2 CO + 4 Cl 2 → C 2 Cl 4 O 2 CO + 4 HCl
Tetraklorür, amin katalizörleri tarafından oksalil klorüre indirgenir.
- C 2 Cl 4 O 2 CO → C 2 O 2 Cl 2 + COCl 2
Ayrıca bakınız
Dış bağlantılar
Referanslar
- ^ "CID 7303 -- PubChem Bileşik Özeti" . pubchem.ncbi.nlm.nih.gov . 2008-03-15 alındı .
- ^ JEFFSOL ETİLEN KARBONAT www.huntsman.com adresindeki katalog girişi. 2010-02-18 tarihinde erişildi.
- ^ a b Buysch, Hans-Josef (2012). "Karbonik Esterler". Ullmann'ın Endüstriyel Kimya Ansiklopedisi . Weinheim: Wiley-VCH. doi : 10.1002/14356007.a05_197 .
- ^ Comerford, James W.; Ingram, Ian DV; Kuzey, Michael; Wu, Xiao (2015). "Beş üyeli halkalar içeren siklik karbonatların sentezi için sürdürülebilir metal bazlı katalizörler". Yeşil Kimya . 17 (4): 1966–1987. doi : 10.1039/C4GC01719F .
- ^ Bhalchandra M. Bhanage; Shin-ichiro Fujita (2003). "Üre bazlı dimetil karbonat sentezi için önemli bir adım olarak üre ve etilen glikolün etilen karbonata transesterifikasyonu". Yeşil Kimya . 5 (4): 429-432. doi : 10.1039/b304182d .
- ^ Gan, Yu Lin; Hu, Xiao-Qian; Wen, Lin-Zhi; Xu, Jie; Xue, Bing (2020-02-24). "Grafitik karbon nitrür malzemeleri tarafından katalize edilen etilen karbonatın transesterifikasyonu yoluyla dimetil karbonatın metal içermeyen sentezi" . Yeni Kimya Dergisi . 44 (8): 3215–3223. doi : 10.1039/C9NJ04530A . ISSN 1369-9261 . S2CID 213404364 .
- ^ Ralph P. Seward; Ernest C. Vieira (1958). "Etilen Karbonatın Dielektrik Sabitleri ve Etilen Karbonat Çözeltilerinin Su, Metanol, Benzen ve Propilen Karbonattaki Çözeltileri". J. Fizik Chem . 62 (1): 127–128. doi : 10.1021/j150559a041 .
- ^ Richard Payne; Ignatius E. Theodorou (1972). "Etilen karbonat ve propilen karbonatta dielektrik özellikler ve gevşeme". J. Fizik Chem . 76 (20): 2892–2900. doi : 10.1021/j100664a019 .
- ^ ER Logan; JR Dahn (2018). "Ester İçeren Li-İyon Pil Elektrolitlerinin Fiziksel Özelliklerinin İncelenmesi". J. Elektrokimya. Soc . 165 (2): A21–A30. doi : 10.1149/2.0271802jes . OSTI 1469344 .
- ^ Yusuf Sayed, Sayed; Kalisvaart, W. Peter; Olsen, Brian; Luber, Erik; Buriak, Jillian (2020-07-13). "Sodyum İyon Pillerde Kalay Anotların Silikonla Alaşımlanarak Stabilize Edilmesi" . incir . doi : 10.26434/chemrxiv.12642956.v1 . 2021-02-24 alındı .
- ^ Pfoertner, Karl-Heinz (2000). "Fotokimya". Ullmann'ın Endüstriyel Kimya Ansiklopedisi . Weinheim: Wiley-VCH. doi : 10.1002/14356007.a19_573 .