Magnezyum hidroksit - Magnesium hydroxide

|
|
|
|
| İsimler | |
|---|---|
|
IUPAC adı
Magnezyum hidroksit
|
|
| Diğer isimler
Magnezyum dihidroksit Magnezyum
sütü |
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| chebi | |
| CHEMBL | |
| Kimyasal Örümcek | |
| ECHA Bilgi Kartı |
100.013.792 |
| AT Numarası | |
| E numarası | E528 (asitlik düzenleyiciler, ...) |
| 485572 | |
|
PubChem Müşteri Kimliği
|
|
| RTECS numarası | |
| ÜNİİ | |
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikler | |
| Mg(OH) 2 | |
| Molar kütle | 58.3197 g/mol |
| Dış görünüş | Beyaz katı |
| Koku | Kokusuz |
| Yoğunluk | 2,3446 g / cc 3. |
| Erime noktası | 350 °C (662 °F; 623 K) ayrışır |
|
Çözünürlük ürünü ( K sp )
|
5,61×10 −12 |
| -22,1 · 10 -6 cm 3 / mol | |
|
Kırılma indisi ( n D )
|
1.559 |
| Yapı | |
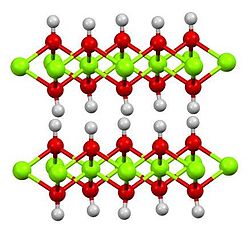
| Altıgen, hP3 | |
| P 3 m1 No. 164 | |
|
a = 0,312 nm, c = 0,473 nm
|
|
| Termokimya | |
|
Isı kapasitesi ( C )
|
77.03 J/mol·K |
|
Std molar
entropi ( S |
64 J·mol -1 ·K -1 |
|
Std
oluşum entalpisi (Δ f H ⦵ 298 ) |
-924.7 kJ·mol -1 |
|
Gibbs serbest enerjisi (Δ f G ˚)
|
-833,7 kJ/mol |
| Farmakoloji | |
| A02AA04 ( WHO ) G04BX01 ( WHO ) | |
| Tehlikeler | |
| Güvenlik Bilgi Formu | Harici MSDS |
| GHS piktogramları |

|
| GHS Sinyal kelimesi | Uyarı |
| H315 , H319 , H335 | |
| P261 , P280 , P305+351+338 , P304+340 , P405 , P501 | |
| NFPA 704 (ateş elması) | |
| Alevlenme noktası | Yanıcı değil |
| Ölümcül doz veya konsantrasyon (LD, LC): | |
|
LD 50 ( ortalama doz )
|
8500 mg/kg (sıçan, ağızdan) |
| Bağıntılı bileşikler | |
|
Diğer anyonlar
|
Magnezyum oksit |
|
Diğer katyonlar
|
|
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
|
|
|
| Bilgi kutusu referansları | |
Magnezyum hidroksit , kimyasal formülü Mg(OH) 2 olan inorganik bileşiktir . Doğada mineral brusit olarak bulunur . Suda çözünürlüğü düşük beyaz bir katıdır ( K sp = 5.61×10 -12 ). Magnezyum hidroksit, magnezyum sütü gibi antasitlerin yaygın bir bileşenidir .
Hazırlık
Birçok magnezyum tuzunun bir çözeltisini alkali su ile birleştirmek , katı Mg(OH) 2'nin çökelmesine neden olur :
- Mg 2+ + 2OH − → Mg(OH) 2
Ticari ölçekte, Mg(OH) 2 , deniz suyunun kireç (Ca(OH) 2 ) ile işlenmesiyle üretilir . 600 m 3 deniz suyu (158.503 ABD galon), Mg (OH) bir ton ilgili verdiği 2 . Ca(OH) 2 , Mg(OH) 2'den çok daha fazla çözünür , dolayısıyla ikincisi katı olarak çöker:
kullanır
MgO'nun öncüsü
Endüstriyel olarak üretilen çoğu Mg(OH) 2 ve ayrıca çıkarılan küçük miktar, kaynaşmış magnezyaya (MgO) dönüştürülür . Magnezya hem zayıf bir elektrik iletkeni hem de mükemmel bir termal iletken olduğu için değerlidir.
Sağlık
Metabolizma
Magnezyum hidroksit kullanılan süspansiyon , bir ya olarak antasit ya da bir laksatif konsantrasyonuna bağlı olarak,.
Hidroksit, magnezyum bir antasit olarak, yaklaşık olarak 0.5-1.5 miktarında kullanıldı yetişkinlerde g ve basit çalışır nötrleştirme hangi, hidroksit iyonları Mg (OH) elde 2 ile birleştirmek asidik H + iyonları ile hidroklorik asit şeklinde üretilen paryetal hücrelerin içinde mide suyu üretmek için.
Müshil olarak, magnezyum hidroksit 2-5 g dozlanır ve çeşitli şekillerde çalışır. İlk olarak, Mg 2+ bağırsak yolundan zayıf bir şekilde emilir, bu nedenle çevre dokudan ozmoz yoluyla su çeker . Su içeriğindeki bu artış sadece dışkıyı yumuşatmakla kalmaz, aynı zamanda bağırsaktaki dışkı hacmini (intralüminal hacim) arttırır ve bu da bağırsak hareketliliğini doğal olarak uyarır . Ayrıca, Mg2 + iyonları kolesistokinin (CCK) salınımına neden olur , bu da intraluminal su, elektrolit birikimi ve artan bağırsak hareketliliği ile sonuçlanır. Bazı kaynaklar, bazik çözeltiler (yani, hidroksit iyonlarının çözeltileri) kuvvetli bir şekilde müshil olmadığından ve MgSO gibi bazik olmayan Mg2 + çözeltileri olmadığından, hidroksit iyonlarının kendilerinin magnezya sütünün müshil etkilerinde önemli bir rol oynamadığını iddia eder. 4 , eşit derecede güçlü müshillerdir, köstebek için köstebek.
Magnezyum hidroksitten gelen magnezyumun sadece küçük bir miktarı genellikle bağırsak tarafından emilir (magnezyum eksikliği olmadığı sürece). Bununla birlikte, magnezyum esas olarak böbrekler tarafından atılır, bu nedenle böbrek yetmezliği olan birinin günlük olarak magnezyum sütü tüketmesi teoride hipermagnezemiye yol açabilir . Emilmeyen ilaç dışkıyla atılır; emilen ilaç hızla idrarla atılır.

Magnezya sütünün tarihi
4 Mayıs 1818'de Amerikalı mucit John Callen, magnezyum hidroksit için bir patent (No. X2952) aldı. 1829'da Sir James Murray , İrlanda Lord Teğmeni Anglesey Markisi'nin mide ağrısını tedavi etmek için kendi tasarımının "yoğunlaştırılmış sıvı magnezya çözeltisi" preparatını kullandı . Bu o kadar başarılı oldu ki (Avustralya'da ilan edildi ve 1838'de Kraliyet Cerrahlar Koleji tarafından onaylandı), Anglesey'e ve müteakip iki Lords Teğmen'e asistan doktor olarak atandı ve şövalye oldu. Sıvı magnezya ürünü, 1873'teki ölümünden iki yıl sonra patentlendi.
Magnezya sütü terimi ilk olarak 1872'de Charles Henry Phillips tarafından yaklaşık % 8 a/ h'de formüle edilmiş bir magnezyum hidroksit süspansiyonu için kullanılmıştır . Tıbbi kullanım için Phillips'in Magnesia Sütü markası altında satıldı .
Adı bir noktada ait olabilir rağmen GlaxoSmithKline , USPTO tescilleri "Magnesia Süt" ve "Magnesia Phillips'in Milk" hem atanmış göstermek Bayer İngiltere'de 1995'ten beri, marka olmayan (jenerik) adı "Magnezyum Sütü" ve "Phillips Magnesia Sütü", "Magnezyum Kreması"dır (Magnezyum Hidroksit Karışımı, BP ).
Bu kullanılmıştır Steven Spielberg'in 'denilen ın ilk kısa filmi Amblin' .
Gıda katkı maddesi olarak
Doğrudan insan gıdasına eklenir ve FDA tarafından genel olarak güvenli olarak kabul edilir . E numarası E528 olarak bilinir .
Magnezyum hidroksit tıbbi kullanım için çiğnenebilir tabletler, kapsüller, toz ve bazen aromalı sıvı süspansiyonlar olarak pazarlanmaktadır . Bu ürünler mide asidini nötralize etmek ve hazımsızlığı ve mide ekşimesini gidermek için antasitler olarak satılmaktadır . Ayrıca kabızlığı hafifletmek için bir müshildir . Bir müshil olarak, magnezyanın ozmotik kuvveti vücuttan sıvı çekmek için hareket eder. Yüksek dozlar ishale yol açabilir ve vücudun potasyum kaynağını tüketebilir ve bazen kas kramplarına neden olabilir .
Antasit kullanımı için satılan bazı magnezyum hidroksit ürünleri ( Maalox gibi ) , mide-bağırsak yolundaki düz kas hücrelerinin kasılmalarını engelleyen alüminyum hidroksitin eklenmesi yoluyla istenmeyen müshil etkileri en aza indirecek ve böylece ozmotik etkilerin neden olduğu kasılmaları dengeleyecek şekilde formüle edilmiştir . magnezyum hidroksit.
Diğer niş kullanımlar
Magnezyum hidroksit ayrıca terlemeyi önleyici maddenin bir bileşenidir . Magnezyum hidroksit topikal olarak kullanıldığında aftlara (aftöz ülser) karşı faydalıdır .
Atık su arıtma
Magnezyum hidroksit tozu endüstriyel olarak asidik atık suları nötralize etmek için kullanılır. Aynı zamanda yapay resifler inşa etmek için Biorock yönteminin bir bileşenidir .
Yangın geciktirici
Doğal magnezyum hidroksit ( brucite ) ticari olarak yangın geciktirici olarak kullanılmaktadır. Endüstriyel olarak kullanılan çoğu magnezyum hidroksit sentetik olarak üretilir. Alüminyum hidroksit gibi, katı magnezyum hidroksit de duman bastırma ve alev geciktirici özelliklere sahiptir. Bu özellik, 332 °C'de (630 °F) maruz kaldığı endotermik ayrışmaya atfedilebilir :
- Mg(OH) 2 → MgO + H 2 O
Reaksiyon tarafından emilen ısı, ilgili maddenin tutuşmasını geciktirerek yangını geciktirir. Açığa çıkan su yanıcı gazları seyreltir. Magnezyum hidroksitin alev geciktirici olarak yaygın kullanımları arasında kablo yalıtımına katkı maddeleri (örneğin, yüksek kaliteli arabalar, denizaltılar , Airbus A380 ve Sony PlayStation için kablolar ), yalıtım plastikleri, çatı kaplaması (örneğin Londra Olimpiyat Stadyumu ) ve çeşitli alev geciktirici kaplamalar bulunur. Benzer alev geciktirici uygulamalarda kullanılan diğer mineral karışımları, Huntit ve hidromanyezitin doğal karışımlarıdır .
mineraloji

Brucite , Mg, mineral formu (OH) 2 1: 2: yaygın olarak da 1 'de ortaya doğada bulunan kil mineralleri olarak, diğerleri arasında klorit normal tek-değerli ve divalent ile doldurulmuş ara tabaka bir konuma sahiptir ki burada, katyon örneğin Na olarak + , K + , Mg 2+ ve Ca 2+ . Sonuç olarak, klorit ara tabakaları brusit ile çimentolanır ve şişemez veya büzülmez.
Mg2 + katyonlarının bir kısmının Al 3+ katyonları ile ikame edildiği Brusit, pozitif yüklü hale gelir ve katmanlı çift hidroksitin (LDH) ana temelini oluşturur . Hidrotalsit olarak LDH mineralleri güçlü anyon emicilerdir ancak doğada nispeten nadirdir.
Brusit ayrıca deniz suyuyla temas halinde çimento ve betonda kristalleşebilir . Gerçekten de Mg 2+ katyonu deniz suyunda Na +'dan hemen sonra ve Ca 2 +'dan önce en bol bulunan ikinci katyondur . Brusit şişen bir mineral olduğundan, betonda çekme gerilmesinden sorumlu yerel bir hacimsel genleşmeye neden olur. Bu, betonda çatlak ve yarıkların oluşmasına yol açarak deniz suyunda bozulmasını hızlandırır.
Aynı nedenle dolomit , beton yapımında inşaat agregası olarak kullanılamaz . Reaksiyon , magnezyum karbonat serbest alkali ile hidroksitler geniş brusit oluşumuna çimento gözenek suyu içinde potansiyel sunmaktadır.
- MgCO 3 + 2 NaOH → Mg (OH) 2 + Na 2 CO 3
İki ana alkali-agregat reaksiyonundan (AAR) biri olan bu reaksiyon, alkali-karbonat reaksiyonu olarak da bilinir .


