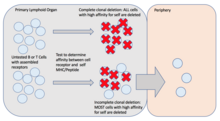
Klonal silme - Clonal deletion
Klonal delesyon yoluyla uzaklaştırılmasıdır apoptoz ve B hücreleri ve T hücreleri tamamıyla bağışıklık limfositlerine geliştirmeden önce öz için reseptörleri ifade etmektedirler. Bu, kendi kendine konakçı hücrelerin tanınmasını ve yok edilmesini önler, bu da onu bir tür negatif seçim veya merkezi tolerans haline getirir . Merkezi tolerans, B ve T lenfositlerinin kendilerine tepki vermesini engeller. Bu nedenle, klonal delesyon, bireylerin otoimmüniteye karşı korunmasına yardımcı olabilir . Klonal delesyonun en yaygın negatif seçim türü olduğu düşünülmektedir. Bağışıklık toleransının bir yöntemidir .
Keşif ve İşlev
Frank Macfarlane Burnet otoreaktif hücreler B ve T hücreleri milyonlarca içinde oluşturulan her ikisi, vücudun içinde var 1959'da yaptığı çalışmada ileri çoğalmasını önlemek için olgunlaşma öncesi sonlandırılır olacağını önerdi kemik iliği ve ikincisi olgunlaştıkça timüs dolayısıyla T. Bu lenfositlerin her biri, belirli bir epitopa veya bir antijenin, B hücresi ve T hücresi reseptörlerinin tanıdığı ve bağlandığı kısmına spesifiklik gösterir . Tanınan çok çeşitli epitoplar vardır ve sonuç olarak bazı B ve T lenfositlerinin kendini tanıma yeteneği ile gelişmesi mümkündür. B ve T hücreleri, henüz birincil lenfoid organlarda iken reseptörler geliştirdikten sonra kendi antijeni ile sunulur . Bu kendi antijeni için yüksek bir afinite sergileyen hücreler, genellikle daha sonra silinir, bu nedenle, konağın otoimmüniteye karşı korunmasına yardımcı olan döl oluşturamazlar. Böylelikle konakçı, bu antijen için bir tolerans veya kendi kendine tolerans geliştirir.
yer
B ve T lenfositleri , birincil lenfoid organları terk etmeden ve çevreye girmeden önce kendi MHC / peptit komplekslerine afiniteleri açısından test edilir . Kendi kendine antijen için yüksek afinite gösterirlerse, otoimmüniteyi önlemenin bir yöntemi klonal delesyondur. Bu, lenfositin antijen sunan hücreden (APC'ler) apoptotik sinyaller alacağı yerdir . Kendi kendine antijen için yüksek afinite ifade eden tüm lenfositlerin klonal delesyona uğramadığına dikkat etmek önemlidir. B lenfositleri ayrıca hafif zincir reseptör düzenlemesine, VH gen replasmanına katılabilir veya salınabilir ve daha sonra çevrede negatif seleksiyona uğrayabilir. T lenfositleri bunun yerine klonal tutuklama, klonal anerji ve klonal düzenlemeye tabi tutulabilir . Otoreaktif hücreler timusta veya kemik iliğinde klonal delesyondan kaçarsa, periferde konağın bir otoimmün hastalık elde etmesini önlemek için T düzenleyici hücreleri içeren mekanizmalar vardır . Bununla birlikte, birincil lenfoid organlardaki hem B hem de T hücreleri için, klonal delesyon, negatif seleksiyonun en yaygın şeklidir.
B Hücreleri
Kendi kendine hücreler için yüksek afinite gösteren B hücreleri, kemik iliği içinde klonal delesyona uğrayabilir. Bu, fonksiyonel B hücre reseptörü (BCR) birleştirildikten sonra gerçekleşir. Kendine afinitesi yüksek olan B hücrelerinin silinmemiş olması mümkündür çünkü bunlar, otomatik tepkimeli T hücrelerinden aktivasyon sinyalleri ve stimülasyon gerektirirler. Bu tür T hücreleri genellikle klonal silme yoluyla uzaklaştırılır ve otoreaktif B hücreleri uyarılmamış ve aktive edilmemiş halde bırakılır. Bu B hücreleri, onları uyarmak için otoreaktif bir T hücresi olmadan aktive edilemedikleri için çevrede bile bir tehdit oluşturmazlar.
T Hücreleri
T hücrelerinin% 2 ila% 5'i oto-reaktif reseptörler geliştirir. Bunların çoğu, klonal silme ile negatif seleksiyona uğrar.
Timik Korteks
Kendi MHC / peptid kompleksleri için yüksek afinite gösteren T hücreleri, timusta klonal delesyona uğrayabilir . Timik dendritik hücreler ve makrofajlar , timik korteksteki otoreaktif T hücrelerine gönderilen apoptotik sinyallerden sorumlu görünmektedir.
Timik Medulla
T hücreleri, kendi MHC / peptid kompleksleri için yüksek afinite ifade ederlerse timik medulla içinde klonal delesyona uğrama fırsatına da sahiptirler. Timik kortekste pozitif seleksiyon meydana gelir, bu da bir hücrenin korteks içinde pozitif seleksiyona ve daha sonra medullada klonal delesyon yoluyla negatif seleksiyona girmesinin mümkün olduğunu düşündürür. Medulla içindeki klonal delesyondan epitel hücreleri sorumludur. Bu medüller epitel hücreleri , bu hücrelerin vücudun diğer kısımlarına özgü proteinleri T lenfositlerine sunmasına izin veren bir otoimmün düzenleyici (AIRE) eksprese eder. Bu, belirli bir vücut bölümünden bir proteini tanıyan otoreaktif T hücrelerinin ortadan kaldırılmasına yardımcı olur.
Tam ve Eksik Klonal Silme
Tam klonal delesyon, kendi antijeni için yüksek afinite ifade eden tüm B ve T lenfositlerinin apoptozuyla sonuçlanır. Eksik klonal delesyon, çoğu otoreaktif B ve T lenfositlerinin apoptozuna neden olur. Tam klonal delesyon , konakçı için olumsuz etkilere sahip olan moleküler taklit için fırsatlara yol açabilir . Bu nedenle, eksik klonal silme, konağın yabancı antijenleri ve kendi antijenlerini tanıma yeteneği arasında bir dengeye izin verir.
Sömürü Yöntemleri
Moleküler Taklit
Klonal delesyon, mikroorganizmaların konakta bulunan proteinlere benzer epitoplar geliştirmesi için bir teşvik sağlar. Otomatik yanıt veren hücrelerin çoğu klonal delesyona uğradığından, bu, konakçı antijene benzer epitoplara sahip mikroorganizmaların, T ve B lenfositleri tarafından tanınmadan ve saptanmadan kaçmasına izin verir. Bununla birlikte, tespit edilirse, bu, mikroorganizma ve konakçı antijen üzerindeki epitopların benzerliğinden dolayı bir otoimmün tepkiye yol açabilir. Bunun örnekleri Streptococcus pyogenes ve Borrelia burgdorferi'de görülmektedir . Moleküler taklitin bir otoimmün hastalığa yol açması mümkündür, ancak nadirdir.
Süperantijenler
Süperantijenler , viral veya bakteriyel proteinlerden oluşur ve timusta ifade edildiğinde klonal silme sürecini ele geçirebilir, çünkü kendi MHC / peptidleriyle T-hücre reseptörü (TCR) etkileşimine benzerler . Böylece, bu süreç sayesinde süperantijenler, aynı kökenli T hücrelerinin olgunlaşmasını etkili bir şekilde önleyebilir.
Referanslar
- ^ a b c d e f g h i j k l m n Jenni., Punt; A., Stranford, Sharon; P., Jones, Patricia; Janis., Kuby (2013/01/01). Kuby immünolojisi . WH Freeman. ISBN 9781429219198 . OCLC 820117219 .
- ^ a b c d e f g E., Paul, William (Ekim 2015). Bağışıklık . ISBN 9781421418025 . OCLC 948563239 .
- ^ a b c d e f g h i j k l m n Rose, Noel R. (2015-06-21). "Moleküler Taklit ve Klonal Delesyon: Yeni Bir Bakış" . Teorik Biyoloji Dergisi . 375 : 71–76. doi : 10.1016 / j.jtbi.2014.08.034 . ISSN 0022-5193 . PMC 4344433 . PMID 25172771 .
- ^ a b Kitz, Alexandra; Hafler, David A. (2015). "Timik Seçim: Kendi Kendine Doğru Olmak İçin" . Bağışıklık . 42 (5): 788–789. doi : 10.1016 / j.immuni.2015.05.007 . PMID 25992854 .
- ^ Grossman, Zvi; Paul, William E (2015-04-10). "Lenfositlerin Dinamik Ayarı: Fizyolojik Temel, Mekanizmalar ve İşlev". Yıllık İmmünoloji İncelemesi . 33 (1): 677–713. doi : 10.1146 / annurev-immunol-032712-100027 . PMID 25665077 .
- ^ a b c d e Klein, Ludger; Kyewski, Bruno; Allen, Paul M .; Hogquist, Kristin A. (2014). "T hücre repertuarının pozitif ve negatif seçimi: timositlerin gördükleri (ve görmedikleri)" . Nature Reviews Immunology . 14 (6): 377–391. doi : 10.1038 / nri3667 . PMC 4757912 . PMID 24830344 .
Dış bağlantılar
- ABD Ulusal Tıp Kütüphanesi Tıbbi Konu Başlıkları'nda (MeSH) klonal + delesyon