alfavirüs -Alphavirus
ve
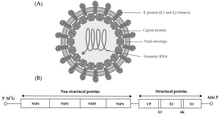
Alphavirus , Togaviridae ailesindekitekcins olan RNA virüslerinin bir cinsidir. Alfavirüsler grup IV ait Baltimore sınıflandırma arasında virüs a, pozitif sens, tek iplikçikli bir RNA genomu. İnsanlar, kemirgenler, balıklar, kuşlar gibiçeşitli omurgalıları ve atlar gibi daha büyük memelileri ve ayrıca omurgasızları enfekte eden 32 alfavirüs vardır. Hem omurgalıları hem de eklembacaklıları enfekte edebilen alfavirüsler, çift konaklı alfavirüsler olarak adlandırılırken, Eilat virüsü ve Yada yada virüsü gibi böceğe özgü alfavirüsler, yetkin arthropod vektörleriyle sınırlıdır. Türler ve bireyler arasındakibulaşmaesas olarak sivrisinekler aracılığıyla gerçekleşir ve alfavirüsleri arbovirüsler veya eklembacaklılarla taşınan virüslerkoleksiyonunun bir üyesiyapar. Alfavirüs parçacıkları zarflıdır, 70 nm çapa sahiptir, küresel olma eğilimindedir (biraz pleomorfik olmasına rağmen) ve 40 nm izometrik nükleokapside sahiptir .
Genetik şifre
| Alpha_E1_glycop | |||||||||
|---|---|---|---|---|---|---|---|---|---|
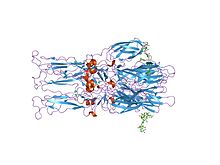 Semliki Forest virüsünden füzyon glikoprotein E1'in homotrimerinin kristal yapısı
| |||||||||
| tanımlayıcılar | |||||||||
| Sembol | Alpha_E1_glycop | ||||||||
| Pfam | PF01589 | ||||||||
| InterPro | IPR002548 | ||||||||
| SCOP2 | 1rer / KAPSAM / SUPFAM | ||||||||
| TCDB | 1.G | ||||||||
| OPM süper ailesi | 109 | ||||||||
| OPM proteini | 1rer | ||||||||
| |||||||||
| Alpha_E2_glycop | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Alfavirüslerin E2 glikoproteininin haritalanması
| |||||||||
| tanımlayıcılar | |||||||||
| Sembol | Alpha_E2_glycop | ||||||||
| Pfam | PF00943 | ||||||||
| InterPro | IPR000936 | ||||||||
| TCDB | 1.G | ||||||||
| OPM süper ailesi | 109 | ||||||||
| OPM proteini | 2 porsuk | ||||||||
| |||||||||
| Alpha_E3_glycop | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| tanımlayıcılar | |||||||||
| Sembol | Alpha_E3_glycop | ||||||||
| Pfam | PF01563 | ||||||||
| InterPro | IPR002533 | ||||||||
| TCDB | 1.G | ||||||||
| OPM süper ailesi | 109 | ||||||||
| |||||||||
Alfavirüsler, tek bir pozitif-sens RNA dizisinden oluşan bir genoma sahip küçük, küresel, zarflı virüslerdir. Toplam genom uzunluğu 11.000 ile 12.000 nükleotit arasında değişir ve 5' başlıklı ve 3' poli-A kuyruğuna sahiptir . Dört yapısal olmayan protein geni, genomun 5' üçte ikisinde kodlanırken, üç yapısal protein, genomun 3' üçte biri ile aynı çizgide olan bir subgenomik mRNA'dan çevrilir.
Genomda yapısal olmayan ve yapısal olmak üzere iki açık okuma çerçevesi (ORF) vardır. Birincisi yapısal değildir ve viral RNA'nın transkripsiyonu ve replikasyonu için gerekli proteinleri (nsP1-nsP4) kodlar. İkincisi, üç yapısal proteini kodlar : çekirdek nükleokapsid proteini C ve bir heterodimer olarak birleşen zarf proteinleri P62 ve E1 . Viral membran bağlantılı yüzey glikoproteinleri , reseptör tanıma ve membran füzyonu yoluyla hedef hücrelere girişten sorumludur .
Yapısal proteinler
Proteolitik E2 ve E3 içine P62 olgunlaşma viral yüzeyinde bir değişikliğe neden olur. Birlikte E1, E2 ve bazen E3, glikoprotein "sivri uçları" bir E1/E2 dimerini veya bir E1/E2/E3 trimerini oluşturur, burada E2 merkezden tepe noktalarına uzanır, E1 tepe noktaları arasındaki boşluğu doldurur ve E3, varsa, spike'ın distal ucundadır. Virüsün endozomun asitliğine maruz kalması üzerine , E1 , hücresel ve viral membranları birlikte sürmek için füzyon adımı için gerekli olan bir E1 homotrimerini oluşturmak üzere E2'den ayrışır . Alfaviral glikoprotein E1, influenza virüsü ve HIV'de bulunan sınıf I füzyon proteinlerinden yapısal olarak farklı olan bir sınıf II viral füzyon proteinidir . Yapı Semliki Forest virüsü, üç ile flaviviral glikoprotein E benzer bir yapı, ortaya yapısal etki , aynı olarak primer dizi düzenlemesi. E2 glikoproteini , sitoplazmik alanı yoluyla nükleokapsid ile etkileşime girme işlevi görürken, ektodomain bir hücresel reseptörün bağlanmasından sorumludur . Çoğu alfavirüs, periferik protein E3'ü kaybeder, ancak Semliki virüslerinde viral yüzeyle ilişkili kalır.
yapısal olmayan proteinler
Tek bir poliprotein olarak üretilen dört yapısal olmayan protein (nsP1–4) virüsün replikasyon mekanizmasını oluşturur. Poliproteinin işlenmesi, genom replikasyonu sırasında RNA şablonu kullanımını etkileyen P2/3 bağlantısındaki bölünme ile yüksek düzeyde düzenlenmiş bir şekilde gerçekleşir. Bu site, dar bir yarığın tabanında yer alır ve kolayca erişilebilir değildir. Bir kez bölündüğünde nsP3, nsP2'yi çevreleyen bir halka yapısı oluşturur. Bu iki protein kapsamlı bir arayüze sahiptir.
P2/P3 arayüz bölgesinde sitopatik olmayan virüsler veya sıcaklığa duyarlı bir fenotip kümesi üreten nsP2'deki mutasyonlar. nsP2 sitopatik olmayan mutasyonların yerinin karşısındaki P3 mutasyonları, P2/3'ün verimli bölünmesini önler. Bu da viral RNA üretim seviyelerini değiştiren RNA enfektivitesini etkiler.
Viroloji
Virüs 60-70 nanometre çapındadır. Zarflı, küreseldir ve ~12 kilobazlık pozitif iplikli bir RNA genomuna sahiptir. Genom iki poliproteini kodlar. İlk poliprotein dört yapısal olmayan birimden oluşur: N terminalinden C terminaline - nsP1, nsP2, nsP3 ve nsP4. İkincisi, beş ifade biriminden oluşan yapısal bir poliproteindir: N terminalinden C terminaline - Kapsid, E3, E2, 6K ve E1. Bir alt genomik pozitif iplikli RNA - 26S RNA - bir negatif iplikli RNA ara maddesinden kopyalanır. Bu, viral yapısal proteinlerin sentezi için şablon görevi görür. Çoğu alfavirüs, viral RNA sentezinin düzenlenmesinde yer alan korunmuş alanlara sahiptir.
40 nanometre çapındaki nükleokapsid, kapsid proteininin 240 kopyasını içerir ve T = 4 ikosahedral simetriye sahiptir. E1 ve E2 viral glikoproteinleri, lipid çift tabakasına gömülüdür. Tek E1 ve E2 molekülleri, heterodimerler oluşturmak üzere birleşir. E1-E2 heterodimerleri, E2 proteini ve nükleokapsid monomerleri arasında bire bir temaslar oluşturur. E1 ve E2 proteinleri, virüs ile konakçı hücre arasındaki temasa aracılık eder.
Birkaç reseptör tanımlanmıştır. Bunlara yasaklama , fosfatidilserin , glikozaminoglikanlar ve ATP sentaz β alt birimi dahildir.
Replikasyon sitoplazma içinde gerçekleşir ve viryonlar, virüs kodlu yüzey glikoproteinleri E2 ve E1'in asimile edildiği plazma zarından tomurcuklanarak olgunlaşır.
Bu iki glikoprotein, nötralizasyon ve hemaglütinasyon inhibisyonu dahil olmak üzere çok sayıda serolojik reaksiyon ve testin hedefidir. Alfavirüsler, bu reaksiyonlarda çeşitli derecelerde antijenik çapraz reaktivite gösterir ve bu, yedi antijenik kompleks, 32 tür ve birçok alt tip ve çeşidin temelini oluşturur. E2 proteini çoğu nötralize edici epitopun yeridir, E1 proteini ise daha fazla korunmuş, çapraz reaktif epitop içerir.
Evrim
Bu taksonun bir araştırması, bu virüs grubunun deniz kökenli - özellikle Güney Okyanusu - olduğunu ve daha sonra hem Eski hem de Yeni Dünya'ya yayıldıklarını göstermektedir.
Bu cinste üç alt grup vardır: Semliki Ormanı virüsü alt grubu (Semliki Ormanı, O'nyong-nyong ve Ross Nehri virüsleri); doğu at ensefaliti virüsü alt grubu (doğu at ensefaliti ve Venezuela at ensefaliti virüsleri) ve Sindbis virüsü alt grubu. Coğrafi olarak Eski Dünya ile sınırlı olan Sindbis virüsü, Eski Dünya'da da bulunan Semliki Ormanı virüsü alt grubuna göre Yeni Dünya virüsleri olan doğu at ensefaliti alt grubu ile daha yakından ilişkilidir.
taksonomi
Aşağıdaki türler cinse atanır:
- aura virüsü
- Barmah Ormanı virüsü
- Bebaru virüsü
- Caaingua virüsü
- Cabassou virüsü
- chikungunya virüsü
- Doğu at ensefalit virüsü
- Eilat virüsü
- Everglades virüsü
- Fort Morgan virüsü
- Geta virüsü
- Highlands J virüsü
- Madariaga virüsü
- Mayaro virüsü
- Middelburg virüsü
- Mosso das Pedras virüsü
- Mucambo virüsü
- Ndumu virüsü
- O'nyong'nyong virüsü
- Pixuna virüsü
- Rio Negro virüsü
- Ross Nehri virüsü
- Somon pankreas hastalığı virüsü
- Şemliki Ormanı virüsü
- Sindbis virüsü
- Güney fil foku virüsü
- tonlama virüsü
- Trokara virüsü
- Una virüsü
- Venezuela at ensefalit virüsü
- Batı at ensefalit virüsü
- Whataroa virüsü
Yedi kompleks şunlardır:
- Barmah Ormanı virüs kompleksi
-
Doğu at ensefalit kompleksi
- Doğu at ensefalit virüsü (yedi antijenik tip)
- Middelburg virüs kompleksi
- Ndumu virüs kompleksi
-
Şemliki Ormanı virüs kompleksi
- Bebaru virüsü
- chikungunya virüsü
- Geta virüsü
-
Mayaro virüsü
- Alt tip: Una virüsü
-
O'nyong'nyong virüsü
- Alt tip: İbo-Ora virüsü
-
Ross Nehri virüsü
- Alt tip: Sagiyama virüsü
-
Şemliki Ormanı virüsü
- Alt tip: Me Tri virüsü
-
Venezüella at ensefalit kompleksi
- Cabassou virüsü
- Everglades virüsü
- Mosso das Pedras virüsü
- Mucambo virüsü
- paramana virüsü
- Pixuna virüsü
- Rio Negro virüsü
- Trokara virüsü
- Alt tip: Bijou Bridge virüsü
- Venezuela at ensefalit virüsü
- Batı at ensefalit kompleksi
- Bu kompleks içindeki rekombinantlar
- Buggy Creek virüsü
- Fort Morgan virüsü
- Highlands J virüsü
- Batı at ensefalit virüsü
-
sınıflandırılmamış
- Eilat virüsü
- Mwinilunga alfavirüsü
- Salmonid Alfavirüsü
- Güney fil foku virüsü
- tonlama virüsü
- Caaingua virüsü
Notlar
Barmah Forest virüsü, Semliki Forest virüsü ile ilişkilidir. Middelburg virüsü, ayrı bir kompleks olarak sınıflandırılmasına rağmen, Semliki Ormanı virüs grubunun bir üyesi olabilir.
Cinsin Eski Dünya'da böcekle taşınan bir bitki virüsünden evrimleşmiş olması muhtemel görünüyor.
Sindbis virüsü Güney Amerika'da ortaya çıkmış olabilir. At ensefalit virüsleri ve Sindbis virüsü ilişkilidir.
Eski Dünya ve Yeni Dünya virüslerinin 2000 ila 3000 yıl önce birbirinden ayrıldığı görülüyor. Venezüella at ensefaliti virüsü ile doğu at virüsü arasındaki farklılık ~ 1400 yıl önce olmuş gibi görünüyor.
Klanı enfekte eden balık, diğer türlere göre bazal gibi görünüyor.
Güney deniz fili virüsü, Sinbis soyundan geliyor gibi görünüyor.
Patogenez ve bağışıklık tepkisi
| Virüs | İnsan Hastalığı | Omurgalı Rezervuarı | Dağıtım |
|---|---|---|---|
| Barmah Ormanı virüsü | insanlar | Avustralya | |
| chikungunya virüsü | Döküntü, artrit | Primatlar, insanlar | Afrika, Latin Amerika, Hindistan , Güneydoğu Asya |
| Doğu at ensefalit virüsü | ensefalit | kuşlar | Amerika |
| Mayaro virüsü | Döküntü, artrit | Primatlar, insanlar | Güney Amerika |
| O'nyong'nyong virüsü | Döküntü, artrit | Primatlar , İnsanlar | Afrika |
| Ross Nehri virüsü | Döküntü, artrit | memeliler, insanlar | Avustralya, Güney Pasifik |
| Şemliki Ormanı virüsü | Döküntü, artrit | kuşlar | Afrika |
| Sindbis virüsü | Döküntü, artrit | kuşlar | Avrupa , Afrika , Avustralya |
| tonlama virüsü | ensefalit | insanlar | Güney Amerika |
| Una virüsü | Döküntü, artrit | Primatlar, insanlar | Güney Amerika |
| Venezuela at ensefalit virüsü | ensefalit | Kemirgenler , atlar | Amerika |
| Batı at ensefalit virüsü | ensefalit | Kuşlar, memeliler | Kuzey Amerika |
İnsan hastalığına neden olma yeteneği ile dünya çapında dağılmış birçok alfavirüs vardır. Enfeksiyöz artrit , ensefalit , döküntüler ve ateş en sık görülen semptomlardır. İnsanlar ve atlar gibi daha büyük memeliler genellikle çıkmaz konaklardır veya viral bulaşmada küçük bir rol oynarlar; bununla birlikte, Venezüella at ensefaliti durumunda , virüs esas olarak atlarda çoğalır. Diğer vakaların çoğunda virüs doğada sivrisinekler, kemirgenler ve kuşlarda bulunur.
Karasal alfavirüs enfeksiyonları, sivrisinekler gibi böcek vektörleri tarafından yayılır. Bir insan enfekte sivrisinek tarafından ısırıldığında, virüs kan dolaşımına girerek viremiye neden olabilir . Alfavirüs ayrıca nöronlar içinde büyüyebildiği ve çoğalabildiği CNS'ye girebilir . Bu, ölümcül olabilen ensefalite yol açabilir .
Bir kişiye bu belirli virüs bulaştığında, bağışıklık sistemi virüs partiküllerini temizlemede rol oynayabilir. Alfavirüsler interferon üretimine neden olabilir . Antikorlar ve T hücreleri de rol oynar. Nötralize edici antikorlar ayrıca daha fazla enfeksiyon ve yayılmayı önlemek için önemli bir rol oynar.
Teşhis, önleme ve kontrol
Teşhis, virüsün kolayca izole edilip tanımlanabileceği klinik örneklere dayanır. Şu anda mevcut hiçbir alfavirüs aşısı yoktur. Kovucularla vektör kontrolü, koruyucu giysiler, üreme alanı tahribatı ve püskürtme, tercih edilen önleyici tedbirlerdir.
Araştırma
Alfavirüsler, gen tedavisi araştırmacılarının ilgisini çekmektedir , özellikle Ross River virüsü, Sindbis virüsü , Semliki Forest virüsü ve Venezüella at ensefalit virüsü, gen aktarımı için viral vektörler geliştirmek için kullanılmıştır. Alfaviral zarflar ve retroviral kapsidler ile oluşturulabilen kimerik virüsler özellikle ilgi çekicidir. Bu tür kimeralara psödotipli virüsler denir. Retrovirüslerin veya lentivirüslerin alfaviral zarf psödotipleri, taşıdıkları genleri, alfaviral zarf proteinleri E2 ve E1 tarafından tanınan ve enfekte olan geniş potansiyel konakçı hücre aralığına entegre edebilir . Viral genlerin stabil entegrasyonuna bu vektörlerin retroviral iç kısımları aracılık eder. Alfavirüslerin gen terapisi alanında kullanımına yönelik sınırlamalar , hedefleme eksikliği nedeniyle vardır, ancak, E2 yapısında korunmamış bir döngüde değişken antikor alanlarının eklenmesi yoluyla, belirli hücre popülasyonları hedeflenmiştir. Ayrıca, gen terapisi için bütün alfavirüslerin kullanımı, hem enfeksiyon üzerine apoptozun indüklenmesinde birkaç dahili alfaviral protein yer aldığından hem de alfaviral kapsid, mRNA'nın konakçı hücrelere yalnızca geçici girişine aracılık ettiği için sınırlı bir etkinliğe sahiptir. Bu sınırlamaların hiçbiri retrovirüslerin veya lentivirüslerin alfaviral zarf psödotiplerini kapsamaz. Bununla birlikte, Sindbis virüs zarflarının ekspresyonu apoptoza yol açabilir ve bunların Sindbis virüsü zarf psödotipli retrovirüsleri tarafından enfeksiyon üzerine konakçı hücrelere dahil edilmesi de hücre ölümüne yol açabilir. Sindbis viral zarflarının toksisitesi, Sindbis psödotiplerini üretmek için yapılandırılmış paketleme hücrelerinden elde edilen çok düşük üretim titrelerinin nedeni olabilir. Alfavirüsleri içeren bir başka araştırma dalı aşılamadır. Alfavirüsler, hümoral ve T-hücresi bağışıklık tepkilerini verimli bir şekilde indükleyen replikon vektörleri yaratmak için tasarlanmaya uygundur . Bu nedenle viral, bakteriyel, protozoan ve tümör antijenlerine karşı aşılama için kullanılabilirler.
Tarih
Başlangıçta, Togaviridae ailesi , Alphavirus cinsi içinde şimdi Flaviviruses olarak adlandırılanları içeriyordu . Flavivirüsler, dizilemenin gelişmesi nedeniyle alfavirüslerle yeterli farklılıklar kaydedildiğinde kendi aileleri haline geldi. Rubella virüsü daha önce Togaviridae ailesine kendi Rubivirus cinsi içinde dahildi , ancak şimdi kendi ailesi Matonaviridae içinde sınıflandırılıyor . Alphavirus artık ailedeki tek cinstir.
- 1930 - Batı at ensefaliti virüsü ilk olarak Amerika Birleşik Devletleri'nde izole edildi (şimdiye kadar izole edilen ilk alfavirüs)
- 1933 - Doğu at ensefaliti virüsü ilk olarak Amerika Birleşik Devletleri'nde izole edildi.
- 1938 - Venezüella at ensefaliti izole edildi.
- 1941 - Amerika Birleşik Devletleri'nde Batı at ensefaliti salgını görüldü. 300.000 atı ve 3.336 insanı etkiler.
- 1941 - Norman Gregg , kızamıkçık salgını sonrasında çok sayıda kataraktlı çocuğun olduğunu fark etti . Bu ve diğer kusurlar daha sonra konjenital kızamıkçık sendromu altında sınıflandırılır .
- 1942 - Semliki Ormanı virüsü Uganda , Bwamba İlçesi, Buliyama'da izole edildi .
- 1952 - Sindbis virüsü , Mısır , Kahire'nin 40 mil (64 km) kuzeyindeki Sindbis sağlık bölgesinde izole edildi .
- 1959 - Ross River virüsü izole edilmiştir Aedes vigilax (şimdi olarak bilinen sivrisinekler Ochlerotatus vigilax noktasında yakalanmışlardır) Ross River Avustralya'da.
- 1963 – Salgın poliartrite neden olan (çoğunlukla Avustralya'da görülen) Ross River virüsü Doherty ve arkadaşları tarafından izole edildi.
- 1971 - Güney Teksas'ta son Venezuela at ensefaliti salgını atlarda görüldü .
- 1986 - Barmah Forest virüsünün Avustralya'da insan hastalığına neden olduğu belirlendi.
- 2001 - Bilim adamları çözüldü kristal yapısını ait glikoprotein kabuk arasında Semliki Forest virüsü .
- 2005-2006 - La Réunion adasında ve Hint Okyanusu'ndaki çevre adalarda chikungunya virüsünün büyük salgını
- 2006 - 1.5 milyondan fazla vakanın bildirildiği Hindistan'da chikungunya virüsünün büyük salgını
Ayrıca bakınız
Kaynaklar
- "Arbovirüsler" . Viroloji-çevrimiçi .
- "ICTV Kaynakları" . ICTV . Arşivlenmiş orijinal 12 Şubat 2006 tarihinde.
- Smerdou, C.; Liljeström, P. (2000). "Alfavirüs vektörleri: protein üretiminden gen tedavisine". Gen Tedavisi ve Regülasyonu . 1 (1): 33–63. ISSN 1568-5586 .
- Rayner JO, Dryga SA, Kamrud KI (2002). "Alfavirüs vektörleri ve aşılama". Tıbbi Virolojide İncelemeler . 12 (5): 279–96. doi : 10.1002/rmv.360 . PMID 12211042 . S2CID 21432844 .
- Rhême, Céline; Ehrengruber, Markus U.; Grandgirard, Denis. "Alfaviral sitotoksisite ve vektör gelişimindeki etkisi" . Deneysel Fizyoloji . 90 (1): 45–52. doi : 10.1113/expphysicol.2004.028142 . PMID 15542620 .
- Schmaljohn, Alan L.; McClain, David (1996). "54. Alfavirüsler (Togaviridae) ve Flavivirüsler (Flaviviridae)" . Baron'da, Samuel (ed.). Tıbbi Mikrobiyoloji (4. baskı). Galveston'daki Texas Üniversitesi Tıp Şubesi. ISBN'si 0-9631172-1-1. PMID 21413253 . NBK7633.