uranyum dioksit - Uranium dioxide
|
|
| İsimler | |
|---|---|
|
IUPAC adları
Uranyum dioksit
Uranyum(IV) oksit |
|
| Diğer isimler
Urania
Uranöz oksit |
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| Kimyasal Örümcek | |
| ECHA Bilgi Kartı |
100.014.273 |
| AT Numarası | |
|
PubChem Müşteri Kimliği
|
|
| RTECS numarası | |
| ÜNİİ | |
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikler | |
| UO 2 | |
| Molar kütle | 270.03 g/mol |
| Dış görünüş | Siyah toz |
| Yoğunluk | 10.97 g / cm 3 |
| Erime noktası | 2.865 °C (5.189 °F; 3.138 K) |
| çözünmez | |
| Yapı | |
| Florit (kübik), cF12 | |
| Fm 3 m, No. 225 | |
|
a = 547.1 pm
|
|
| Dörtyüzlü (O 2− ); kübik (U IV ) | |
| Termokimya | |
|
Std molar
entropi ( S |
78 J·mol -1 ·K -1 |
|
Std
oluşum entalpisi (Δ f H ⦵ 298 ) |
-1084 kJ·mol -1 |
| Tehlikeler | |
| Güvenlik Bilgi Formu | ICSC 1251 |
| GHS piktogramları |
  
|
| GHS Sinyal kelimesi | Tehlike |
| H300 , H330 , H373 , H400 , H410 , H411 | |
| P260 , P264 , P270 , P271 , P273 , P284 , + 310 P301 , P304 + = 340 , P310 , P314 , P320 , P321 , P330 , P391 , P403 + 233 , P405 , P501 | |
| NFPA 704 (ateş elması) | |
| Alevlenme noktası | Yok |
| Bağıntılı bileşikler | |
|
Triuranyum oktoksit Uranyum trioksit |
|
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
|
|
|
| Bilgi kutusu referansları | |
Uranyum dioksit ya da uranyum (IV) oksit ( U O 2 ) olarak da bilinen Urania veya uranlı oksit , bir bir oksit ve uranyum ve siyah, bir radyoaktif , kristal halinde doğal mineral oluşur, toz uraninit . Nükleer reaktörlerde nükleer yakıt çubuklarında kullanılır . MOX yakıtı olarak uranyum ve plütonyum dioksitlerin bir karışımı kullanılır . 1960 öncesi seramik sırlarında ve camlarda sarı ve siyah renk olarak kullanılmıştır .
Üretme
Uranyum dioksit, uranyum trioksitin hidrojen ile indirgenmesiyle üretilir .
- UO 3 + H 2 → UO 2 + H 2 O, 700 °C'de (973 K)
Bu reaksiyon , nükleer yeniden işleme ve uranyum zenginleştirme yoluyla nükleer yakıtın yaratılmasında önemli bir rol oynar .
Kimya
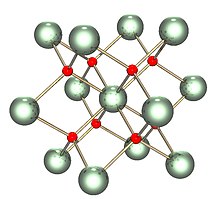
Yapı
Katı izo- (aynı şekilde bir yapıya sahiptir) ile florit ( kalsiyum florür Her bir U kübik düzenlemede sekiz O yakın komşuları ile çevrilidir). Ayrıca seryum , toryum , plütonyum ve neptünyumun dioksitleri de aynı yapılara sahiptir. Başka hiçbir elementel dioksit florit yapıya sahip değildir. Erime üzerine, ölçülen ortalama UO koordinasyonu kristal katıda (UO 8 küp) 8'den eriyikte 6,7±0,5'e (3270 K'da) düşer. Bu ölçümlerle tutarlı modeller, eriyiğin esas olarak UO 6 ve UO 7 çokyüzlü birimlerinden oluştuğunu gösterir , burada çokyüzlüler arasındaki bağlantıların kabaca 2 ⁄ 3'ü köşe paylaşımı ve 1 ⁄ 3'ü kenar paylaşımıdır.
Oksidasyon
Uranyum dioksit olan oksitlenmiş ile temas halinde oksijen için triuranium octaoxide .
- 3 UO 2 + O 2 → U 3 O 8 , 700 °C'de (970 K)
Elektrokimya olarak uranyum dioksit ayrıntılı olarak araştırılmıştır galvanik korozyon uranyum dioksit kullanılır hızını kontrol eden nükleer yakıt erir. Daha fazla ayrıntı için kullanılmış nükleer yakıta bakın. Su , plütonyum ve uranyum metallerinin oksidasyon hızını arttırır .
karbonizasyon
Uranyum dioksit olan karbonize ile temas halinde karbon oluşturan, uranyum karbid ve karbon monoksit .
- .
Bu işlem, bir alt yapılmalıdır atıl gaz olarak uranyum karbid kolayca geri oksitlenir uranyum oksit .
kullanır
Nükleer yakıt
UO 2 ağırlıklı olarak kullanılan nükleer yakıt , özellikle UO olarak, 2 veya UO karışımı olarak 2 ve puo 2 ( plütonyum dioksit karışık oksit (adlandırılır) MOX yakıt formunda) yakıt çubuğu içinde , nükleer reaktörler .
Uranyum dioksitin termal iletkenliğinin uranyum , uranyum nitrür , uranyum karbür ve zirkonyum kaplama malzemesi ile karşılaştırıldığında çok düşük olduğuna dikkat edin . Bu düşük termal iletkenlik, yakıt peletlerinin merkezlerinde lokalize aşırı ısınmaya neden olabilir. Aşağıdaki grafik, farklı yakıt bileşiklerindeki farklı sıcaklık gradyanlarını göstermektedir. Bu yakıtlar için ısıl güç yoğunluğu aynıdır ve tüm peletlerin çapı aynıdır.
Cam seramik sır için renk
Uranyum oksit (uranyum), II. Dünya Savaşı'ndan önce cam ve seramikleri renklendirmek için kullanıldı ve radyoaktivite uygulamaları keşfedilene kadar ana kullanımı buydu. 1958'de hem ABD hem de Avrupa'daki ordu, tükenmiş uranyum olarak ticari kullanımına yeniden izin verdi ve kullanımı daha sınırlı bir ölçekte yeniden başladı. Urania bazlı seramik sırlar, indirgemede pişirildiğinde veya UO 2 kullanıldığında koyu yeşil veya siyahtır ; daha yaygın olarak parlak sarı, turuncu ve kırmızı sırlar üretmek için oksidasyonda kullanılır. Turuncu renkli Fiestaware , uranyum renkli sırlı bir ürünün iyi bilinen bir örneğidir. Uranyum camı soluk yeşil ila sarı renktedir ve genellikle güçlü floresan özelliklere sahiptir. Urania, emaye ve porselen formülasyonlarında da kullanılmıştır . 1958'den önce üretilmiş bir sır veya camın uranyum içerip içermediğini bir Geiger sayacıyla belirlemek mümkündür .
Diğer kullanım
Radyasyonun zararlılığının farkına varılmadan önce, hafif floresansı takma dişlerin çeşitli aydınlatma koşullarında gerçek dişler gibi görünmesini sağladığı için uranyum takma dişlere ve takma dişlere dahil edildi.
Tükenmiş UO 2 (DUO 2 ) radyasyon kalkanı için bir malzeme olarak kullanılabilir . Örneğin, DUCRETE , çakılın uranyum dioksit agrega ile değiştirildiği "ağır beton " bir malzemedir ; bu malzeme kullanım için incelenmiştir fıçıları için radyoaktif atık . Tahta da DUO yapılabilir 2 - çelik sermet , bir kompozit malzemeden bir imal agrega radyasyon koruma olarak hizmet uranyum dioksit , grafit ve / veya silisyum karbür olarak hizmet nötron radyasyonu yüksek termal ortam olarak tutucu ve moderatör ve çelik iletkenlik, bozunma ısısının kolayca uzaklaştırılmasını sağlar.
Tükenmiş uranyum dioksit de bir şekilde kullanılabilir katalizör degradasyonu için, örneğin, uçucu organik bileşikler , gaz fazında, oksidasyon bölgesinin metan için metanol ve çıkarılması sülfür arasından petrol . Ticari bazılarıyla karşılaştırıldığında VOC yok etmek için kullanılan yüksek verimlilik ve uzun süreli kararlılığını katalizörler gibi değerli metaller , TiO 2 ve Co 3 O 4 katalizörler. Bu alanda pek çok araştırma yapılmakta olup, düşük radyoaktivitesi nedeniyle uranyum bileşeni için DU tercih edilmektedir.
Uranyum dioksitin şarj edilebilir piller için bir malzeme olarak kullanımı araştırılmaktadır. Piller yüksek güç yoğunluğuna ve hücre başına 4,7 V potansiyele sahip olabilir . Araştırılan başka bir uygulama, UO 2'nin bir fotoanot olarak kullanıldığı güneş destekli hidrojen üretimi için fotoelektrokimyasal hücrelerdedir . Daha önceki zamanlarda, uranyum dioksit, yarı iletken özelliklerinin ilk kullanımı olan akım sınırlaması (URDOX-direnci) için ısı iletkeni olarak da kullanılıyordu.
Uranyum dioksit ayrıca 30 kelvin'in altındaki kriyojenik sıcaklıklarda gözlemlenen antiferromanyetik durumda bilinen en güçlü piezomanyetiktir . UO 2 , uygulanan manyetik alanın işaretiyle işaret değiştiren doğrusal bir manyetostriksiyon ve 180.000 Oe'ye yakın manyetik alanlarda manyetoelastik bellek geçişi gösterir.
yarı iletken özellikleri
Bant boşluk uranyum dioksit kişilerce karşılaştırılabilir silikon ve galyum arsenit çok verimli için olası kullanımını öneren, güneş radyasyonunun emilmesi için bir bant boşluk eğrisi karşı etkinlik için optimuma yakın güneş hücreleri göre Schottky diyodu yapısı; ayrıca kızılötesi de dahil olmak üzere beş farklı dalga boyunda soğurur ve verimliliğini daha da artırır. Oda sıcaklığında içsel iletkenliği, tek kristal silikon ile yaklaşık olarak aynıdır .
Dielektrik sabiti uranyum dioksit neredeyse iki kat silikon (11.2) ve GaAs (14.1) arasında gibi yüksek olan, 22 ile ilgilidir. Bu, entegre devrelerin yapımında Si ve GaAs'a göre bir avantajdır , çünkü daha yüksek arıza gerilimleri ile daha yüksek yoğunluklu entegrasyona ve CMOS tünelleme arızasına karşı daha düşük hassasiyete izin verebilir .
Seebeck katsayısı , oda sıcaklığında uranyum dioksit olan yaklaşık 750 uV / K, 270 uV / arasında K önemli ölçüde daha yüksek bir değer talyum, kalay tellür (Tl 2 SNTE 5 ) ve talyum germanyum tellür (Tl 2 Gete 5 ) ve bizmut - tellür alaşımları, termoelektrik enerji üretimi uygulamaları için umut vaat eden diğer malzemeler ve Peltier elementleri .
Radyoaktif bozunma etkisi 235 U ve 238 onun yarı iletken özelliklerine U bu izotopların yavaş çürüme oranına 2005. Due olarak ölçülen değildi, anlamlı uranyum dioksit güneş pilleri ve termoelektrik cihazların özelliklerini etkileyen, ancak olmamalıdır VLSI çipleri için önemli bir faktör olabilir . Kullanımı tükenmiş uranyum oksit bu nedenle gereklidir. Radyoaktif bozunma sırasında yayılan alfa parçacıklarının kristal kafeste helyum atomları olarak yakalanması da özelliklerinde kademeli uzun vadeli değişikliklere neden olabilir.
Stoikiometri malzemesinin önemli ölçüde elektrik özelliklerini etkiler. Örneğin, UO elektriksel iletkenliği 1.994 olan büyüklüklerdir UO iletkenliğinden daha yüksek sıcaklıklarda daha düşük olan 2.001 .
Uranyum dioksit, U 3 O 8 gibi , yüksek sıcaklıklara dayanabilen seramik bir malzemedir (silikon veya GaAs için en fazla 200 °C'ye kıyasla yaklaşık 2300 °C), bu da onu termofotovoltaik cihazlar gibi yüksek sıcaklık uygulamaları için uygun hale getirir.
Uranyum dioksit ayrıca radyasyon hasarına karşı dirençlidir , bu da onu özel askeri ve havacılık uygulamaları için rad-hard cihazlar için faydalı kılar .
Bir diyodu arasında U 3 O 8 ve PNP transistor UO 2 başarılı bir şekilde laboratuarda üretilmiştir.
toksisite
Uranyum dioksitin akciğerlerde fagositoz tarafından emildiği bilinmektedir .
Ayrıca bakınız
Referanslar
daha fazla okuma
- Barrett, SA; Jacobson, AJ; Tofield, M.Ö.; Çamurluk, BEF (1982). "Baryum uranyum oksit BaUO3+x'in hazırlanması ve yapısı". Acta Crystallographica Bölüm B . 38 (11): 2775. doi : 10.1107/S0567740882009935 .
Dış bağlantılar
- Uranyum oksitlerin yarı iletken özellikleri
- Uranyum Dioksit için Ücretsiz Sözlük Listesi
- Uranyum dioksit Uluslararası Bio-Analitik Industries, Inc.








