miyoglobin - Myoglobin
Miyoglobin (sembol Mb veya MB ), genel olarak omurgalıların kalp ve iskelet kası dokusunda ve hemen hemen tüm memelilerde bulunan demir ve oksijen bağlayıcı bir proteindir . Miyoglobin, hemoglobin ile uzaktan ilişkilidir . Hemoglobine kıyasla , miyoglobinin oksijen için daha yüksek bir afinitesi vardır ve hemoglobinin yaptığı gibi oksijenle işbirliğine dayalı bağlanma yoktur. İnsanlarda, miyoglobin sadece kas yaralanmasından sonra kan dolaşımında bulunur .
Kas hücrelerindeki yüksek miyoglobin konsantrasyonları, organizmaların nefeslerini daha uzun süre tutmalarını sağlar. Balinalar ve foklar gibi dalış yapan memeliler, özellikle yüksek miktarda miyoglobin içeren kaslara sahiptir. Miyoglobin Tip I kas, Tip II A ve Tip II B'de bulunur, ancak çoğu metin miyoglobinin düz kasta bulunmadığını düşünür .
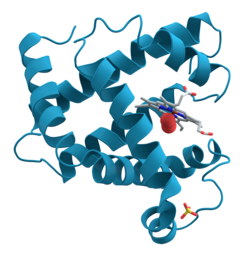
Miyoglobin, X-ışını kristalografisi ile üç boyutlu yapısını ortaya çıkaran ilk proteindi . Bu başarı 1958'de John Kendrew ve ortakları tarafından rapor edildi . Bu keşif için Kendrew, 1962 Nobel Kimya Ödülü'nü Max Perutz ile paylaştı . Biyolojide en çok çalışılan proteinlerden biri olmasına rağmen, fizyolojik işlevi henüz kesin olarak belirlenmemiştir: genetik olarak miyoglobinden yoksun olacak şekilde tasarlanmış fareler yaşayabilir ve verimli olabilir, ancak kaybın üstesinden gelmek için birçok hücresel ve fizyolojik adaptasyon gösterir. Miyoglobin eksikliği olan farelerde bu değişiklikleri gözlemleyerek, miyoglobin fonksiyonunun kaslara artan oksijen taşınması ve oksijen depolanması ile ilgili olduğu varsayılır; aynı zamanda, reaktif oksijen türlerinin bir temizleyicisi olarak da hizmet eder .
İnsanlarda miyoglobin, MB geni tarafından kodlanır .
Miyoglobin, oksihemoglobin (HbO 2 ), karboksihemoglobin (HbCO) ve methemoglobin (met-Hb) biçimlerini alan hemoglobine benzer şekilde oksimiyoglobin (MbO 2 ), karboksimiyoglobin (MbCO) ve metmiyoglobin (met-Mb) biçimlerini alabilir .
Hemoglobinden farklılıklar
Hemoglobin gibi, miyoglobin de bir hem grubu üzerinde oksijeni bağlayan sitoplazmik bir proteindir . Sadece bir globulin grubu içerirken, hemoglobinde dört tane bulunur. Hem grubu Hb'dekilerle aynı olmasına rağmen, Mb'nin oksijene afinitesi hemoglobinden daha yüksektir. Bu farklılık onun farklı rolüyle ilgilidir: hemoglobin oksijeni taşırken, miyoglobinin işlevi oksijen depolamaktır.
mutfaktaki rolü
Miyoglobin, kırmızı etin renginden sorumlu pigmentler olan hemes içerir . Etin aldığı renk kısmen miyoglobinin oksidasyon derecesi ile belirlenir. Taze ette demir atomu, bir oksijen molekülüne (O 2 ) bağlı demirli (+2) oksidasyon durumundadır . İyi pişmiş et kahverengidir çünkü demir atomu artık bir elektron kaybetmiş ferrik (+3) oksidasyon durumundadır. Et nitritlere maruz kalmışsa , demir atomu NO'ya, nitrik okside (örneğin konserve sığır eti veya kurutulmuş jambon için geçerlidir ) bağlı olduğu için pembe kalacaktır . Izgara etler ayrıca karbon monoksite bağlanan heme merkezinden gelen kırmızımsı pembe bir "duman halkası" alabilir . Karbon monoksit atmosferinde paketlenmiş çiğ et de aynı prensiplerden dolayı aynı pembe "duman halkasını" gösterir. Özellikle, bu çiğ etin yüzeyi, tüketicilerin zihninde genellikle taze et ile ilişkilendirilen pembe rengi de gösterir. Bu yapay olarak indüklenen pembe rengin bir yıla kadar sürebildiği bildiriliyor. Hormel ve Cargill'in (ABD'deki et işleme şirketleri) her ikisinin de bu et paketleme sürecini kullandığı bildiriliyor ve bu şekilde işlenen et, 2003'ten beri tüketici pazarında.
Hastalıktaki rolü
Miyoglobin, çok yüksek konsantrasyonlarda miyoglobin içeren hasarlı kas dokusundan ( rabdomiyoliz ) salınır . Salınan miyoglobin böbrekler tarafından süzülür ancak renal tübüler epitel için toksiktir ve bu nedenle akut böbrek hasarına neden olabilir . Toksik olan miyoglobinin kendisi değil (bir protoksindir ) fakat asidik ortamlarda (örneğin asidik idrar, lizozomlar ) miyoglobinden ayrılan ferrihemat kısmıdır .
Miyoglobin, kas yaralanması için hassas bir belirteçtir ve göğüs ağrısı olan hastalarda kalp krizi için potansiyel bir belirteçtir . Ancak, yükselmiş miyoglobinin akut miyokard enfarktüsü (AMI) için düşük özgüllüğü vardır ve bu nedenle tanı koymak için CK-MB , kardiyak troponin , EKG ve klinik belirtiler dikkate alınmalıdır.
Yapı ve yapıştırma
Miyoglobin , proteinlerin globin süper ailesine aittir ve diğer globinlerde olduğu gibi, halkalarla birbirine bağlanan sekiz alfa sarmaldan oluşur . Miyoglobin 153 amino asit içerir.
Miyoglobin , merkezinde demir bulunan bir porfirin halkası içerir . Bir proksimal histidin grubu (His-93) doğrudan demire bağlanır ve bir distal histidin grubu (His-64) karşı yüzün yakınında gezinir. Distal imidazol demire bağlanmış, ancak substrat olarak O ile etkileşim mevcuttur değildir 2 . Bu etkileşim, O bağlanmasını teşvik 2 , ancak karbon monoksit (CO), yine de burada daha güçlü olarak O fazla bağlandığı x yaklaşık 240 2 .
O bağlanmasını 2 nedenleri N4 cep merkezine yarıçapı ve hamlede küçülür Fe merkezinde önemli bir yapı değişikliği,. O 2 -bağlayıcı indükler "eğirme-eşleştirme": demir deoksi formu beş koordinat yüksek sıkma ve altı oksi bir şekilde düşük bir dönme ve koordinat diyamanyetik .
sentetik analoglar
Birçok miyoglobin modeli, geçiş metali dioksijen komplekslerine olan geniş ilginin bir parçası olarak sentezlenmiştir . İyi bilinen bir örnek, tetrafenilporfirinin sterik olarak hacimli bir türevinin bir demirli kompleksinden oluşan çitli porfirindir . Bir varlığında imidazol ligand, bu demir kompleksi tersinir olarak O bağlanan 2 . O 2 alt-tabaka demir merkezi altıncı konum işgal, bükülmüş bir geometriye benimser. Bu modelin önemli bir özelliği, aktif olmayan bir diferrik durum olan μ-oxo dimerin yavaş oluşumudur. Doğada, bu tür deaktivasyon yolları, Fe-porfirin düzeneklerinin yakın yaklaşımını önleyen protein matrisi tarafından bastırılır.
 Metilimidazol (yeşil) ve dioksijen tarafından işgal edilen eksenel koordinasyon bölgelerine sahip Fe'nin bir çitli porfirin kompleksi . R grupları O kuşatan 2 bağlama sahası.
Metilimidazol (yeşil) ve dioksijen tarafından işgal edilen eksenel koordinasyon bölgelerine sahip Fe'nin bir çitli porfirin kompleksi . R grupları O kuşatan 2 bağlama sahası.
Ayrıca bakınız
- sitoglobin
- Hemoglobin
- hemoprotein
- nöroglobin
- fitoglobin
- Miyoglobinüri - İdrarda miyoglobin varlığı
- Apendiküler kas-iskelet sisteminin iskemi-reperfüzyon hasarı
Referanslar
daha fazla okuma
- Collman JP, Boulatov R, Sunderland CJ, Fu L (Şubat 2004). "Sitokrom c oksidaz, miyoglobin ve hemoglobinin fonksiyonel analogları". Kimyasal İncelemeler . 104 (2): 561–88. doi : 10.1021/cr0206059 . PMID 14871135 .
- Reeder BJ, Svistunenko DA, Cooper CE, Wilson MT (Aralık 2004). "Miyoglobin ve hemoglobinin radikal ve redoks kimyası: in vitro çalışmalardan insan patolojisine". Antioksidanlar ve Redoks Sinyali . 6 (6): 954–66. doi : 10.1089/ars.2004.6.954 . PMID 15548893 .
- Schlieper G, Kim JH, Molojavyi A, Jacoby C, Laussmann T, Flögel U, Gödecke A, Schrader J (Nisan 2004). "Miyoglobin nakavt farenin hipoksik strese uyarlanması" . Amerikan Fizyoloji Dergisi. Düzenleyici, Bütünleştirici ve Karşılaştırmalı Fizyoloji . 286 (4): R786-92. doi : 10.1152/ajpregu.00043.2003 . PMID 14656764 . S2CID 24831969 .
- Takano T (Mart 1977). "2-0 A çözünürlükte rafine miyoglobinin yapısı. II. Sperm balinasından deoksimiyoglobinin yapısı". Moleküler Biyoloji Dergisi . 110 (3): 569-84. doi : 10.1016/S0022-2836(77)80112-5 . PMID 845960 .
- Roy A, Sen S, Chakraborti AS (Şubat 2004). "İn vitro enzimatik olmayan glikasyon, oksidatif stres kaynağı olarak miyoglobinin rolünü arttırır". Serbest Radikal Araştırma . 38 (2): 139-46. doi : 10.1080/10715160310001638038 . PMID 15104207 . S2CID 11631439 .
- Stewart JM, Blakely JA, Karpowicz PA, Kalanxhi E, Thatcher BJ, Martin BM (Mart 2004). "Olağandışı zayıf oksijen bağlama, fiziksel özellikler, kısmi dizi, otoksidasyon oranı ve beluga balina (Delphinapterus leucas) miyoglobin potansiyel bir fosforilasyon sitesi". Karşılaştırmalı Biyokimya ve Fizyoloji B . 137 (3): 401–12. doi : 10.1016/j.cbpc.2004.01.007 . PMID 15050527 .
- Wu G, Wainwright LM, Poole RK (2003). Mikrobiyal globinler . Mikrobiyal Fizyolojideki Gelişmeler. 47 . s. 255–310. doi : 10.1016/S0065-2911(03)47005-7 . ISBN'si 9780120277476. PMID 14560666 .
- Mirceta S, Signore AV, Burns JM, Cossins AR, Campbell KL, Berenbrink M (Haz 2013). "Miyoglobin net yüzey yükü tarafından izlenen memeli dalış kapasitesinin evrimi" . Bilim . 340 (6138): 1234192. doi : 10.1126/science.1234192 . PMID 23766330 . S2CID 9644255 .. Ayrıca bu bulguyla ilgili Proteopedia makalesine bakın.
Dış bağlantılar
- İnsanda Çevrimiçi Mendel Kalıtımı (OMIM): 160000 insan genetiği
- Miyoglobin Proteini
- RCSB PDB özellikli molekül
- "Hangi Kesim Daha Yaşlı? (Bu Bir Hile Sorusu)" , The New York Times , 21 Şubat 2006 tarihli et endüstrisinde etin kırmızı görünmesini sağlamak için karbon monoksit kullanımına ilişkin makale.
- "Mağazalar Et Raporlarına Tepki Veriyor" , The New York Times , 1 Mart 2006'da etin taze görünmesi için karbon monoksit kullanımına ilişkin makale.
- Uygun yapısal bilginin her genel PDB için Uniprot : P02144 de (İnsan miyoglobin) PDBe-KB .