Vinpocetine - Vinpocetine
 | |
 | |
| Klinik veriler | |
|---|---|
| AHFS / Drugs.com | Uluslararası İlaç İsimleri |
| Hamilelik kategorisi |
|
Yönetim yolları |
Ağızdan, damardan |
| ATC kodu | |
| Hukuki durum | |
| Hukuki durum | |
| Farmakokinetik veriler | |
| biyoyararlanım | 56,6 +/- %8,9 |
| Metabolizma | karaciğer |
| Eliminasyon yarı ömrü | 2.54 +/- 0.48 saat |
| Boşaltım | böbrek |
| tanımlayıcılar | |
| |
| CAS numarası | |
| PubChem Müşteri Kimliği | |
| IUPHAR/BPS | |
| Kimyasal Örümcek | |
| ÜNİİ | |
| fıçı | |
| CHEMBL | |
| CompTox Panosu ( EPA ) | |
| ECHA Bilgi Kartı |
100.050.917 |
| Kimyasal ve fiziksel veriler | |
| formül | C 22 H 26 N 2 O 2 |
| Molar kütle | 350,462 g·mol -1 |
| 3B model ( JSmol ) | |
| |
| |
|
| |
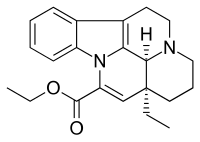
Vinpocetine ( etil apovincaminate ) sentetik bir türev arasında vinka alkaloidi vinkamin . Vincamin, Voacanga africana'nın tohumlarından veya Vinca minör (küçük deniz salyangozu) yapraklarından çıkarılır .
Tıbbi kullanımlar
Vinpocetine, birçok Asya ve Avrupa ülkesinde inme ve bunama gibi serebrovasküler bozuklukların tedavisi için otuz yılı aşkın bir süredir kullanılmaktadır. Vinpocetine, Amerika Birleşik Devletleri'nde herhangi bir terapötik kullanım için onaylanmamıştır.
FDA nedeniyle sentetik doğası ve önerilen terapötik kullanımları, yani Vinpocetine kararına vardı olarak pazarlanacak men edilmesi besin takviyesi altında Federal Gıda, İlaç ve Kozmetik Yasası . Buna rağmen, vinpocetine, genellikle nootropik olarak pazarlanan diyet takviyelerinde yaygın olarak bulunur .
Vinpocetine'in ek olarak satışı, "potansiyel zararlı nootropik özellikler" nedeniyle Avustralya ve Yeni Zelanda'da yasaklanmıştır. Vinpocetine Kanada'da yasal olarak satılmaktadır. Daha fazla ayrıntı için Health Canada web sitesine bakın. Vinpocetine ne demansta ne de felçte bir faydayı tam olarak desteklemez . 2003 itibariyle, üç kontrollü klinik çalışma "hafıza sorunları olan yaşlı yetişkinleri" test etti.
Vinpocetine, Health Canada tarafından aşağıdaki önerilen kullanımlar için ek olarak satılmak üzere lisanslanmıştır: "yaşa bağlı bilişsel gerileme olanlarda bilişsel işlevi geliştirmeye yardımcı olmak için" [1] ve "hafıza ve bilişi geliştirmek için" [2] (diğer kimyasallara ve/veya bitkilere ek olarak alındığında diğer amaçlara/kullanımlara ek olarak).
Yan etkiler
Hamilelik sırasında kullanılması bebeğe zarar verebilir veya düşükle sonuçlanabilir .
Vinpocetine'in yan etkileri arasında kızarma, mide bulantısı, baş dönmesi, ağız kuruluğu, geçici hipo ve hipertansiyon, baş ağrıları, mide ekşimesi ve düşük kan basıncı bulunur. FDA, 2019'da "vinpocetine'in düşüklere neden olabileceği veya fetal gelişime zarar verebileceği" konusunda uyarıda bulunan bir bildiri yayınladı. Vinpocetine, bir vakada, granülositlerin belirgin şekilde azaldığı ciddi bir durum olan agranülositozun indüklenmesiyle ilişkilendirilmiştir . Bazı insanlar, sürekli vinpocetine kullanımının bağışıklık fonksiyonunu azalttığını anekdot olarak kaydetmiştir. Komisyon E , vinpocetine ile azaltılmış bağışıklık fonksiyonunun uzun vadede apoptoza (hücresel ölüm) neden olabileceği konusunda uyardı .
Hareket mekanizması
Vinpocetine'in etki mekanizmasının üç potansiyel etki içerdiği varsayılmıştır: sodyum kanallarının tıkanması , hücresel kalsiyum akışının azalması ve antioksidan aktivite. Çalışmalar ayrıca vinpocetine'in izole tavşan aortunda PDE-1'i inhibe edebileceğini ileri sürmüştür ; engelleme , IKK , in vitro önlenmesi, IKB bozulması ve aşağıdaki translokasyonu NF-KB hücre çekirdeğine; ve sıçanların izole striatal sinir uçlarında dopaminin metabolik bir parçalanma ürünü olan DOPAC'ı arttırır .
Diyet takviyesi
Vinpocetine'in ABD'de diyet takviyelerine dahil edilmesi, tanımlanmış dozaj parametrelerinin olmaması, kanıtlanmamış kısa ve uzun vadeli faydaları ve insan sağlığına yönelik riskleri nedeniyle inceleme altına alındı. ABD'de, vinpocetine takviyeleri spor takviyeleri, beyin geliştiriciler ve kilo kaybı takviyeleri olarak pazarlanmaktadır.
GNC ve Vitamin Shoppe perakende mağazalarında satılan 23 marka vinpocetine diyet takviyesinin 2015 analizi, yaygın etiketleme hataları bildirdi. 23 ek etiketten sadece 6'sı (%26) tüketicilere doğru dozlarda vinpocetin sağladı (önerilen günlük porsiyon başına 0,3 ila 32 mg arasında değişirken), 23'ten 6'sı (%26) etiketlerine rağmen hiç vinpocetin içermiyordu. madde onların içindeydi. Toplamda, test edilen 23 ürünün 9'u yanlış etiketlenmiş ve 23 ürünün 17'si (%74) vinpocetine miktarı hakkında herhangi bir bilgi sağlamamıştır.
Çalışmada yanıt olarak, o zaman Senatör Claire McCaskill , zaman üst olarak görev yaparken Demokrat üzerinde Yaşlanma üzerine Senato Özel Komitesi vinposetindir takviyelerinin satışını askıya FDA çağırdı ve gönüllü durdurma vinposetindir ürünleri satan 10 perakendecilerin istedi. McCaskill, "Bu takviyeleri düzenleme şeklimiz işe yaramıyor - ve tüketicilerin hayatlarını ve refahını riske atıyor. Sahte etiketler, kusurlu içerik maddeleri, çılgınca yasa dışı iddialar ve şimdi içeren ürünler gördük. diğer ülkelerde reçeteli ilaçlar olarak sınıflandırılan sentezlenmiş bileşenler."
ABD'de satılan sekiz marka vinpocetin takviyesinin 2016 analizi, içerdiği vinpocetin miktarının, porsiyon başına 0,6 ila 5,1 mg arasında oldukça değişken olduğunu ve ürün etiketlerinin çoğunun vinpocetin miktarı hakkında hiçbir bilgi sağlamadığını buldu. Test edilen ürünlerden sadece biri etikette belirtilen vinpocetine miktarını içeriyordu (porsiyon başına 1.070 mg). Çalışmanın yazarları, ürünlerdeki vinpocetine miktarlarıyla ilgili uygun etiketleme eksikliğinin tüketiciler için olumsuz etki riski oluşturabileceğini kaydetti.
davalar
Procera AVH, huperzin A ve asetil-l-karnitin ile kombinasyon halinde açıklanmayan miktarlarda vinpocetin içeren bir besin takviyesidir . 2012 yılında, üretici Brain Research Labs (BRL), şirketin Procera AVH'yi Tüketici Sahtekarlığı Yasası'nı ihlal ederek beyin işlevini iyileştirme yeteneğine sahip olarak yanlış bir şekilde pazarladığını iddia eden bir toplu davayı çözmek için 500.000 $ ödemeyi kabul etti.
Temmuz 2015'te ABD Federal Ticaret Komisyonu (FTC), ürünü hafıza kaybı ve bilişsel gerilemeye "çözüm" olarak tanıtan Procera AVH için pazarlama iddialarının yanlış, yanıltıcı, asılsız ve FTC Yasasını ihlal ettiğine karar verdi. . BRL ve bağlı şirketleri, Brain Power Partners, Brain Power Founders ve MedHealth Direct (tümü Laguna Beach, California'da yerleşiktir ) 91 milyon dolar para cezasına çarptırıldı. 2012 yılında BRL'yi satın alan Tampa, Florida merkezli KeyView Labs, 61 milyon dolar para cezasına çarptırıldı. FTC şikayetinde ayrıca BRL'nin kurucusu ve baş bilim yetkilisi George Reynolds (aka Josh Reynolds) ve MedHealth'in tek yetkilisi ve çalışanı John Arnold da yer aldı. FTC şikayeti, Reynolds'ı Procera AVH için aldatıcı uzman onayları yapmakla suçladı. Davadaki sanıklar nihayetinde FTC ve California kolluk kuvvetleri tarafından getirilen aldatıcı reklam iddialarını çözmek için 1,4 milyon dolar ödemeyi kabul etti. Ayrıca, kalıcı bir ihtiyati tedbir, sanıkların gelecekte Procera AVH hakkında benzer aldatıcı iddialarda bulunmalarını ve herhangi bir bilimsel çalışmanın varlığını, sonuçlarını veya sonuçlarını yanlış beyan etmelerini engelledi.
