Tioredoksin redüktaz - Thioredoxin reductase
| tioredoksin redüktaz | |
|---|---|
| tanımlayıcılar | |
| Sembol | ? |
| InterPro | IPR005982 |
| PROZİT | PS00573 |
| SCOP2 | 1zof / KAPSAM / SUPFAM |
Tioredoksin redüktazlar ( TR , TrxR ) ( EC 1.8.1.9 ), tioredoksin (Trx) indirgediği bilinen tek enzimdir . Tioredoksin redüktazın iki sınıfı tanımlanmıştır: bakterilerde ve bazı ökaryotlarda bir sınıf ve hayvanlarda bir sınıf. Bakterilerde TrxR, NrdH olarak bilinen glutaredoksin benzeri proteinlerin indirgenmesini de katalize eder. Her iki sınıf da homodimer olarak işlev gören flavoproteinlerdir . Her monomer, bir FAD prostetik grubu, bir NADPH bağlanma alanı ve redoks-aktif disülfid bağı içeren bir aktif bölge içerir .
Hücresel rol
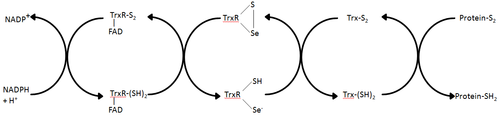
Tioredoksin redüktaz, tioredoksinin indirgenmesini katalize ettiği bilinen tek enzimdir ve bu nedenle tioredoksin sisteminde merkezi bir bileşendir. Tioredoksin (Trx) ve NADPH ile birlikte bu sistemin en genel tanımı hücrelerde indirgenmiş disülfid bağları oluşturma yöntemidir. Elektronlar NADPH'den TrxR yoluyla alınır ve protein disülfidleri veya diğer substratları indirgeyen Trx'in aktif bölgesine aktarılır. Trx sistemi tüm canlı hücrelerde bulunur ve genetik bir materyal olarak DNA'ya, oksijen metabolizmasından kaynaklanan oksidatif hasara karşı savunmaya ve hidrojen peroksit ve nitrik oksit gibi molekülleri kullanarak redoks sinyaline bağlı evrimsel bir geçmişe sahiptir.
Çeşitlilik
Tioredoksin redüktazın iki sınıfı bağımsız olarak evrimleşmiştir:
- Aktif bölgesinde bir selenosistein kalıntısı içeren yüksek moleküler ağırlıklı (MW = ~55,000) tip, insanlar dahil daha yüksek ökaryotlarda tanımlanmıştır. Bu TxR glutatyon redüktaz , tripanotion redüktaz , cıva redüktaz ve lipoamid dehidrojenaz ile ilgilidir .
- Arke, bakteri ve diğer ökaryalarda düşük moleküler ağırlıklı (MW = ~ 35.000) bir tip tespit edilmiştir.
Bu iki TrxR sınıfı, güvenilir bir şekilde hizalanabilecekleri birincil dizi bölümünde yalnızca ~%20 dizi özdeşliğine sahiptir. Her iki TrxR sınıfının net reaksiyonu aynıdır ancak her birinin etki mekanizması farklıdır.
İnsanlar üç tioredoksin redüktaz izozimini ifade eder: tioredoksin redüktaz 1 (TrxR1, sitozolik), tioredoksin redüktaz 2 (TrxR2, mitokondriyal), tioredoksin redüktaz 3 (TrxR3, testise özgü). Her izozim ayrı bir gen tarafından kodlanır:
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Yapı
E. koli
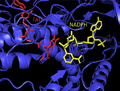
Olarak , E. coli ThxR iki bağlanma alanları, için bir tane FAD ve başka NADPH . Bu iki alan arasındaki bağlantı, iki iplikli bir anti-paralel β-tabakadır . Her alan ayrı ayrı glutatyon redüktaz ve lipoamid dehidrojenazdaki benzer alanlara çok benzer , ancak bu alanların ThxR'deki nispi yönelimi 66 derece döndürülür. Bu, aşağıda açıklanan enzim etki mekanizmasında önemli hale gelir. ThxR, üç alfa-helis ve iki döngü tarafından oluşturulan iki monomer arasındaki arayüz ile homo-dimerize olur . Her monomer, bir tioredoksin molekülünü ayrı ayrı bağlayabilir .
Memeli
Memeli TrxR yapısı E. coli'ye benzer . Bir FAD ve NADPH bağlanma alanı ve iki monomer alt birimi arasında bir arayüz içerir. Memeli ThxR'de, küçük bir çift beta zinciri oluşturan iki alfa sarmalı arasında FAD bağlanma alanında bir ekleme vardır . Enzimdeki aktif disülfid bu sarmallardan biri üzerinde yer alır ve bu nedenle aktif disülfid bağı E. coli ve diğer prokaryotlarda olduğu gibi NADPH alanında değil FAD alanında bulunur .
mekanizma
E. koli
Olarak , E. coli ThxR FAD ve NADPH etki uzamsal konumlandırılmasının FAD ve NADPH redoks-aktif halkaları birbirine yakın olmadığı şekildedir. E. coli'nin FAD alanı , NADPH alanı sabit kalırken 66 derece döndürüldüğünde, iki prostetik grup, elektronların NADPH'den FAD'ye ve ardından aktif bölge disülfid bağına geçmesine izin vererek yakın temasa geçer. E. coli'de korunan aktif site kalıntıları -Cys-Ala-Thr-Cys-'dir.
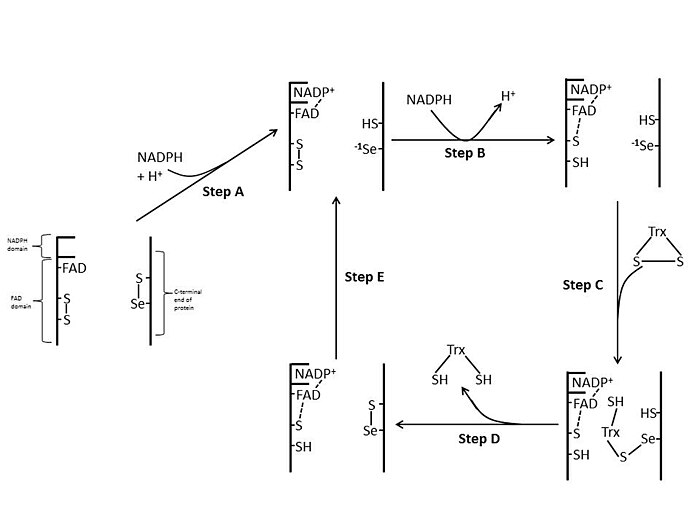
Memeli
Memeli TrxR'leri glutatyon redüktaz ile E. coli'den çok daha yüksek bir dizi homolojisine sahiptir . FAD alanındaki ve bağlı NADPH alanındaki aktif bölge Cys kalıntıları, E. coli'de bulunan elektron transferi için 66 derecelik bir dönüş gerekliliğini ortadan kaldırmaktadır . Memeli mekanizmasının ek bir özelliği, proteinin C-terminal ucunda katalitik aktivite için gerekli olan bir selenosistein kalıntısının varlığıdır. Memeli aktif bölgesindeki korunan kalıntılar -Cys-Val-Asn-Val-Gly-Cys-.
Algılama yöntemleri
Tioredoksin redüktaz, Ellman reaktifi kullanılarak DTNB tahlili gibi çeşitli yöntemlerle ölçülebilir . Disülfid bazlı TRFS serisi floresan problar, TrxR'nin seçici tespitini göstermiştir. Mafireyi, TrxR tespitinde uygulanan ilk diselenid probunu sentezledi. Diğer saptama yöntemleri arasında immünolojik teknikler ve selenosistin-tioredoksin redüktaz tahlili (SC-TR tahlili) yer alır.
Klinik önemi
Kanser tedavisi
Bu enzimin aktivitesi hücre büyümesi ve hayatta kalması için gerekli olduğundan, anti-tümör tedavisi için iyi bir hedeftir. Ayrıca, enzim, malign mezotelyoma dahil olmak üzere çeşitli kanser türlerinde yukarı doğru düzenlenir . Örneğin, moteksafin gadolinyum (MGd), tümör hücrelerini seçici olarak hedef alan, tioredoksin redüktaz ve ribonükleotit redüktazın inhibisyonu yoluyla hücre ölümüne ve apoptoza yol açan yeni bir kemoterapötik ajandır .
kardiyomiyopati
Dilate kardiyomiyopati ( DCM ), konjestif kalp yetmezliği vakalarında yaygın bir tanıdır . Tioredoksin redüktazlar, hücresel redoks dengesini düzenlemek ve mitokondride oksidatif fosforilasyon yoluyla üretilen reaktif oksijen türlerinin neden olduğu hasarı azaltmak için gerekli proteinlerdir . Farelerde mitokondriyal TrxR2'nin etkisizleştirilmesi, ventriküler kalp duvarlarının incelmesi ve yenidoğan ölümü ile sonuçlanır. Ayrıca, bir kontrol popülasyonunda değil, DCM tanısı konan hastalarda TrxR2 geninde iki mutasyon bulunur. Bu mutasyonların patolojik etkisinin, kardiyak miyositlerde oksidatif hasarı kontrol etme yeteneğinin bozulması olduğu varsayılmaktadır .
Antibiyotik
Son zamanlarda düşük moleküler ağırlıklı tioredoksin redüktazın yeni antibiyotikler (auranofin veya Ebselen gibi) için bir hedef olabileceğini gösteren bazı araştırmalar yapılmıştır. Bu özellikle Mycobacterium Haemophilum için geçerlidir ve antibiyotiğe dirençli bakteriler için kullanılabilir.
Referanslar
Dış bağlantılar
- ABD Ulusal Tıp Kütüphanesi Tıbbi Konu Başlıklarında (MeSH) Tioredoksin+Redüktaz+(NADPH )