Sülfür tetraflorür - Sulfur tetrafluoride

|
|||
|
|
|||
| İsimler | |||
|---|---|---|---|
|
IUPAC adı
Sülfür (IV) florür
|
|||
| Diğer isimler
Kükürt tetraflorür
|
|||
| Tanımlayıcılar | |||
|
3B modeli ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA Bilgi Kartı |
100.029.103 |
||
|
PubChem Müşteri Kimliği
|
|||
| RTECS numarası | |||
| UNII | |||
| BM numarası | 2418 | ||
|
CompTox Kontrol Paneli ( EPA )
|
|||
|
|||
|
|||
| Özellikleri | |||
| SF 4 | |||
| Molar kütle | 108.07 g / mol | ||
| Görünüm | renksiz gaz | ||
| Yoğunluk | 1,95 g / cm 3 , -78 ° C | ||
| Erime noktası | -121.0 ° C | ||
| Kaynama noktası | −38 ° C | ||
| tepki | |||
| Buhar basıncı | 10,5 atm (22 ° C) | ||
| Yapısı | |||
| Tahterevalli ( C 2 v ) | |||
| 0.632 D | |||
| Tehlikeler | |||
| Ana tehlikeler | oldukça toksik aşındırıcı |
||
| Güvenlik Bilgi Formu | ICSC 1456 | ||
| NFPA 704 (ateş elması) | |||
| NIOSH (ABD sağlık maruziyet sınırları): | |||
|
PEL (İzin Verilebilir )
|
Yok | ||
|
REL (Önerilen)
|
C, 0.1 ppm (0.4 mg / m 3 ) | ||
|
IDLH (Ani tehlike)
|
ND | ||
| Bağıntılı bileşikler | |||
|
Diğer anyonlar
|
Sülfür diklorür Disülfür dibromür Sülfür triflorür |
||
|
Diğer katyonlar
|
Oksijen diflorür Selenyum tetraflorür Tellür tetraflorür |
||
|
İlgili kükürt florürler
|
Disülfür diflorür Sülfür diflorür Disülfür dekaflorür Sülfür hekzaflorür |
||
|
Bağıntılı bileşikler
|
Tiyonil florür | ||
|
Aksi belirtilmedikçe, veriler standart hallerinde (25 ° C [77 ° F], 100 kPa) malzemeler için verilmiştir. |
|||
|
|
|||
| Bilgi kutusu referansları | |||
Sülfür tetraflorür , S F 4 formülüne sahip kimyasal bileşiktir . Su veya neme maruz kaldığında tehlikeli HF açığa çıkaran renksiz bir aşındırıcı gazdır . Bu istenmeyen özelliklere rağmen, bu bileşik , bazıları farmasötik ve özel kimya endüstrilerinde önemli olan organoflorin bileşiklerinin hazırlanmasında yararlı bir reaktiftir .
Yapısı
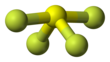
SF 4'teki kükürt formal +4 oksidasyon durumundadır . Kükürtün toplam altı değerlik elektronundan ikisi yalnız bir çift oluşturur . SF 4'ün yapısı bu nedenle VSEPR teorisinin prensipleri kullanılarak tahmin edilebilir : Merkezde S ile bir testere şeklidir . Üç ekvator pozisyonundan biri, bağlanmayan yalnız bir elektron çifti tarafından işgal edilmiştir . Sonuç olarak molekül, iki farklı F ligandı tipine sahiptir, iki eksenel ve iki ekvatoral . İlgili tahvil mesafeleri S – F ax = 164,3 pm ve S – F eq = 154,2 pm'dir. Hipervalent moleküllerdeki eksenel ligandların daha az güçlü bir şekilde bağlanması tipiktir . SF aksine 4 , ilgili molekül SF 6 6+ halde sülfür vardır, bir valans elektronları kükürt bağlayıcı olmayan kalır, bu nedenle molekülün, yüksek ölçüde simetrik oktahedral yapıya sahiptir. Bundan başka SF ile zıt 4 , SF 6 olağanüstü atıl kimyasal olup.
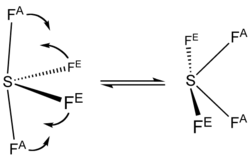
19 K NMR SF spektrumu 4 gösterir sadece bir sinyal ortaya eksenel ve hızlı le birbirlerine yoluyla ekvatoral F atomu ile pozisyonları pseudorotation .
Sentez ve üretim
SF 4 reaksiyonu ile üretilir SCL 2 ve NaF içinde asetonitril :
- 3 SCl 2 + 4 NaF → SF 4 + S 2 Cl 2 + 4 NaCl
SF 4 ayrıca yüksek sıcaklıklarda çözücü olmadan üretilir.
Alternatif olarak, yüksek verimde SF 4 , reaksiyon ortamının yokluğunda, ayrıca daha az istenen yüksek reaksiyon sıcaklıklarında (örn. 225–450 ° C) sülfür (S) , NaF ve klor (Cl 2 ) kullanılarak üretilir.
Reaksiyon ortamına gerek duymadan yüksek verimde SF 4 üretmenin düşük sıcaklıkta (örneğin 20–86 ° C) bir yöntemi klor (Cl 2 ) , S ve KF yerine brom (Br 2 ) kullanılarak gösterilmiştir :
- S + (2 + x ) Br 2 + 4 KF → SF 4 ↑ + x Br 2 + 4 KBr
Florokarbon sentezi için SF 4 kullanımı
Olarak organik sentez SF 4 CF CF içine COH ve C = O grupları dönüştürmek için kullanılan 2 sırasıyla grup. Bazı alkoller , karşılık gelen florokarbonu kolayca verir . Ketonlar ve aldehitler , geminal diflorürler verir. Karbonile alfa protonlarının varlığı, yan reaksiyonlara ve azalmış (% 30-40) verime yol açar. Ayrıca dioller olabilir vermek siklik sülfit esterleri, (RO) 2 SO. Karboksilik asitler triflorometil türevlerine dönüşür. Örneğin, heptanoik asidin 100-130 ° C'de SF 4 ile işlenmesi 1,1,1-trifloroheptan üretir. Hekzafloro-2-butin , benzer şekilde asetilendikarboksilik asitten üretilebilir . Reaksiyona girmemiş SF dahil olmak üzere bu florinleştirilmeleri gelen eş çarpımlar 4 SOF ile birlikte 2 SO 2 , toksik, ancak sulu KOH ile muamele ile nötralize edilebilir.
SF kullanılması 4 daha uygun işlenen son yıllarda yerini olan dietilaminosülfür triflorür , Et 2 NSF 3 , "DAST", Et = CH 3 CH 2 . Bu reaktif SF 4'ten hazırlanmıştır :
- SF 4 + Me 3 SiNEt 2 → Et 2 NSF 3 + Me 3 SiF
Diğer tepkiler
Sülfür klorür pentaflorür ( SF
5 SF 5 grubunun yararlı bir kaynağı olan Cl ), SF 4'ten hazırlanır .
SF 4'ün hidrolizi kükürt dioksit verir :
- SF 4 + 2 H 2 O → SO 2 + 4 HF
Bu reaksiyon aracılığı yoluyla ilerlemektedir tionil florür genellikle SF kullanımı ile karışmaz, 4 , bir reaktif olarak.
Toksisite
SF
4 ciğerlerin içinde nemle reaksiyona girerek kükürt dioksit ve hidrojen florür oluşturur :
- SF 4 + 2 H 2 O → SO 2 + 4 HF