Demir(II) klorür - Iron(II) chloride
 Susuz demir klorürün yapısı (
Fe, Cl)
|
|||
|
|||
| İsimler | |||
|---|---|---|---|
|
IUPAC adları
Demir(II) klorür
Demir diklorür |
|||
| Diğer isimler
Demir klorür
Rokühnit |
|||
| tanımlayıcılar | |||
|
3B model ( JSmol )
|
|||
| chebi | |||
| Kimyasal Örümcek | |||
| ECHA Bilgi Kartı |
100.028.949 |
||
| AT Numarası | |||
|
PubChem Müşteri Kimliği
|
|||
| RTECS numarası | |||
| ÜNİİ | |||
|
CompTox Panosu ( EPA )
|
|||
|
|||
|
|||
| Özellikleri | |||
| FeCl 2 | |||
| Molar kütle | 126.751 g/mol (susuz) 198.8102 g/mol (tetrahidrat) |
||
| Görünüm | Tan katı (susuz) Soluk yeşil katı (di-tetrahidrat) |
||
| Yoğunluk | 3.16 g / cc 3 (susuz) 2.39 g / cm ' 3 (dihidrat) 1.93 g / cm' 3 (tetrahidrat) |
||
| Erime noktası | 677 °C (1.251 °F; 950 K) (susuz) 120 °C (dihidrat) 105 °C (tetrahidrat) |
||
| Kaynama noktası | 1.023 °C (1.873 °F; 1.296 K) (susuz) | ||
| 64,4 g/100 mL (10 °C), 68,5 g/100 mL (20 °C), 105,7 g/100 mL (100 °C) |
|||
| Çözünürlük olarak THF | Çözünür | ||
| günlük P | -0,15 | ||
| +14 750 ·10 −6 cm 3 /mol | |||
| yapı | |||
| monoklinik | |||
| Fe'de oktahedral | |||
| Farmakoloji | |||
| B03AA05 ( WHO ) | |||
| Tehlikeler | |||
| Güvenlik Bilgi Formu | Demir (II) klorür MSDS | ||
| NFPA 704 (ateş elmas) | |||
| NIOSH (ABD sağlığa maruz kalma sınırları): | |||
|
REL (Önerilen)
|
TWA 1 mg / m 3 | ||
| Bağıntılı bileşikler | |||
|
Diğer anyonlar
|
Demir(II) florür Demir(II) bromür Demir(II) iyodür |
||
|
Diğer katyonlar
|
Kobalt(II) klorür Manganez(II) klorür Bakır(II) klorür |
||
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|||
|
|
|||
| Bilgi kutusu referansları | |||
(II) klorür, demir olarak da bilinen, demir klorür , bir kimyasal bileşik , formül FeC arasında 2 . Bu a, paramanyetik yüksek bir erime noktasına sahip bir katı. Bileşik beyazdır, ancak tipik örnekler genellikle kirli beyazdır. FeCl 2 , ticarette ve laboratuvarda en sık karşılaşılan form olan yeşilimsi tetrahidrat olarak sudan kristalleşir . Ayrıca bir dihidrat var. Bileşik suda oldukça çözünür ve soluk yeşil çözeltiler verir.
Üretim
Hidratlı demir klorür formları, çelik üretiminden kaynaklanan atıkların hidroklorik asit ile işlenmesiyle üretilir . Bu tür çözeltiler, özellikle hidroklorik asit tamamen tüketilmediğinde "harcanmış asit" veya "turşu likörü" olarak adlandırılır:
- Fe + 2 HCl → FeCl 2 + H 2
Harcanan asit, atılırsa işlem gerektirir. Demir klorür üretiminde demir klorür kullanılır. Hidroklorik asidi yeniden oluşturmak için demir klorür de kullanılabilir. Bazı titanyum cevherleri demir içerdiğinden , aynı zamanda titanyum üretiminin bir yan ürünüdür .
susuz FeCl 2
Demir klorür, metanol içindeki bir hidroklorik asit çözeltisine demir tozu ilave edilerek hazırlanır . Bu reaksiyon üzerine ° ile yaklaşık 160 ° C dönüştürür bir vakumda ısıtma diklorür, metanol solvatını sağlar , susuz FeC 2 . Net reaksiyon gösterilir:
- Fe + 2 HCl → FeCl 2 + H 2
FeBr 2 ve FeI 2 benzer şekilde hazırlanabilir.
Susuz demir klorür alternatif bir sentezi, azaltılmasıdır FeC 3 ile klorobenzen :
- 2 FeCl 3 + C 6 H 5 Cl → 2 FeCl 2 + C 6 H 4 Cl 2 + HCl
İki klasik sentezlere birinde ferrosen , Wilkinson FeC üretilen 2 in situ FeC arasında comproportionation ile 3 demir tozu ile tetrahidrofuran (THF). Demir klorür, yüksek sıcaklıklarda demir klorüre ayrışır.
hidratlar
Dihidrat, FeC 2 (lH 2 O) 2 , konsantre edilmiş hidroklorik asit ile kristalize edilmiştir. Dihidrat bir koordinasyon polimeridir . Her Fe merkezi, dört çift köprülü klorür ligandıyla koordine edilir . Oktahedron, bir çift karşılıklı trans aquo ligand tarafından tamamlanır .
Reaksiyonlar
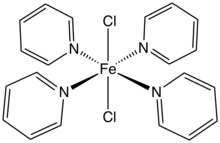
FeC 2 ve hidratları birçok ligandlarla kompleksleri oluştururlar. Örneğin, hidratlar çözeltileri iki mol eşdeğeri ile reaksiyona [(Cı- 2 , H 5 ) 4 N] CI tuzunu elde etmek üzere [(Cı- 2 , H 5 ) 4 N] 2 [FeC 4 ].
Susuz FeC 2 THF içinde çözünür olan, organometalik sentezinde standart öncüsüdür. FeCb 2 üretmek için kullanılan NHC kompleksleri için in situ çapraz birleştirme reaksiyonları .
Uygulamalar
İlgili demir sülfat ve demir klorürün aksine , demir klorürün birkaç ticari uygulaması vardır. Demir komplekslerinin laboratuvar sentezinde kullanılmasının yanı sıra, demir klorür , atık su arıtımında , özellikle kromat veya sülfür içeren atıklar için pıhtılaşma ve topaklaştırma maddesi olarak hizmet eder . Atıksu arıtımında koku kontrolü için kullanılır. Çeşitli pigmentlerde kullanılabilen çeşitli derecelerde hematit yapmak için bir öncü olarak kullanılır. Manyetik pigmentler olan hidratlı demir(III) oksitlerin öncüsüdür. FeCl 2 , organik sentezde bir reaktif olarak bir miktar kullanım bulur .
Doğal oluşum
Lawrencite , (Fe,Ni)Cl 2 , doğal karşılığıdır ve tipik olarak (nadiren meydana gelmesine rağmen) bir meteoritik mineraldir. Dihidratın doğal formu rokühnittir - çok nadir bir mineraldir. İlgili, ancak daha karmaşık (özellikle bazik veya hidratlı) mineraller, hibbingit , droninoit ve kuliginittir .