döngüsel nükleotid - Cyclic nucleotide

Bir siklik nükleotit (cNMP), şeker ve fosfat grupları arasında siklik bir bağ düzenlemesi olan tek bir fosfat nükleotitidir . Diğer nükleotitler gibi, siklik nükleotitler de üç fonksiyonel gruptan oluşur: şeker, azotlu baz ve tek fosfat grubu. Siklik adenozin monofosfat (cAMP) ve siklik guanozin monofosfat (cGMP) görüntülerinde görülebileceği gibi , 'siklik' kısım, fosfat grubu ile şekerin 3' ve 5' hidroksil grupları arasındaki iki bağdan oluşur; riboz .
Biyolojik önemleri, geniş bir protein - ligand etkileşimleri yelpazesini içerir . Bunlar olarak tespit edilmiştir , ikincil haberciler hem de hormon ve iyon kanalı sinyalleme ökaryotik hücreler, hem de alosterik bileşiklerinin , DNA içinde bağlama proteinleri prokaryotik hücreler. cAMP ve cGMP şu anda en iyi belgelenmiş siklik nükleotidlerdir, ancak cCMP'nin ( sitozin ) ökaryotik hücresel mesajlaşmada da yer aldığına dair kanıtlar vardır . Siklik üridin monofosfatın (cUMP) rolü daha da az bilinmektedir.
Döngüsel nükleotidlerin keşfi, genel olarak protein düzenlemesinin yanı sıra kinaz ve fosfataz mekanizmalarının anlaşılmasına büyük ölçüde katkıda bulunmuştur . İlk keşiflerinden bu yana 50 yıldan fazla bir süre geçmesine rağmen, siklik nükleotidlere ve bunların biyokimyasal ve fizyolojik önemine olan ilgi devam etmektedir.
Tarih
İkinci haberciler kavramının ve özellikle siklik nükleotitlerin rolü ve fizyolojik sinyalleri bir hücreye iletme yeteneklerinin anlaşılması , kökenlerini Carl ve Gerty Cori'nin glikojen metabolizması araştırmalarına borçludur ve bu araştırmaları için kendilerine Nobel verilmiştir. 1947'de Fizyoloji veya Tıp Ödülü. 1950'ler boyunca, araştırmalarına eklenen, öncelikle köpek karaciğerindeki glikojen fosforilaz aktivitesine odaklanan bir dizi artan ama önemli keşif . Glikojen fosforilaz, glikojenolizdeki ilk adımı katalize eder, glikojeni ikame eden glikoz parçalarına ayırma işlemi . Earl Sutherland , adrenalin ve glukagon hormonlarının glikojen fosforilaz üzerindeki etkisini araştırdı ve 1971'de ona Nobel Fizyoloji veya Tıp Ödülü'nü kazandırdı.
1956'da Edwin Krebs ve Edmond Fischer , glikojen fosforilaz b'nin glikojen fosforilaz a'ya dönüştürülmesi için adenozin trifosfatın (ATP) gerekli olduğunu keşfettiler . Sutherland ve Walter Wosilait, adrenalinin ertesi yıl glikojenoliz üzerindeki etkisini araştırırken, karaciğer fosforilaz enzimi inaktive edildiğinde inorganik fosfat salındığını ; ancak aktive edildiğinde bir fosfat içerir. Hormonların ürettiği “aktif faktör” nihayet 1958'de saflaştırıldı ve daha sonra eşit oranlarda bir riboz , bir fosfat ve bir adenin içerdiği tespit edildi . Ayrıca, bu faktörün etkisiz hale getirildiğinde 5'-AMP'ye geri döndüğü kanıtlanmıştır.
Evgeny Fesenko, Stanislav Kolesnikov ve Arkady Lyubarsky 1985'te siklik guanozin monofosfatın (cGMP) çubuklarda fototepkiyi başlatabildiğini keşfettiler . Kısa bir süre sonra, kemosensitif arasında kapılı iyon kanallarında cNMP rolü kirpikler arasında koku alma duyusal nöronlar Tadashi Nakamura ve Geoffrey altın tarafından rapor edilmiştir. 1992'de Lawrence Haynes ve King-Wai Yau, koni fotoreseptörlerinin ışığa bağımlı siklik-nükleotit kapılı kanalında cNMP'nin rolünü ortaya çıkardı . On yılın sonunda, iki tip intramembran reseptörünün varlığı anlaşıldı: Rs ( siklazı stimüle eden ) ve Ri (siklazı inhibe eden). Wei-Jen Tang ve James Hurley 1998'de cAMP'yi sentezleyen adenilil siklazın sadece hormonlar ve nörotransmiterler tarafından değil , aynı zamanda fosforilasyon , kalsiyum , forskolin ve guanin nükleotid bağlayıcı proteinler ( G proteinleri ) tarafından da düzenlendiğini bildirdi .
cNMP'lerin kimyası
Yapı
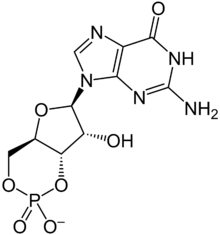
En iyi çalışılmış iki siklik nükleotid, siklik AMP (cAMP) ve siklik GMP (cGMP) iken, siklik CMP (cCMP) ve siklik UMP (cUMP) daha az anlaşılır. cAMP, 3'5'-siklik adenosin monofosfattır, cGMP, 3'5'-siklik guanozin monofosfattır, cCMP, sitidin 3',5'-monofosfattır ve cUMP, üridin 2',3'-siklik fosfattır.
Her siklik nükleotidin üç bileşeni vardır. Azotlu bir baz içerir (yani azot içerir): örneğin, cAMP'de adenin ve cGMP'de guanin . Aynı zamanda bir şeker, özellikle beş karbonlu riboz içerir. Ve son olarak, bir siklik nükleotid bir fosfat içerir. Çift halkalı bir pürin , cAMP ve cGMP için azotlu bazdır, sitozin, timin ve urasil'in her biri tek halkalı bir azotlu baza ( pirimidin ) sahiptir.
Bu üç bileşen, azotlu baz ribozun birinci karbonuna (1' karbon) ve fosfat grubu ribozun 5' karbonuna bağlanacak şekilde bağlanır. Bütün nükleotidler bu yapıya sahipken, fosfat grubu siklik nükleotidlerde 3' karbondaki riboz halkasına ikinci bir bağlantı yapar. Fosfat grubu riboz şekerine iki ayrı bağa sahip olduğundan, halkalı bir halka oluşturur.
Atomu numaralandırma anlaşması bir siklik nükleotid içinde karbon ve azotu tespit etmek için kullanılır. Pentozda, karbonil grubuna en yakın karbon , C-1 olarak etiketlenir. Bir pentoz azotlu bir baza bağlandığında, karbon atomu numaralandırması, bu karbonları azotlu bazın atom numaralarından ayıran bir asal (') notasyonu ile ayırt edilir.
Bu nedenle, cAMP için, 3'5'-siklik adenosin monofosfat, tek bir fosfat grubunun, riboz grubunun 3' ve 5' karbonlarında siklik bir yapı oluşturduğunu, riboz grubunun da adenosine bağlı olduğunu gösterir (bu bağ, ribozun 1' konumunda olmak).
biyokimya
Siklik nükleotitler hem prokaryotik hem de ökaryotik hücrelerde bulunur. Hücre içi konsantrasyonların kontrolü, birkaç protein ailesini içeren bir dizi enzimatik reaksiyon yoluyla sağlanır. Daha yüksek dereceli memelilerde, cNMP'ler birçok doku tipinde bulunur.
Sentez ve Bozunma
Siklik nükleotid cNMP + PP → genel reaksiyon NTP üretilir ı K azotlu bir baz temsil eder. Reaksiyon spesifik nükleotidil siklazlar tarafından katalize edilir, öyle ki cAMP üretimi adenilil siklaz tarafından katalize edilir ve cGMP üretimi guanilil siklaz tarafından katalize edilir . Adenilil siklaz , farklı protein sınıflarını ve farklı cAMP kaynaklarını temsil eden hem transmembran hem de sitozolik formda bulunmuştur .
Hem cAMP hem de cGMP , 3' fosfodiester bağının hidrolizi ile bozulur ve bir 5'NMP ile sonuçlanır. Bozunma, öncelikle fosfodiesterazlar (PDE'ler) olarak bilinen bir enzim sınıfı tarafından gerçekleştirilir . Memeli hücrelerinde, hücrenin düzenleyici ihtiyaçlarına göre ifade edilen her proteinin değişen izoformlarına sahip bilinen 11 PDE ailesi vardır . Bazı fosfodiesterazlar cNMP'ye özgüdür, diğerleri ise spesifik olmayan şekilde hidrolize edebilir. Bununla birlikte, cAMP ve cGMP bozunma yolları, cCMP veya cUMP için olanlardan çok daha fazla anlaşılmıştır. cCMP ve cUMP için spesifik PDE'lerin tanımlanması tam olarak oluşturulmamıştır.
hedef bağlama
Siklik nükleotitler, foto-reseptör çubuklar ve koniler, düz kas hücreleri ve karaciğer hücreleri dahil olmak üzere birçok farklı ökaryotik hücre türünde bulunabilir . Siklik nükleotitlerin hücresel konsantrasyonları, 10 −7 M aralığında çok düşük olabilir , çünkü metabolizma ve fonksiyon genellikle hücrenin belirli kısımlarında lokalizedir. Biyolojik fonksiyonlarından bağımsız olarak cNMP'leri bağlayan tüm proteinlerde yüksek oranda korunmuş bir siklik nükleotid bağlama alanı (CNB) bulunur. Alan, beta sayfaları arasında döngüsel nükleotid bağlama cebi ile bir beta sandviç mimarisinden oluşur . cNMP'nin bağlanması, proteinin aktivitesini etkileyen bir konformasyonel değişikliğe neden olur. CCMP etkili konsantrasyonunu (EC indirgenmeyle, birden çok siklik nükleotidler arasında sinerjistik bir etki bağlayıcı destekleyen veriler de vardır 50 aktivasyonu için cAMP) protein, bir kinaz (PKA).
Biyoloji
Döngüsel nükleotitler, hücreler içinde hareket eden bir iletişim sisteminin ayrılmaz bir parçasıdır. Hormonlar ve nörotransmitterler gibi birçok birinci habercinin sinyallerini fizyolojik hedeflerine ileterek "ikinci haberciler" olarak hareket ederler. Siklik nükleotidler, reseptör-efektör eşleşmesi, ilaç tepkisinin aşağı regülasyonu, protein-kinaz kaskadları ve transmembran sinyal iletimi dahil olmak üzere birçok fizyolojik tepkiye katılır.
Siklik nükleotidler, hücreye giremeyen ilk haberciler bunun yerine hücre zarındaki reseptörlere bağlandığında ikinci haberciler olarak hareket eder. Reseptör, konformasyonu değiştirir ve hücre zarının iç kısmında adenilil siklaz adı verilen bir enzimi aktive eden bir sinyal iletir. Bu, cAMP'yi hücre içine bırakır ve burada siklik AMP'ye bağımlı protein kinazı adı verilen bir protein kinazı uyarır. Proteinleri fosforile ederek, siklik AMP'ye bağımlı protein kinaz, protein aktivitesini değiştirir. cAMP'nin bu süreçteki rolü, fosfodiesteraz tarafından AMP'ye hidroliz edildikten sonra sona erer.
| döngüsel nükleotid | Bilinen bağlayıcı proteinler | Yol/Biyolojik dernek |
|---|---|---|
| kamp |
|
|
| cGMP |
|
|
| cCMP |
|
|
Döngüsel nükleotitler, birkaç nedenden dolayı ikinci haberciler olarak hareket etmek için çok uygundur. Sentezleri enerjik olarak uygundur ve ortak metabolik bileşenlerden (ATP ve GTP) türetilirler. AMP/GMP ve inorganik fosfata parçalandıklarında bu bileşenler toksik değildir. Son olarak, siklik nükleotitler, daha küçük ve daha az polar oldukları için siklik olmayan nükleotidlerden ayırt edilebilirler .
biyolojik önemi
Döngüsel nükleotidlerin biyolojik işlevlere katılımı çeşitlilik gösterirken, rollerinin anlaşılması da gelişmeye devam ediyor. Biyolojik etkilerinin birkaç örneği vardır. Uzun süreli ve kısa süreli hafıza ile ilişkilidirler. Ayrıca kan şekerini ve diğer besinleri kontrol eden çeşitli enzimleri koordine etmek için karaciğerde çalışırlar . İçinde bakteri , siklik nükleotid bağlama hızını arttırarak metabolik enzimatik etkinliği arttırmak için de faaliyet katabolit gen aktivatör protein (CAP) için DNA, transkripsiyonu . Ayrıca vasküler dokudaki düz kas hücrelerinin gevşemesini kolaylaştırırlar ve retinal fotoreseptörlerde ve koku alma duyu nöronlarında siklik CNG kanallarını aktive ederler . : Buna ek olarak, bu potansiyel olarak siklik CNG kanalları etkinleştirmek pineal bez ışık hassasiyeti, duyusal nöronlar Bu organ (tespiti katılır feromonlar ), tat reseptör hücreleri, hücre sinyal olarak sperm , solunum yolu epitel hücreler, gonadotropin salgılatıcı hormon (GnRH) salgılayan nöronal hücre hattı ve renal iç medüller toplayıcı kanal .
cNMP yollarının bozulması örnekleri şunları içerir: CNG kanal genlerindeki mutasyonlar , retina dejenerasyonu ve renk körlüğü ile ilişkilidir ; ve sitozolik veya çözünür adenilil siklazın (sAC) aşırı ekspresyonu , insan prostat karsinomuyla ilişkilendirilmiştir . sAC'nin inhibisyonu veya RNA interferansı (RNAi) transfeksiyonu ile yıkımın prostat karsinomu hücrelerinin proliferasyonunu önlediği gösterilmiştir . Düzenleyici yol, PKA yolunun değil, EPAC yolunun bir parçası gibi görünmektedir.
cNMP bozulmasının temel düzenleyicileri olan fosfodiesterazlar, genellikle terapötikler için hedeflerdir. Kafein bilinen bir PDE inhibitörüdür, sildenafil ve tadalafil gibi erektil disfonksiyon tedavisinde kullanılan ilaçlar da fosfodiesterazların aktivitesini inhibe ederek etki gösterir.
Referanslar
Dış bağlantılar
- Nükleotidler,+Siklik ABD Ulusal Tıp Kütüphanesinde Tıbbi Konu Başlıkları (MeSH)


