Varisella zoster virüsü - Varicella zoster virus
| İnsan alfaherpes virüsü 3 | |
|---|---|
|
|
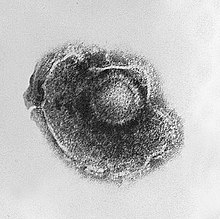
| Bir İnsan alphaherpesvirus 3 virionunun elektron mikrografı | |
|
Virüs sınıflandırması |
|
| (rütbesiz): | Virüs |
| Bölge : | Duplodnaviria |
| Krallık: | heunggongvirae |
| filum: | peploviricota |
| Sınıf: | Herviviricetes |
| Emir: | herpes virüsü |
| Aile: | herpes virüsü |
| cins: | suçiçeği virüsü |
| Türler: |
İnsan alfaherpes virüsü 3
|
| Eş anlamlı | |
|
|
Genellikle varicella-zoster virüsü ( VZV )olarak adlandırılan insan alfaherpes virüsü 3 ( HHV-3 ),insanları enfekte ettiği bilinendokuz herpes virüsünden biridir. Bu neden suçiçeği (suçiçeği) , bir hastalık en sık çocukları, gençleri ve genç yetişkinleri ve etkileyen zona (herpes zoster) erişkinlerde; çocuklarda zona nadirdir. VZV enfeksiyonlarıinsanlara özgü türlerdir , ancak dış ortamlarda birkaç saat hayatta kalabilirler.
VZV akciğerlerde çoğalır ve çok çeşitli semptomlara neden olur. Birincil enfeksiyondan (suçiçeği) sonra virüs, kraniyal sinir gangliyonları, dorsal kök gangliyonları ve otonomik gangliyonlar dahil olmak üzere sinirlerde uykuda kalır. Kişi su çiçeği hastalığından kurtulduktan yıllar sonra, VZV nörolojik koşullara neden olmak için yeniden aktif hale gelebilir.
epidemiyoloji
Birincil suçiçeği zoster virüsü enfeksiyonu , ensefalit , pnömoni (doğrudan viral pnömoni veya ikincil bakteriyel pnömoni ) veya bronşit (viral bronşit veya ikincil bakteriyel bronşit) dahil olmak üzere komplikasyonlara neden olabilen su çiçeği (varisella) ile sonuçlanır . Suçiçeğinin klinik semptomları düzeldiğinde bile VZV , enfekte kişinin sinir sisteminde ( virüs latansı ), trigeminal ve dorsal kök ganglionlarında uykuda kalır . VZV solunum sistemi yoluyla girer. Kuluçka süresi 10-21 gün, ortalama 14 gün. Deriyi ve periferik siniri hedef alan hastalık süresi 3 ila 4 gündür. Döküntülerin ortaya çıkmasından 1-2 gün önce bu virüsün en bulaşıcı olduğu zamandır. İşaretler ve semptomlar, iyileşmeden önce irin, yırtılma ve kabukla dolan vezikülleri içerir. Lezyonlar en sık yüz, boğaz, bel, göğüs ve omuzlarda görülür.
Vakaların yaklaşık üçte birinde, VZV yaşamın ilerleyen dönemlerinde yeniden etkinleşir ve zona veya herpes zoster olarak bilinen bir hastalığa neden olur .
Herpes zoster geliştirmenin yaşam boyu bireysel riskinin %20 ile %30 arasında veya yaklaşık olarak 4 kişide 1 olduğu düşünülmektedir. Ancak 85 yaş ve üzeri bireylerde bu risk 2 kişide 1'e çıkmaktadır. Nilsson ve arkadaşları (2015) tarafından İsveç'te yapılan bir çalışmada, herpes zoster enfeksiyonunun yıllık insidansı, her yaş için 100.000 kişi başına toplam 315 vaka ve 50 yaş ve üzeri kişiler için 100.000 kişi başına 577 vaka olarak tahmin edilmektedir. VZV, İsviçre'de 100.000 kişi başına 1.02 vaka insidans oranı ve İsveç'te 100.000 kişi başına yıllık 1.8 vaka insidans oranı bildiren bir 2013 makalesi ile merkezi sinir sistemini de enfekte edebilir.
Genellikle yanma olarak tanımlanan zona lezyonları ve ilişkili ağrı, bir veya iki bitişik duyu siniri tarafından innerve edilen ciltte, neredeyse her zaman vücudun sadece bir tarafında meydana gelme eğilimindedir. Deri lezyonları genellikle birkaç hafta içinde azalırken, ağrı genellikle daha uzun süre devam eder. Olguların %10-15'inde ağrı, postherpetik nevralji olarak bilinen kronik ve sıklıkla sakat bırakan bir durum olan üç aydan fazla sürer . Varicella zoster enfeksiyonunun diğer ciddi komplikasyonları arasında Mollaret menenjiti , zoster multipleks ve beyinde felç, miyelit, herpes oftalmikus veya zoster sinüs herpete yol açan arterlerin iltihaplanması yer alır. In Ramsay Hunt sendromu , VZV yüz sinirinin belirli dalları izleyin lezyonlar veren genikulate ganglion etkiler. Semptomlar, dilde ve kulakta ağrılı kabarcıkların yanı sıra tek taraflı yüz zayıflığı ve işitme kaybını içerebilir. Hamileliğin ilk aşamalarında enfekte olursa, fetusta ciddi hasar meydana gelebilir. Reye sendromu , ilk enfeksiyondan sonra ortaya çıkabilir ve sürekli kusmaya ve aşırı uyuşukluk veya kavgacı davranış gibi beyin fonksiyon bozukluğu belirtilerine neden olabilir. Bazı durumlarda, ölüm veya koma takip edebilir. Reye sendromu çoğunlukla çocukları ve gençleri etkiler, enfeksiyon sırasında aspirin kullanmak bu riski artırabilir.
morfoloji
VZV, çok fazla genom homolojisi paylaşan herpes simpleks virüsleri (HSV) ile yakından ilişkilidir . Bilinen zarf glikoproteinleri (gB, gC, gE, gH, gI, gK, gL) HSV'dekilere karşılık gelir; ancak, HSV gD'nin eşdeğeri yoktur. VZV ayrıca, HSV gecikmesinin (herpes simpleks virüsü) oluşturulmasında önemli bir rol oynayan LAT'yi (gecikme ile ilişkili transkriptler) üretmede başarısız olur. VZV viryonları küreseldir ve çapı 180-200 nm'dir. Lipit zarfları , ikosahedral biçimde düzenlenmiş 162 heksamerik ve pentamerik kapsomerin 100 nm nükleokapsidini çevreler . DNA'sı 125.000 nt uzunluğunda tek, doğrusal, çift sarmallı bir moleküldür . Kapsid, topluca tegument olarak bilinen gevşek bir şekilde ilişkili proteinlerle çevrilidir; bu proteinlerin çoğu, enfekte olmuş hücrede virüs üreme sürecini başlatmada kritik roller oynar. Tegument sırayla, her biri yaklaşık 8 nm uzunluğunda olan virionun dışında görüntülenen glikoproteinlerle süslenmiş bir lipit zarfla kaplanır.
genomlar
Genom ilk olarak 1986'da dizilendi. Bu lineer bir dubleks DNA molekülüdür, bir laboratuvar suşu 124.884 baz çiftine sahiptir. Genom, S segmentinin oryantasyonuna bağlı olarak, toplam %90-95'lik bir frekans için eşit frekansta bulunan P (prototip) ve I S (ters S) olmak üzere 2 baskın izomere sahiptir . L segmenti ayrıca ters çevrilerek toplam dört lineer izomer ( IL ve ILS ) elde edilebilir. Bu, HSV'nin eşit olası dağılımından farklıdır ve ayrımcı mekanizma bilinmemektedir. İzole edilmiş moleküllerin küçük bir yüzdesi, hakkında çok az şey bilinen dairesel genomlardır. (HSV'nin enfeksiyon üzerinde sirkülerleştiği bilinmektedir.) Genomda en az 70 açık okuma çerçevesi vardır.
Bu virüsün en az beş kolu var . Klasör 1 ve 3, Avrupa/Kuzey Amerika soylarını içerir; clade 2, özellikle Japonya'dan gelen Asya suşlarıdır; ve 5. madde Hindistan'da yerleşik gibi görünüyor . Clade 4, Avrupa'dan bazı suşları içerir, ancak coğrafi kökenlerinin daha fazla açıklığa kavuşturulması gerekir.
Evrim
HSV1 ve HSV2 ile benzerlik, ortak bir ataya işaret eder; beş gen, karşılık gelen HSV genlerine sahip değildir. Diğer insan herpes virüsleri ile ilişki daha az güçlüdür, ancak birçok homolog ve korunmuş gen bloğu hala bulunmaktadır.
Beş ana dal (1-5) ve bu dallara uymayan dört genotip vardır. Bu dalların şu anki dağılımı Asya (1, 2 ve 5) ve Avrupa'dır (1, 3 ve 4). VZV suşlarının tüm virüs genomunun gerekli dizisini kladlara tahsisi. Pratik olarak küresel VZV suşlarının dağılımına ilişkin tüm moleküler epidemiyolojik veriler, seçilen bölgelerin hedeflenen dizilimi ile elde edilir.
VZV genomik dizilerinin filogenetik analizi, vahşi tip suşları 9 genotipe (E1, E2, J, M1, M2, M3, M4, VIII ve IX) ayırır. M3 ve M4 suşları için tam sekanslar mevcut değildir, ancak temsili suşların hedeflenen analizleri, bunların stabil, dolaşan VZV genotipleri olduğunu göstermektedir. VZV izolatlarının dizi analizi, her genotip için hem paylaşılan hem de spesifik belirteçleri tanımladı ve birleşik bir VZV genotipleme stratejisini doğruladı. Yüksek genotip çeşitliliğine rağmen, genotipik rekombinasyon için hiçbir kanıt gözlenmedi. Yedi VZV genotipinden beşi, ORF22'de bulunan sadece dört tek nükleotid polimorfizmi (SNP) kullanılarak güvenilir bir şekilde ayırt edildi ve E1 ve E2 genotipleri, ORF21, ORF22 veya ORF50'de bulunan SNP kullanılarak çözüldü. 18 Avrupa ülkesinden 342 klinik suçiçeği ve zoster örneğinin dizi analizi, aşağıdaki VZV genotip dağılımını tanımladı: E1, 221 (%65); E2, 87 (%25); M1, 20 (%6); M2, 3 (% 1); M4, 11 (% 3). M3 veya J suşu gözlenmedi. Avustralya ve Yeni Zelanda'dan bu yaklaşım kullanılarak tiplendirilen 165 klinik suçiçeği ve zoster izolatından 127 doğu Avustralya izolatının 67'si E1, 30'u E2, 16'sı J, 10'u M1 ve 4'ü M2 idi; 38 Yeni Zelanda izolatından 25'i E1, 8'i E2 ve 5'i M1 idi.
Herpesvirüsler arasındaki eşanlamlı ve eş anlamlı olmayan mutasyon oranları için mutasyon oranı , yüksek oranda korunmuş gB genine dayalı olarak sırasıyla 1 × 10 −7 ve 2,7 × 10 −8 mutasyon/yer/yıl olarak tahmin edilmiştir .
Tedavi
İnsan vücudunda , su çiçeği için asiklovir , famsiklovir , zona için valasiklovir , zoster-immün globulin (ZIG) ve vidarabin dahil olmak üzere bir dizi ilaç ve terapötik ajan ile tedavi edilebilir . VZV immün globulin de bir tedavidir. Asiklovir, primer VZV enfeksiyonlarında sıklıkla tercih edilen ilaç olarak kullanılır ve uygulamaya erken başlanması herhangi bir semptomun süresini önemli ölçüde kısaltabilir. Bununla birlikte, etkili bir serum asiklovir konsantrasyonuna ulaşmak tipik olarak intravenöz uygulamayı gerektirir ve bu da hastane dışında kullanımını zorlaştırır.
aşı
Canlı, zayıflatılmış bir VZV Oka/Merck suşu aşısı mevcuttur ve Amerika Birleşik Devletleri'nde Varivax ticari adı altında pazarlanmaktadır . Bu tarafından geliştirilen Merck, Sharp & Dohme izole edilmiş ve zayıflatılmış Oka gerginlik virüs 1980'lerde Michiaki Takahashi 1970'lerde ve meslektaşları. 1990 yılında ABD Gıda ve İlaç Dairesi'ne onay için sunulmuş ve 1995 yılında onaylanmıştır. O zamandan beri Avustralya , Amerika Birleşik Devletleri ve diğer birçok ülkede çocuklar için önerilen aşı programlarına eklenmiştir . Suçiçeği aşısı, bazılarında aşının neden olduğu bağışıklığın ömür boyu olamayacağı endişelerini artırdı ve muhtemelen yetişkinleri çocukluk aşılarının bağışıklığı azaldıkça daha ciddi hastalıklara karşı savunmasız bıraktı. Amerika Birleşik Devletleri'nde aşılama için önerilen popülasyonda aşı kapsamı %90'a yaklaşıyor ve buna eşlik eden suçiçeği vakaları ve VZV'ye bağlı hastaneye yatışlar ve ölümlerde azalma. Şimdiye kadar, klinik veriler, aşının sağlıklı bireylerde suçiçeği enfeksiyonunu önlemede on yılı aşkın bir süredir etkili olduğunu ve çığır açan enfeksiyonlar meydana geldiğinde, hastalığın tipik olarak hafif olduğunu kanıtlamıştır . 2006 yılında, CDC'nin Bağışıklama Uygulamaları Danışma Komitesi (ACIP), suçiçeği bağışıklığının yüksek seviyelerinin korunmasını sağlamak için okula başlamadan önce ikinci bir aşı dozu önerdi.
2006 yılında Amerika Birleşik Devletleri Gıda ve İlaç Dairesi Zostavax'ı zona hastalığının önlenmesi için onayladı . Zostavax, VZV'ye karşı bağışıklığı ilerleyen yaşla birlikte azalan yaşlı erişkinlerde bir bağışıklık tepkisi ortaya çıkarmak için tasarlanmış, Varivax aşısının daha konsantre bir formülasyonudur. Cochrane Kütüphanesi tarafından yapılan sistematik bir inceleme , Zostavax'ın zona insidansını neredeyse %50 oranında azalttığını gösteriyor.
Shingrix, GlaxoSmithKline tarafından geliştirilen ve Amerika Birleşik Devletleri'nde FDA tarafından Ekim 2017'de onaylanan bir V. zoster aşısıdır . ACIP, Zostavax almış olanlar da dahil olmak üzere 50 yaşın üzerindeki yetişkinler için Shingrix'i önerdi. Komite, zoster ve ilgili komplikasyonların önlenmesinde Zostavax'a göre Shingrix'in tercih edildiğine oy verdi, çünkü faz 3 klinik verileri, tüm yaş gruplarında zonaya karşı >%90'lık bir aşı etkinliğinin yanı sıra 4 yıllık bir takipte sürekli etkinlik gösterdi. Tek atış olarak verilen Zostavax'tan farklı olarak Shingrix, iki ila altı ay arayla iki intramüsküler doz olarak verilir.
Bir herpes-zoster alt birimi (HZ-su) aşısının, insan immün yetmezlik virüsü olan yetişkinlerde immünojenik ve güvenli olduğu gösterilmiştir.
Tarih
Su çiçeği benzeri döküntüler eski uygarlıklar tarafından tanındı ve tanımlandı; zoster ve suçiçeği arasındaki ilişki 1888'e kadar fark edilmedi. 1943'te zoster lezyonlarından izole edilen virüs partikülleri ile suçiçeğinden izole edilen virüs partikülleri arasındaki benzerlik kaydedildi. 1974'te ilk suçiçeği aşısı tanıtıldı.
Ayrıca bakınız
Referanslar
Dış bağlantılar
- "Suçiçeği (Suçiçeği) Aşısı" . Hastalık Kontrol ve Önleme Merkezleri (CDC). 2017-07-07.
