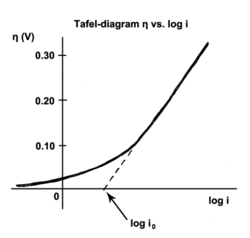
Tafel denklemi - Tafel equation
Tafel eşitliği bir denklemdir elektrokimyasal kinetik bir oranını bulunan elektrokimyasal reaksiyon üst potansiyeli . Tafel denklemi ilk olarak deneysel olarak çıkarıldı ve daha sonra teorik bir gerekçeye sahip olduğu gösterildi. Denklem ismini İsviçreli kimyager Julius Tafel'in almıştır .
"Bir elektrottan geçen elektrik akımının basit, tek moleküllü bir redoks reaksiyonu için elektrot ile toplu elektrolit arasındaki voltaj farkına nasıl bağlı olduğunu açıklar".
Ayrı elektrotlarda iki yarım tepkimede bir elektrokimyasal tepkime meydana geldiğinde , Tafel denklemi her elektroda ayrı ayrı uygulanır. Tek bir elektrot üzerinde Tafel denklemi şu şekilde ifade edilebilir:
-
( 1 )
nerede
- üs altındaki artı işareti anodik bir reaksiyonu ve eksi işareti katodik reaksiyonu belirtir,
- : aşırı potansiyel
- : " Tafel eğimi ", V
- : Akım yoğunluğu , A / m'den 2
- : " Kuru akım yoğunluğu ", A / m 2 .
Bu denklem için bir doğrulama ve daha fazla açıklama burada bulunabilir. Tafel denklemi, durumunda Butler-Volmer denkleminin bir yaklaşımıdır .
"[Tafel denklemi], elektrottaki konsantrasyonların pratik olarak toplu elektrolitteki konsantrasyonlara eşit olduğunu varsayar ve akımın yalnızca potansiyelin bir fonksiyonu olarak ifade edilmesini sağlar. Başka bir deyişle, elektrot kütle aktarım hızının şu olduğunu varsayar. reaksiyon hızından çok daha büyüktür ve reaksiyona daha yavaş kimyasal reaksiyon hızı hakimdir ".
Ayrıca, belirli bir elektrotta Tafel denklemi, ters yarı reaksiyon hızının ileri reaksiyon hızına kıyasla ihmal edilebilir olduğunu varsayar.
Terimlere genel bakış
Değişim akımı, dengedeki akımdır, yani oksitlenmiş ve indirgenmiş türlerin elektrotla elektron transfer etme hızıdır. Başka bir deyişle, değişim akımı yoğunluğu, tersinir potansiyeldeki reaksiyon hızıdır (aşırı potansiyel tanım gereği sıfır olduğunda). Tersinir potansiyelde, reaksiyon dengededir, yani ileri ve geri reaksiyonların aynı hızlarda ilerlediği anlamına gelir. Bu oran, değişim akımı yoğunluğudur.
Tafel eğimi deneysel olarak ölçülür. Bununla birlikte, teorik olarak, baskın reaksiyon mekanizması, tek bir elektronun transferini içerdiğinde gösterilebilir.
burada A olarak tanımlanır
-
( 2 )
nerede
- olan Boltzmann sabiti ,
- bir mutlak sıcaklık ,
- bir elektronun elektrik temel yüküdür ,
- olan termal gerilim ve
- değeri 0 ile 1 arasında olması gereken " yük transfer katsayısı " dır .
İhmal edilemeyen elektrot kütle transferi durumunda denklem
Daha genel bir durumda,
"Genişletilmiş Butler-Volmer denkleminin aşağıdaki türevi Bard ve Faulkner ve Newman ve Thomas-Alyea'nınkinden uyarlanmıştır". "[...] akım yalnızca potansiyelin (basit versiyondaki gibi) değil, verilen konsantrasyonların da bir fonksiyonu olarak ifade edilir. Kütle aktarım hızı nispeten küçük olabilir, ancak kimyasal üzerindeki tek etkisi reaksiyon, değişen (verilen) konsantrasyonlar aracılığıyladır. Gerçekte, konsantrasyonlar da potansiyelin bir fonksiyonudur ".
Tafel denklemi şu şekilde de yazılabilir:
-
( 3 )
nerede
- n, Nernst denkleminde olduğu gibi, değiştirilen elektron sayısıdır ,
- üs altındaki artı işareti anodik bir reaksiyonu ve eksi işareti katodik reaksiyonu belirtir,
- k, s −1'deki elektrot reaksiyonu için hız sabitidir ,
- R, evrensel gaz sabitidir ,
- C, mol / m² cinsinden elektrot yüzeyindeki reaktif tür konsantrasyonudur.
Gösteri
Denklem ( 1 ) ' de görüldüğü gibi ,
, yani:
, denklem ( 2 ) ' de görüldüğü gibi ve çünkü .
Çünkü
sonunda denklemi ( 3 ) veren elektrot kütle transferi nedeniyle .
Düşük polarizasyon değerleri durumunda denklem
Düşük polarizasyon değerlerinde başka bir denklem uygulanabilir . Böyle bir durumda, akımın polarizasyona bağımlılığı genellikle doğrusaldır (logaritmik değil):
Bu doğrusal bölgeye, Ohm yasasına biçimsel benzerliği nedeniyle kutuplaşma direnci denir .
Ayrıca bakınız
- Aşırı potansiyel
- Butler-Volmer denklemi
- Elektrokatalizör
- Sınırlama akımı
- Faraday'ın elektroliz yasaları
Referanslar
- GT Burstein (2005). "Tafel Denkleminin Yüzyılı: 1905–2005 Korozyon Biliminin Hatıra Sorunu". Korozyon Bilimi . 47 (12): 2858–2870. doi : 10.1016 / j.corsci.2005.07.002 .
Dış bağlantılar
-
 Wikimedia Commons'ta Tafel denklemiyle ilgili medya
Wikimedia Commons'ta Tafel denklemiyle ilgili medya