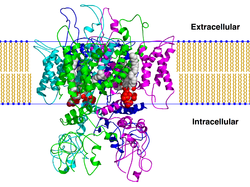
TRPV1 - TRPV1
Geçici reseptör potansiyel katyon kanalı alt ailesi V 1 ( TRPV1 olarak da bilinir), kapsaisin reseptörü ve vanilloid reseptörü 1 , a, bir protein , insanlarda, ile kodlanan, bu TRPV1 geni . Bu, geçici reseptör potansiyel protein grubunun bir alt ailesi olan geçici reseptör potansiyel vanilloid reseptör proteinlerinin ilk izole edilmiş üyesiydi. Bu protein, iyon kanallarının geçici reseptör potansiyel ailesinin TRPV grubunun bir üyesidir .
TRPV1'in işlevi, vücut sıcaklığının tespiti ve düzenlenmesidir . Ek olarak, TRPV1, haşlanma ısısı ve ağrı hissi ( nosisepsiyon ) sağlar. Birincil afferent duyusal nöronlarda , zararlı çevresel uyaranların saptanmasına aracılık etmek için TRPA1 (kimyasal tahriş edici bir reseptör) ile işbirliği yapar .
İşlev
TRPV1, memeli somatosensör sistemi tarafından kullanılan bir element veya mekanizmadır . Çok çeşitli eksojen ve endojen fiziksel ve kimyasal uyaranlar tarafından aktive edilebilen seçici olmayan bir katyon kanalıdır . TRPV1'in en iyi bilinen etkinleştiricileri şunlardır: 43 °C'den (109 °F) yüksek sıcaklık; asidik koşullar; kapsaisin (acı biberlerdeki tahriş edici bileşik); ve alil izotiyosiyanat , keskin hardal ve wasabi'ait bileşik. TRPV1'in aktivasyonu ağrılı, yanma hissine yol açar. Endojen aktivatörleri şunları içerir: düşük pH (asidik koşullar), endokannabinoid anandamid , N-oleil-dopamin ve N-arakidonoil-dopamin . TRPV1 reseptörleri esas olarak periferik sinir sisteminin nosiseptif nöronlarında bulunur , ancak merkezi sinir sistemi de dahil olmak üzere diğer birçok dokuda da tanımlanmıştır . TRPV1, ağrının iletimi ve modülasyonunda ( nosisepsiyon ) ve ayrıca çeşitli ağrılı uyaranların entegrasyonunda yer alır.
Duyarlılık
TRPV1'in yüksek sıcaklıklar gibi zararlı uyaranlara duyarlılığı statik değildir. Doku hasarı ve bunun sonucunda meydana gelen iltihaplanma üzerine , çeşitli prostaglandinler ve bradikinin gibi bir dizi enflamatuar aracı madde salınır. Bu ajanlar, nosiseptörlerin zararlı uyaranlara duyarlılığını arttırır. Bu, ağrılı uyaranlara karşı artan hassasiyet ( hiperaljezi ) veya ağrısız uyaranlara yanıt olarak ağrı hissi ( allodini ) olarak kendini gösterir. Hassaslaştırıcı proinflamatuar ajanların çoğu, fosfolipaz C yolunu aktive eder . TRPV1'in protein kinaz C tarafından fosforilasyonunun, TRPV1'in duyarlılaşmasında rol oynadığı gösterilmiştir. PIP2'nin PLC-beta tarafından bölünmesi, TRPV1'in disinhibisyonu ile sonuçlanabilir ve sonuç olarak, TRPV1'in zararlı uyaranlara duyarlılığına katkıda bulunur.
duyarsızlaştırma
Kapsaisine uzun süre maruz kalındığında TRPV1 aktivitesi azalır, buna duyarsızlaşma adı verilir . Bu fenomen için hücre dışı kalsiyum iyonları gereklidir, bu nedenle kalsiyum akışı ve buna bağlı olarak hücre içi kalsiyum artışı bu etkiye aracılık eder. Gibi çeşitli sinyal yolları kalmodulin ve kalsinörin ve azalması PIP 2 , TRPV1 duyarsızlaştırılmasında etkili olduğu görülmüştür. TRPV1'in duyarsızlaştırılmasının kapsaisinin paradoksal analjezik etkisinin altında yattığı düşünülmektedir .
Klinik önemi
Periferik sinir sistemi
Nosisepsiyondaki katılımının bir sonucu olarak TRPV1, ağrı azaltıcıların ( analjezikler ) geliştirilmesi için bir hedef olmuştur . Üç ana strateji kullanılmıştır:
TRPV1 Kullanımı
TRPV1 reseptörü, bir organizmanın sıcaklık değişimini nasıl algıladığını ölçebilmek için faydalıdır. Laboratuarda reseptör, farelerden ortam sıcaklığındaki farklılıkları tespit edememelerine neden olacak şekilde çıkarılabilir. Farmasötik alanda bu, enflamatuar rahatsızlıkları veya şiddetli yanma ağrıları olan hastalara ağrı olmadan iyileşme şansı veren ısı reseptörlerinin bloke edilmesine izin verir. TRPV1 reseptörünün olmaması, ısı çoğu organizmayı yeterince büyük dozlarda öldürebildiğinden, gelişmekte olan beyne bir bakış sağlar, bu nedenle bu uzaklaştırma işlemi, araştırmacılara, ısıyı algılayamamanın bir organizmanın hayatta kalmasına nasıl zararlı olabileceğini gösterir ve ardından bunu, insan ısı bozuklukları.
antagonistler
Antagonistler TRPV1 aktivitesini bloke ederek ağrıyı azaltır. Tanımlanan antagonistler, rekabetçi antagonist kapsazepin ve rekabetçi olmayan antagonist rutenyum kırmızısını içerir . Bu ajanlar, sistemik olarak uygulandığında faydalı olabilir. İlaç firmaları tarafından çok sayıda TRPV1 antagonisti geliştirilmiştir. TRPV1 antagonistleri , sıçanlarda inflamatuar ve nöropatik ağrı modellerinden gelen nosisepsiyonun azaltılmasında etkinlik göstermiştir . Bu, TRPV1'in kapsaisinin tek reseptörü olduğuna dair kanıt sağlar . İnsanlarda, TRPV1 reseptörlerine etki eden ilaçlar , multipl skleroz , kemoterapi veya ampütasyon ile ilişkili nöropatik ağrının yanı sıra, örneğin hasarlı dokunun inflamatuar yanıtıyla ilişkili ağrıyı tedavi etmek için kullanılabilir. osteoartritte olduğu gibi .
Bu ilaçlar, terapötik uygulama için bir zorluk olan vücut ısısını ( hipertermi ) etkileyebilir . Örneğin, TRPV1 antagonisti AMG-9810'un uygulanmasıyla sıçanlarda geçici bir sıcaklık artışı (yaklaşık 40 dakikalık bir süre için ~1 °C, 40 dakikada taban çizgisine geri döner) ölçülmüştür . TRPV1'in vücut sıcaklığının düzenlenmesindeki rolü son birkaç yılda ortaya çıkmıştır. Vücut sıcaklığında hafif bir artışa ( hipertermi ) neden olan bir dizi TRPV seçici antagoniste dayanarak , TRPV1'in in vivo tonik olarak aktif olduğu ve vücuda "kendini soğumasını" söyleyerek vücut ısısını düzenlediği öne sürülmüştür. Bu sinyaller olmadan vücut aşırı ısınır. Benzer şekilde, bu, kapsaisinin (bir TRPV1 agonisti) terlemeye neden olma eğilimini açıklar (yani, vücut ısısını düşürmek için bir sinyal). Yakın tarihli bir raporda, tonik olarak aktif TRPV1 kanallarının iç organlarda bulunduğu ve vücut ısısı üzerinde devam eden bir baskılayıcı etkiyi sürdürdüğü bulundu. Son zamanlarda, TRPV1'in baskın fonksiyonunun vücut sıcaklığının korunması olduğu öne sürülmüştür. Deneyler, TRPV1 blokajının, kemirgenler ve insanlar da dahil olmak üzere birçok türde vücut ısısını arttırdığını göstermiştir, bu da TRPV1'in vücut ısısının korunmasına dahil olduğunu düşündürmektedir. 2008'de, yüksek düzeyde seçici bir TRPV1 antagonisti olan AMG-517 , hipertermi (~38.3 °C ortalama artış, 1. günde en yoğun olan ancak 2-7. günlerde zayıflayan) nedeniyle klinik deneylerden çıkarıldı. Başka bir molekül, SB-705498 de klinikte değerlendirildi ancak vücut ısısı üzerindeki etkisi rapor edilmedi.TRPV1'in modaliteye özgü agonizminin anlaşılmasını artırdıkça , TRPV1'i hedefleyen yeni nesil terapötiklerin yan basamak hipertermi potansiyeline sahip olduğu görülüyor. en az iki endikasyon veya yaklaşım bu ikincil bir sorun olabilir Terapötik yaklaşımın (örneğin analjezide) agonist aracılı duyarsızlaştırma olduğu durumlarda, antagonistlerin etkilerinin hipertermik etkileri ilgili olmayabilir.İkincil olarak TRPV1 antagonizması gibi uygulamalarda kalp yetmezliği gibi ciddi durumların tedavisi, o zaman hafif hipertermi ile kabul edilebilir bir takas olabilir, ancak kemirgen kalp yetmezliği modellerinde hipertermi gözlenmemiştir. BCTC, SB-366791 veya AMG-9810 ile yeniden işleme tabi tutulur . TRPV1 proteininin fosforilasyonu ile translasyon sonrası modifikasyonu , işlevselliği için kritiktir. NIH'den yayınlanan raporlar, ligand kaynaklı kanal açılması için TRPV1'in Cdk5 aracılı fosforilasyonunun gerekli olduğunu göstermektedir.
agonistler
TRPV1, doğal kaynaklardan çok sayıda agonist tarafından aktive edilir. Kapsaisin ve resiniferatoksin gibi agonistler, TRPV1'i aktive eder ve uzun süreli uygulama üzerine, TRPV1 aktivitesinin azalmasına (duyarsızlaşma) neden olarak, zararlı uyaranlara maruz kalmanın ardından TRPV1 aracılı enflamatuar moleküllerin salınımında müteakip azalma yoluyla ağrının hafiflemesine yol açar. Agonistler ağrılı bölgeye çeşitli şekillerde, genellikle yama veya merhem şeklinde lokal olarak uygulanabilir. Düşük konsantrasyonlarda kapsaisin (%0.025 - 0.075%) içeren çok sayıda kapsaisin içeren kremler tezgahta mevcuttur. Bu preparatların gerçekten TRPV1 duyarsızlaşmasına yol açıp açmadığı tartışılmaktadır; karşı tahriş yoluyla hareket etmeleri mümkündür. Daha yüksek kapsaisin konsantrasyonu (%10'a kadar) içeren yeni müstahzarlar klinik deneyler altındadır. Yüzde sekiz kapsaisin yamaları yakın zamanda klinik kullanım için uygun hale geldi ve 30 dakikalık bir tedavinin ciltte TRPV1 içeren nöronların gerilemesine neden olarak 3 aya kadar analjezi sağlayabileceğini gösteren destekleyici kanıtlar var. Halihazırda, bu tedaviler, analjezik etkilerini sürdürmek için düzenli (nadiren de olsa) bir programa göre yeniden uygulanmalıdır.
Yağ asidi metabolitleri
Çoklu doymamış yağ asitlerinin belirli metabolitlerinin, hücreleri TRPV1'e bağımlı bir şekilde uyardığı gösterilmiştir. 13( S )-hidroksi-9Z,11E-oktadekadienoik asit (13(S)-HODE), 13( R )-hidroksi-9Z,11E-oktadekadienoik asit (13( R )-HODE dahil olmak üzere linoleik asit metabolitleri , 9( S )-hidroksi-10(E),12(Z)-oktadekadienoik asit (9( S )-HODE), 9( R )-hidroksi-10(E),12(Z)-oktadekadienoik asit (9( R )-HODE) ve bunların ilgili keto analogları, 13-oxoODE ve 9-oxoODE ( Doğrudan eylemler hakkındaki 13-HODE ve 9-HODE bölümlerine bakın), periferik ve merkezi fare ağrı algılama nöronlarını aktive eder. örneğin en güçlü olanı 9( S )-HODE olan, en az 10 mikromol/litre veya TRPV1'i kemirgen nöronlarında aktive etmek için 10 nanomol/litreden daha fazla fizyolojik konsantrasyon gerektiren metabolitler.Bu metabolitlerin TRPV1-bağımlılığı aktiviteleri, TPRV1 ile doğrudan etkileşimlerini yansıtıyor gibi görünmektedir.Anandamide kıyasla TRPV1'in nispeten zayıf agonistleri olmasına rağmen, bu linoleat metabolitlerinin, kemirgenlerde ağrı algısına aracılık etmede TRPV1 aracılığıyla etki ettiği ve solunum yolu epitel hücrelerinde hasara neden olur ve böylece farelerde ve dolayısıyla muhtemelen insanlarda astım hastalığına katkıda bulunur . 20-hidroksi-5 Z ,8 Z ,11 Z ,14 Z- eikosatetraenoik asit (bakınız 20-Hidroksiyeikosatetraenoik asit ) ve 12( S )-hidroperoksi-5 Z ,8 Z ,10 E ,12 S dahil olmak üzere belirli araşidonik asit metabolitleri ,14 Z- eikosatetraenoik asit (12(S)-HpETE), 12( S )-hidroksi-5 Z ,8 Z ,10 E ,12 S ,14 Z- eikosatetraenoik asit (12( S )-HETE (bakınız 12- HETE ), hepoksilin A3 (yani 8R/S-hidroksi-11,12-oksido-5Z,9E,14Z-eikosatrienoik asit) ve HxB3 (yani 10R/S-hidroksi-11,12-oksido-5Z,8Z,14Z- eikosatrienoik asit) benzer şekilde TRPV1'i aktive eder ve böylece dokunsal hiperaljezi ve allodiniye katkıda bulunabilir (bkz. Hepoxilin#Ağrı algısı ).
Fareler, kobay ve insan dokuları ve kobaylarda yapılan çalışmalar, başka bir araşidonik asit metaboliti olan Prostaglandin E2'nin , öksürük tepkilerini tetiklemek için prostaglandin EP3 G proteini ile eşleştirilmiş reseptörü aracılığıyla çalıştığını göstermektedir . Etki mekanizması , muhtemelen dolaylı bir mekanizma ile TRPV1 (aynı zamanda TRPA1 ) reseptörlerinin aktivasyonunu ve/veya hassaslaştırılmasını içerir . EP3 reseptöründeki (rs11209716) genetik polimorfizm , insanlarda ACE inhibitörünün neden olduğu öksürük ile ilişkilendirilmiştir .
Resolvin E1 (RvE1), RvD2 ( resolvinlere bakınız ), nöroprotektin D1 (NPD1) ve maresin 1 (Mar1), omega 3 yağ asitleri , eikosapentaenoik asit (RvE1 için) veya dokosaheksaenoik asit (RvD2, NPD1 ve Mar1 için) metabolitleridir. ). Bu metabolitler, hayvan modellerinde ve insanlarda çeşitli inflamatuar reaksiyonları ve hastalıkları çözme işlevi gören özelleşmiş proresolve mediatörler ( SPM'ler ) sınıfının üyeleridir . Bu SPM'ler ayrıca hayvan modellerinde çeşitli iltihaplanma temelli nedenlerden kaynaklanan ağrı algısını da azaltır. Ağrı kesici etkilerinin arkasındaki mekanizma, muhtemelen (en azından belirli durumlarda) nöronlar veya yakındaki mikroglia veya astrositlerde bulunan diğer reseptörleri aktive ettikleri dolaylı bir etki ile TRPV1'in inhibisyonunu içerir . CMKLR1 , GPR32 , FPR2 ve NMDA reseptörlerinin , bu SPM'lerin TRPV1'i ve dolayısıyla ağrı algısını aşağı regüle etmek için çalıştığı reseptörler olduğu öne sürülmüştür .
Yağ asidi konjugatları
N-arakidonoil dopamin kapsaisin yapısal olarak benzer, insan CNS'de bir endokanabinoid Bulunan, bir ile TRPV1 kanalını aktive EC 50 , yaklaşık 50 nM.
Başka bir endojen agonist olan N-Oleyil-dopamin, 36 Nm'lik bir Ki ile insan VR1'ine bağlanır.
Başka bir endokannabinoid anandamidin de TRPV1 reseptörleri üzerinde etkili olduğu gösterilmiştir.
AM404 -an aktif metabolit arasında parasetamol bir şekilde karşılık vermektedir -yani (Asetaminofen olarak da bilinir) anandamid geri alım inhibitörü ve COX inhibitörü, aynı zamanda etkili bir TRPV1 agonisti olarak görev yapar.
Bitki biyosentezli kannabinoid kannabidiol ayrıca TRPV1 reseptörlerinin "doğrudan veya dolaylı aktivasyonunu" gösterir. TRPV1 , sırasıyla duyusal ve beyin nöronlarında CB1 reseptörleri ve CB2 reseptörleri ile aynı yerde bulunur ve CBN , CBG , CBC , THCV ve CBDV gibi diğer bitki kannabinoidleri de bu iyon kanalının agonistleridir . Myrcene gibi Cannabis sekonder metabolomunun kannabinoid olmayan bileşenlerinin TRPV1'i aktive ettiğine dair kanıtlar da vardır .
Merkezi sinir sistemi
TRPV1 ayrıca merkezi sinir sisteminde yüksek seviyelerde ifade edilir ve sadece ağrı tedavisi için değil, aynı zamanda anksiyete gibi diğer durumlar için de bir hedef olarak önerilmiştir . Ayrıca, TRPV1'in hipokampusta uzun süreli sinaptik depresyona (LTD) aracılık ettiği görülmektedir . LTD, hafıza oluşumuna yardımcı olan uzun vadeli güçlenmenin (LTP) aksine, yeni hatıralar oluşturma yeteneğinde bir azalma ile bağlantılıdır . Birçok sinapsta meydana gelen dinamik bir LTD ve LTP modeli, hafıza oluşumu için bir kod sağlar. Uzun süreli depresyon ve ardından azaltılmış aktivite ile sinapsların budanması, hafıza oluşumunun önemli bir yönüdür. Sıçan beyin dilimlerinde, TRPV1'in ısı veya kapsaisin ile aktivasyonu LTD'yi indüklerken kapsazepin, kapsaisinin LTD'yi indükleme yeteneğini bloke etti. Beyin sapında (soliter sistem çekirdeği), TRPV1, miyelinsiz kraniyal visseral afferentlerden asenkron ve spontan glutamat salınımını kontrol eder - normal sıcaklıklarda aktif olan ve dolayısıyla ağrılı ısıdaki TRPV1 tepkilerinden oldukça farklı olan salınım süreçleri. Bu nedenle, belki epilepsi tedavisi olarak merkezi sinir sisteminde TRPV1'in modüle edilmesinde terapötik potansiyel olabilir (TRPV1 zaten periferik sinir sisteminde ağrının giderilmesi için bir hedeftir).
Etkileşimler
TRPV1'in aşağıdakilerle etkileşime girdiği gösterilmiştir :
keşif
Dorsal kök gangliyon (DRG) nöronları , memelilerin kapsaisin tarafından aktive edilebilecek bir ısıya-hassas iyon kanalı eksprese ettiği bilinen. Bu nedenle David Julius'un araştırma grubu, dorsal kök ganglion nöronlarında eksprese edilen genlerden oluşan bir cDNA kütüphanesi oluşturdu , HEK 293 hücrelerinde klonları eksprese etti ve kapsaisine kalsiyum akışı ile yanıt veren (HEK-293'ün normalde yapmadığı) hücreleri aradı. . Birkaç tur tarama ve kitaplığın bölünmesinden sonra, TRPV1 kanalını kodlayan tek bir klon nihayet 1997'de tanımlandı. Bu, tanımlanan ilk TRPV kanalıydı. Julius, keşfinden dolayı 2021 Nobel Fizyoloji veya Tıp ödülüne layık görüldü.
Ayrıca bakınız
- kapsaisin
- kapsinoidler
- Vanilloidler
- vanillotoksin
- kannabinoid reseptörü
- TRPV1 antagonistlerinin keşfi ve geliştirilmesi
- rutenyum kırmızısı
- termoreseptör
- Kategori:Somatosensoriyel sistem
Referanslar
daha fazla okuma
- Premkumar LS, Ahern GP (Aralık 2000). "Protein kinaz C ile vanilloid reseptör kanal aktivitesinin uyarılması". Doğa . 408 (6815): 985-90. Bibcode : 2000Natur.408..985P . doi : 10.1038/35050121 . PMID 11140687 . S2CID 4372628 .
- Immke DC, Gavva NR (Ekim 2006). "TRPV1 reseptörü ve nosisepsiyon". Hücre ve Gelişim Biyolojisi Seminerleri . 17 (5): 582–91. doi : 10.1016/j.semcdb.2006.09.004 . PMID 17196854 .
- Heiner I, Eisfeld J, Lückhoff A (2004). "Nötrofil granülositlerde TRP kanallarının rolü ve düzenlenmesi". Hücre Kalsiyumu . 33 (5–6): 533–40. doi : 10.1016/S0143-4160(03)00058-7 . PMID 12765698 .
- Geppetti P, Trevisani M (Nisan 2004). "Vanilloid reseptörünün aktivasyonu ve duyarlılığı: gastrointestinal inflamasyon ve fonksiyondaki rolü" . İngiliz Farmakoloji Dergisi . 141 (8): 1313–20. doi : 10.1038/sj.bjp.0705768 . PMC 1574908 . PMID 15051629 .
- Szallasi A, Cruz F, Geppetti P (Kasım 2006). "TRPV1: yeni analjezik ilaçlar için terapötik bir hedef?". Moleküler Tıpta Eğilimler . 12 (11): 545-54. doi : 10.1016/j.molmed.2006.09.001 . PMID 16996800 .
- Pingle SC, Matta JA, Ahern GP (2007). "Kapsaisin reseptörü: TRPV1 rastgele bir TRP kanalı". Geçici Reseptör Potansiyeli (TRP) Kanalları . Handb Exp Pharmacol . Deneysel Farmakoloji El Kitabı. 179 . s. 155–71. doi : 10.1007/978-3-540-34891-7_9 . ISBN'si 978-3-540-34889-4. PMID 17217056 .
- Liddle RA (Ağustos 2007). "Pankreatitte Geçici Reseptör Potansiyel Vanilloid 1 (TRPV1) kanallarının rolü" . Biochimica et Biophysica Açta (BBA) - Hastalığın Moleküler Temeli . 1772 (8): 869-78. doi : 10.1016/j.bbadis.2007.02.012 . PMC 1995747 . PMID 17428642 .
Dış bağlantılar
- ABD Ulusal Tıp Kütüphanesi Tıbbi Konu Başlıklarında (MeSH) vanilloid+reseptörler
- Uygun yapısal bilginin her genel PDB için Uniprot : O35433 (Fare geçici reseptör potansiyel katyon kanalı alt ailesi V 1) en PDBe-KB .