Tümör nekroz faktörü - Tumor necrosis factor
Tümör nekroz faktörü ( TNF , kaşeksin veya kaşektin ; genellikle tümör nekroz faktörü alfa veya TNF-a olarak adlandırılır ) bir sitokindir – bağışıklık sistemi tarafından hücre sinyali için kullanılan küçük bir proteindir . Makrofajlar (belirli beyaz kan hücreleri ) bir enfeksiyon tespit ederse , inflamatuar yanıtın bir parçası olarak diğer bağışıklık sistemi hücrelerini uyarmak için TNF salgılarlar . TNF, homolog bir TNF alanına sahip çeşitli transmembran proteinlerinden oluşan TNF süper ailesinin bir üyesidir .
TNF sinyali iki reseptör aracılığıyla gerçekleşir: TNFR1 ve TNFR2. TNFR1 çoğu hücre tipinde yapısal olarak eksprese edilirken, TNFR2 esas olarak endotelyal, epitelyal ve immün hücrelerin alt kümeleriyle sınırlıdır. TNF1 sinyali proinflamatuar ve apoptotik olma eğilimindeyken , TNFR2 sinyali antiinflamatuardır ve hücre proliferasyonunu destekler . TNFR1 sinyalinin baskılanması otoimmün hastalığın tedavisi için önemliyken, TNFR2 sinyali yara iyileşmesini destekler .
TNF-a, bir transmembran formu (mTNF-a) ve çözünür bir form (sTNF-a) olarak bulunur. sTNF-a, mTNF-a'nın enzimatik bölünmesinden kaynaklanır. mTNF-α esas olarak hücreden hücreye temas yoluyla doku reseptörleri ile etkileşime girdiği monosit/makrofajlarda bulunur. sTNF-a seçici olarak TNFR1'e bağlanırken mTNF-a hem TNFR1 hem de TNFR2'ye bağlanır. TNFR1'e TNF-a bağlanması geri döndürülemezken, TNFR2'ye bağlanma tersine çevrilebilir.
TNF'nin birincil rolü, bağışıklık hücrelerinin düzenlenmesindedir . TNF, endojen bir pirojen olarak ateş , apoptotik hücre ölümü , kaşeksi ve inflamasyonu indükleyebilir , tümörijenezi ve viral replikasyonu inhibe edebilir ve IL-1 ve IL-6 üreten hücreler yoluyla sepsise yanıt verebilir . TNF üretiminin düzensizliği, Alzheimer hastalığı , kanser , majör depresyon , sedef hastalığı ve inflamatuar bağırsak hastalığı (IBD) dahil olmak üzere çeşitli insan hastalıklarına dahil edilmiştir . Tartışmalı olmasına rağmen, bazı çalışmalar depresyon ve IBD'yi artan TNF seviyelerine bağladı.
Tasonermin adı altında TNF, bazı kanserlerin tedavisinde immün sistemi uyarıcı bir ilaç olarak kullanılmaktadır . TNF'nin etkisine karşı koyan ilaçlar, örneğin romatoid artrit gibi çeşitli iltihaplı hastalıkların tedavisinde kullanılır .
Bazı kanserler aşırı TNF üretimine neden olabilir. TNF, hem sekonder hiperkalsemiye neden olmada hem de aşırı üretimin ilişkili olduğu kanserlerde paratiroid hormonuna paraleldir .
keşif
İn vivo olarak bağışıklık sisteminin bir anti-tümör tepkisi teorisi , doktor William B. Coley tarafından kabul edildi . 1968'de Irvine , California Üniversitesi'nden Gale A Granger, lenfositler tarafından üretilen sitotoksik bir faktör bildirdi ve buna lenfotoksin (LT) adını verdi . Bu keşif için övgü , aynı ay içinde yayınlanan bir dizi arka arkaya makalesinde aynı aktiviteyi bildiren Yale Üniversitesi'nden Nancy H. Ruddle tarafından paylaşılıyor . Daha sonra, 1975 yılında Memorial Sloan-Kettering Cancer Center , New York'tan Lloyd J. Old , makrofajlar tarafından üretilen başka bir sitotoksik faktör bildirdi ve buna tümör nekroz faktörü (TNF) adını verdi . Her iki faktör de fare fibrosarkom L-929 hücrelerini öldürme yeteneklerine göre tanımlanmıştır . Bu kavramlar 1981'de, Avustralya Ulusal Üniversitesi'nden Ian A. Clark'ın , Old'un grubundaki Elizabeth Carswell ile işbirliği içinde , dizileme öncesi dönem verileriyle çalışarak, aşırı TNF üretiminin sıtma hastalığına ve endotoksine neden olduğu sonucuna vardığında, sistemik hastalıkları da kapsayacak şekilde genişletildi. zehirlenme.
CDNA'lar LT ve TNF kodlayan edildi klonlanmış 1984 ve benzer olduğu ortaya çıkarılmıştır. TNF'nin reseptörüne bağlanması ve LT tarafından yer değiştirmesi , iki faktör arasındaki fonksiyonel homolojiyi doğruladı . TNF ve LT'nin sıralı ve fonksiyonel homolojisi, TNF'nin TNFa ve LT'nin TNFβ olarak yeniden adlandırılmasına yol açtı . 1985 yılında Bruce A. Beutler ve Anthony Cerami , kaşektinin ( kaşeksiyi indükleyen bir hormon ) aslında TNF olduğunu keşfettiler . Daha sonra TNF'yi ölümcül endotoksin zehirlenmesinin bir aracısı olarak tanımladılar . Kevin J. Tracey ve Cerami, ölümcül septik şokta TNF'nin anahtar aracı rolünü keşfettiler ve monoklonal anti-TNF antikorlarının terapötik etkilerini belirlediler.
Mark Mattson Laboratuvarı'nda yapılan araştırmalar , TNF'nin , antioksidan enzimlerin ve Bcl-2'nin ekspresyonunu indükleyen transkripsiyon faktörü NF-κB'nin aktivasyonunu içeren bir mekanizma ile nöronların ölümünü/ apoptozunu önleyebildiğini göstermiştir .
Gen
İnsan TNF geni 1985'te klonlanmıştır. Kromozom 6p 21.3 ile eşleşir , yaklaşık 3 kilobaz kapsar ve 4 ekzon içerir . Son ekson, lenfotoksin alfa ile benzerlik gösterir (LTA, bir zamanlar TNF-β olarak adlandırılır). Üç asal çevrilmemiş bölge TNF (3'-UTR) bir içeriyor AU-zengin elemanı (ARE).
Yapı
TNF, esas olarak , stabil homotrimerlerde düzenlenen 233- amino asit uzunluğunda tip II transmembran proteini olarak üretilir . Bu membrana entegre formdan, çözünür homotrimerik sitokin (sTNF), metaloproteaz TNF alfa dönüştürücü enzim (TACE, ADAM17 olarak da adlandırılır ) tarafından proteolitik bölünme yoluyla salınır . Çözünür 51 kDa trimerik sTNF, nanomolar aralığın altındaki konsantrasyonlarda ayrışma eğilimi gösterir ve böylece biyoaktivitesini kaybeder. İnsan TNF'sinin salgılanan formu üçgen piramit şeklini alır ve yaklaşık 17 kDa ağırlığındadır. Hem salgılanan hem de zara bağlı formlar biyolojik olarak aktiftir, ancak her birinin spesifik işlevleri tartışmalıdır. Ancak, her iki form da örtüşen ve farklı biyolojik aktivitelere sahiptir.
Yaygın ev faresi TNF'si ve insan TNF'si yapısal olarak farklıdır. 17- kilodalton (kDa) TNF protomerler (185 amino asit uzunluğunda), iki oluşur anti-paralel β-plili tabakanın ile anti-paralel β-şerit TNF ailesinin için tipik bir 'jel silindir' β-yapı oluşturan, aynı zamanda bulunan viral kapsid proteinleri .
Telefon sinyali
TNF, TNFR1 ( TNF reseptör tip 1; CD120a; p55/60) ve TNFR2 (TNF reseptör tip 2; CD120b; p75/80) olmak üzere iki reseptöre bağlanabilir . TNFR1 55-kDa'dır ve TNFR2 75-kDa'dır. TNFR1 çoğu dokuda eksprese edilir ve TNF'nin hem membrana bağlı hem de çözünür trimerik formları tarafından tamamen aktive edilebilirken, TNFR2 tipik olarak bağışıklık sisteminin hücrelerinde bulunur ve TNF homotrimerinin membrana bağlı formuna yanıt verir. TNF sinyalleşmesine ilişkin çoğu bilgi TNFR1'den türetildiği için TNFR2'nin rolü muhtemelen hafife alınmaktadır. En azından kısmen TNFR2'nin hücre içi ölüm alanı olmadığı için nöroprotektif özellikler gösterir .
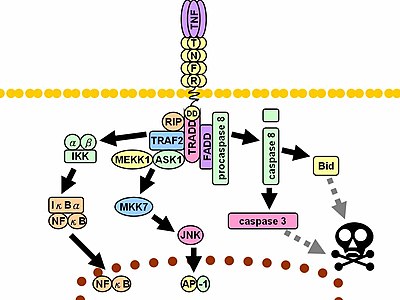
Bunların ile temas üzerine bir ligand , TNF reseptörleri aynı zamanda uçları TNF monomerler arasında oluşturulan oluklara uyan, trimerler oluşturur. Bu bağlanma, reseptörde konformasyonel bir değişikliğin meydana gelmesine neden olarak, inhibitör protein SODD'nin hücre içi ölüm alanından ayrılmasına yol açar. Bu ayrışma, bağdaştırıcı protein TRADD'nin , sonraki protein bağlanması için bir platform görevi görerek ölüm alanına bağlanmasını sağlar. TRADD bağlanmasını takiben üç yol başlatılabilir.
- NF-κB'nin aktivasyonu : TRADD, TRAF2 ve RIP'yi işe alır . TRAF2 da çok-bileşenli protein acemi kinaz IKK serin-treonin sağlayan kinaz etkinleştirmek için RIP. Normalde NF-κB'ye bağlanan ve translokasyonunu inhibe eden inhibitör bir protein olan IκBa , IKK tarafından fosforile edilir ve ardından bozunarak NF- KB'yi serbest bırakır. NF-KB, bir heterodimerik bir transkripsiyon faktörü edilene yer değiştirir çekirdeği aracılık ettiği ve hücre hayatta kalması ve proliferasyonu yer alan proteinlerin geniş bir dizi transkripsiyon inflamatuar yanıt , ve anti- apoptotik faktörler.
- MAPK yollarının aktivasyonu : Üç ana MAPK kademesinden TNF, stresle ilişkili JNK grubunun güçlü bir aktivasyonunu indükler , p38- MAPK'nın orta derecede tepkisini uyandırır ve klasik ERK'lerin minimum aktivasyonundan sorumludur . TRAF2 / Rac aktive JNK üst indükleyen kinazlar arasında MLK2 / MLK3 , TAK1 , MEKK1 ve ASK1 (sırasıyla, doğrudan ya da GCKs ve Trx aracılığıyla). SRC- Vav- Rac eksene MLK2 / MLK3 harekete geçirir ve bu kinazlar fosforile MKK7 sonra aktive JNK . JNK çekirdeğe yer değiştirir ve c-Jun ve ATF2 gibi transkripsiyon faktörlerini aktive eder . JNK yoluna karışır hücre farklılaşması , proliferasyon ve genellikle orantılı olduğu apoptotik .
- Ölüm sinyalinin uyarılması: TNFR üst ailesinin tüm ölüm alanı içeren üyeleri gibi, TNFR1 de ölüm sinyallemesinde yer alır. Bununla birlikte, TNF'nin neden olduğu hücre ölümü, iltihaplanma sürecindeki ezici işlevlerine kıyasla sadece küçük bir rol oynar. Ölüme neden olma yeteneği, diğer aile üyelerine ( Fas gibi ) kıyasla zayıftır ve sıklıkla NF-κB'nin antiapoptotik etkileri tarafından maskelenir . Bununla birlikte, TRADD bağlanan FADD sonra acemi sistein proteaz kaspaz-8 . Yüksek bir kaspaz- 8 konsantrasyonu , otoproteolitik aktivasyonunu ve ardından efektör kaspazların bölünmesini indükleyerek hücre apoptozisine yol açar .
Yukarıdaki yolların aracılık ettiği sayısız ve çoğu zaman çatışan etkiler, kapsamlı çapraz konuşmanın varlığına işaret eder. Örneğin, NF-KB transkripsiyonunu arttıran Cı-FLIP , Bcl-2 ve cIAP1 / cIAP2 , ölüm sinyalleme müdahale önleyici proteinler. Öte yandan, aktive edilmiş kaspazlar, RIP, IKK ve NF-KB'nin kendisinin alt birimleri dahil olmak üzere NF-KB yolunun çeşitli bileşenlerini parçalar. Hücre tipi, diğer sitokinlerin aynı anda uyarılması veya reaktif oksijen türlerinin (ROS) miktarı gibi diğer faktörler, dengeyi bir yol veya diğeri lehine değiştirebilir. Bu tür karmaşık sinyalizasyon, TNF salındığında, çok çeşitli işlevlere ve koşullara sahip çeşitli hücrelerin hepsinin iltihaplanmaya uygun şekilde yanıt verebilmesini sağlar . Her iki protein molekülü, tümör nekroz faktörü alfa ve keratin 17, oral submuköz fibroz durumunda ilişkili görünmektedir.
Hayvan modellerinde TNF, otoreaktif T hücrelerini seçici olarak öldürür .
Ayrıca TNF-a sinyalinin hücrelerde proinflamatuar yanıtların kalıcı olarak artmasıyla sonuçlanan aşağı yönde epigenetik modifikasyonları tetiklediğine dair kanıtlar da vardır.
enzim regülasyonu
Bu protein , allosterik düzenlemenin morfein modelini kullanabilir .
fizyoloji
TNF'nin öncelikle makrofajlar tarafından üretildiği düşünülüyordu , ancak lenfoid hücreler, mast hücreleri , endotelyal hücreler , kardiyak miyositler , yağ dokusu , fibroblastlar ve nöronlar dahil olmak üzere çok çeşitli hücre tipleri tarafından da üretiliyor . Lipopolisakkarit , diğer bakteriyel ürünler ve interlökin-1'e (IL-1) yanıt olarak büyük miktarlarda TNF salınır . Deride, mast hücreleri, inflamatuar uyaran (örn., LPS) üzerine salınabilen önceden oluşturulmuş TNF'nin baskın kaynağı gibi görünmektedir.
Genellikle IL-1 ve interlökin-6 (IL-6) ile birlikte çeşitli organ sistemleri üzerinde bir dizi etkiye sahiptir :
- Açık hipotalamus :
- Uyarılması , hipotalamik-hipofiz-böbrek üstü bezi ekseninin salınımını uyararak kortikotropin salan hormon (CRH)
- iştahı bastırmak
- Ateş
- Açık karaciğer : uyarıcı akut faz tepkisini bir artışa yol açan, C-reaktif protein ve diğer aracıların. Ayrıca , insülin sinyalini bozan insülin reseptör substratı-1'in (IRS-1) serin fosforilasyonunu teşvik ederek insülin direncini indükler.
- Nötrofiller için güçlü bir kemo-çekicidir ve endotel hücreleri üzerindeki yapışma moleküllerinin ekspresyonunu teşvik ederek nötrofillerin göç etmesine yardımcı olur .
- Makrofajlar üzerinde: fagositozu ve IL-1 oksidanlarının ve inflamatuar lipid prostaglandin E2'nin (PGE 2 ) üretimini uyarır
- Diğer dokularda: artan insülin direnci . TNF, insülin reseptörü serin kalıntılarını fosforile ederek sinyal iletimini bloke eder.
- Metabolizma ve gıda alımı üzerine: acı tat algısını düzenler.
TNF konsantrasyonunda lokal bir artış, iltihaplanmanın başlıca belirtilerinin ortaya çıkmasına neden olacaktır: ısı, şişme, kızarıklık, ağrı ve fonksiyon kaybı.
Yüksek konsantrasyonlarda TNF, şok benzeri semptomlara neden olurken , düşük konsantrasyonlarda TNF'ye uzun süre maruz kalmak , bir tükenme sendromu olan kaşeksi ile sonuçlanabilir . Bu, örneğin kanser hastalarında bulunabilir.
Said ve ark. TNF'nin, PD-1'in PD-L tarafından bağlanmasından sonra monositler tarafından IL-10 üretimine yol açan monositler üzerindeki PD-1 seviyelerini yukarı regüle ederek CD4 T-hücre genişlemesinin ve fonksiyonunun IL-10'a bağlı bir inhibisyonuna neden olduğunu gösterdi.
Pedersen ve ark. sepsise yanıt olarak TNF artışının egzersizle indüklenen miyokin üretimi tarafından inhibe edildiğini gösterir . Akut egzersizin gerçek bir anti-inflamatuar yanıtı indükleyip indüklemediğini incelemek için, sağlıklı gönüllülere düşük dozda E. coli endotoksininin uygulandığı bir 'düşük dereceli inflamasyon' modeli oluşturuldu. endotoksin uygulaması. Dinlenen deneklerde endotoksin, dolaşımdaki TNF seviyelerinde 2 ila 3 kat artışa neden oldu. Buna karşılık, denekler 3 saatlik ergometre döngüsü gerçekleştirdiğinde ve 2,5 saatte endotoksin bolusu aldığında, TNF yanıtı tamamen körelmiştir. Bu çalışma, akut egzersizin TNF üretimini engelleyebileceğine dair bazı kanıtlar sunmaktadır.
Beyinde TNF, eksitotoksisiteye karşı koruma sağlayabilir . TNF sinapsları güçlendirir. Nöronlardaki TNF, hayatta kalmalarını desteklerken, makrofajlar ve mikroglialardaki TNF, apoptozu indükleyen nörotoksinlerle sonuçlanır.
TNF-α ve IL-6 konsantrasyonları obezitede yükselir . TNF-a'ya karşı monoklonal antikor , obezitede azalmadan ziyade artışlarla ilişkilidir, bu da inflamasyonun obezitenin nedeni değil sonucu olduğunu gösterir.
Farmakoloji
TNF, romatoid artrit , ankilozan spondilit , inflamatuar bağırsak hastalığı , sedef hastalığı , hidradenitis süpürativa ve refrakter astım gibi otoimmün bozukluklarla ilişkili klinik sorunların çoğuna neden olan inflamatuar yanıtı destekler . Bu bozukluklar bazen bir TNF inhibitörü kullanılarak tedavi edilir . Bu inhibisyon, doğrudan TNF'ye bağlanan infliksimab (Remicade), adalimumab (Humira), sertolizumab pegol (Cimzia) gibi bir monoklonal antikorla veya TNF'ye daha fazla bağlanan etanercept (Enbrel) gibi bir tuzak dolaşımdaki reseptör füzyon proteini ile elde edilebilir. TNFR'den daha yakınlık.
Öte yandan, TNF inhibitörleri ile tedavi edilen bazı hastalarda, hastalıklarının alevlenmesi veya yeni bir otoimmünite başlangıcı gelişir. TNF'nin de immünosupresif bir yönü var gibi görünüyor. Olası bir mekanizma için bir açıklama, TNF'nin tümör nekroz faktör reseptörü 2'ye (TNFR2) bağlanması nedeniyle düzenleyici T hücreleri (Treg'ler) üzerinde olumlu bir etkiye sahip olduğu gözlemidir.
Anti-TNF tedavisi, kanser tedavisinde sadece mütevazı etkiler göstermiştir. Tedavi renal hücre karsinomu olan infliksimab bazı hastalarda uzun süre hastalık stabilizasyonu ile sonuçlanmıştır. Etanercept , IL-6 ve CCL2'nin aşağı regülasyonu yoluyla belirli hastalarda uzun süreli hastalık stabilizasyonu gösteren meme kanseri ve yumurtalık kanseri hastalarının tedavisi için test edilmiştir . Öte yandan, ilerlemiş pankreas kanseri olan hastaları tedavi etmek için gemsitabine infliksimab veya etanersept eklenmesi , plasebo ile karşılaştırıldığında etkinlik farklılıkları ile ilişkili değildi.
Etkileşimler
TNF'nin TNFRSF1A ile etkileşime girdiği gösterilmiştir .
isimlendirme
Çünkü LTa artık önceki gen sembolü olarak, TNFp, TNFa'ya olarak anılır gösterildiği gibi, artık sadece, TNF denir HGNC (HUGO Gen Nomenklatür Komitesi) veritabanı.
Referanslar
Dış bağlantılar
- "Tasonermin" . İlaç Bilgi Portalı . ABD Ulusal Tıp Kütüphanesi.
- "Tümör Nekroz Faktörü-alfa" . İlaç Bilgi Portalı . ABD Ulusal Tıp Kütüphanesi.
- ABD Ulusal Tıp Kütüphanesinde Tümör Nekroz Faktörü-alfa Tıbbi Konu Başlıkları (MeSH)
- Uygun yapısal bilginin her genel PDB için Uniprot : P01375 (tümör nekroz faktörü) de PDBe-KB .