Rimonabant - Rimonabant
 | |
 | |
| Klinik veriler | |
|---|---|
| AHFS / Drugs.com | Tüketici İlaç Bilgileri |
| Lisans verileri | |
| Gebelik kategorisi |
|
Yönetim yolları |
Oral |
| ATC kodu | |
| Hukuki durum | |
| Hukuki durum | |
| Farmakokinetik veriler | |
| Biyoyararlanım | Belirlenmemiş |
| Protein bağlama | Yaklaşık% 100 |
| Metabolizma | Hepatik , CYP3A4 dahil |
| Eliminasyon yarı ömrü | Değişken: 6 ila 9 gün, normal BMI ile 16 gün, eğer BMI> 30 ise |
| Boşaltım | Dışkı (% 86) ve böbrek (% 3) |
| Tanımlayıcılar | |
| |
| CAS numarası | |
| PubChem Müşteri Kimliği | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| CompTox Kontrol Paneli ( EPA ) | |
| ECHA Bilgi Kartı |
100.210.978 |
| Kimyasal ve fiziksel veriler | |
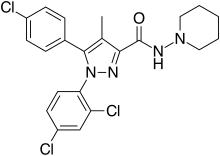
| Formül | C 22 H 21 Cl 3 N 4 O |
| Molar kütle | 463,79 g · mol −1 |
| 3B modeli ( JSmol ) | |
| |
| |
| (Doğrulayın) | |
Rimonabant (olarak da bilinen SR141716 ; ticari isimler Acomplia , Zimulti bir olan) anorectic obeziteye karşı ilaç ilk olarak 2006 yılında Avrupa'da onaylandı fakat ciddi psikiyatrik yan etkilere 2008 yılında dünya çapında geri çekildi; Birleşik Devletler'de asla onaylanmadı. Rimonabant, kanabinoid reseptörü CB 1 için ters bir agonisttir ve bu sınıfta onaylanan ilk ilaçtır.
Tarih
Rimonabant, seçici bir CB 1 reseptör blokeridir ve Sanofi-Aventis tarafından keşfedilmiş ve geliştirilmiştir ;
21 Haziran 2006 tarihinde, Avrupa Komisyonu rimonabantın o zamanki 25 üyesi olan Avrupa Birliği'nde vücut kitle indeksi (BMI) 30 kg / m2'den büyük olan hastalar için diyet ve egzersizle birlikte kullanılmak üzere reçeteli bir ilaç olarak satışını onayladı. 2 27 kg / m den BMI daha sonra ile veya hastalarda 2 , tip 2 olarak ilişkili risk faktörleri olan diyabet ya da dislipidemi . Kendi sınıfında dünyanın herhangi bir yerinde onaylanan bir ilkti.
Rimonabant, 2005 yılında Amerika Birleşik Devletleri'nde onay için Gıda ve İlaç Dairesine (FDA) sunulmuştur ; 2007'de FDA'nın Endokrin ve Metabolik İlaçlar Danışma Komitesi (EMDAC), Sanofi-Aventis'in rimonabant'ın güvenliğini gösteremediği sonucuna vardı ve anti-obezite tedavisini onay için önermeye karşı oy kullandı ve iki hafta sonra şirket başvuruyu geri çekti.
İlaç, Nisan 2007'de Brezilya'da onaylandı.
Ekim 2008'de, Avrupa İlaç Ajansı , Beşeri Tıbbi Ürünler Komitesi'nin (CHMP) intihar da dahil olmak üzere ciddi psikiyatrik problemler nedeniyle Acomplia risklerinin faydalarından daha ağır bastığını belirlemesinin ardından Acomplia'nın askıya alınmasını tavsiye etti. Kasım 2008'de Brezilya'daki bir danışma komitesi de askıya almayı önerdi ve o ay Sanofi-Aventis ilacın dünya çapında satışını askıya aldı. EMA onayı Ocak 2009'da geri çekildi. 2009'da Hindistan ilacın üretimini ve satışını yasakladı.
Yan etkiler
Düzenleyici makamlara sunulan klinik araştırmalardan elde edilen veriler, rimonabant'ın deneklerin% 10'una kadar depresif bozukluklara veya duygudurum değişikliklerine ve yaklaşık% 1'inde intihar düşüncesine neden olduğunu ve Avrupa'da depresif veya intihar eğilimli kişiler dahil olmak üzere herhangi bir psikiyatrik bozukluğu olan kişiler için kontrendike olduğunu gösterdi .
Ek olarak, mide bulantısı ve üst solunum yolu enfeksiyonları çok yaygın yan etkilerdir (insanların% 10'undan fazlasında meydana gelir); yaygın yan etkiler (insanların% 1 ila% 10'unda görülür) mide iltihabı , anksiyete, sinirlilik, uykusuzluk ve diğer uyku bozuklukları, sıcak basması, ishal, kusma, kuru veya kaşıntılı cilt, tendinit, kas krampları ve spazmları, yorgunluk, grip benzeri semptomlar ve artan düşme riski.
FDA'nın danışma komitesi, hayvan verilerine dayanarak, CNS toksisitesine ve özellikle nöbetlere ilişkin terapötik pencerenin neredeyse hiç yokmuş gibi göründüğüne dair endişeleri dile getirdi ; Hayvanlarda nöbetlere neden olan terapötik doz ve doz aynı göründü.
EMA pazarlama sonrası gözetim verilerini incelediğinde, rimonabant alan kişilerde psikiyatrik bozukluk riskinin iki katına çıktığını buldu.
Kimya
Rimonabant'ın kimyasal sentezi şu şekilde açıklanmaktadır:
Araştırma
Düzenleyici makamlara sunulan verileri oluşturan obezite ile ilgili klinik çalışmaların yanı sıra, rimonabant ayrıca diyabet, ateroskleroz ve sigarayı bırakma gibi diğer durumlar için potansiyel bir tedavi olarak klinik çalışmalarda incelenmiştir.

