Nörofilament - Neurofilament
| NF-L düşük moleküler ağırlıklı nörofilament proteini | |||||||
|---|---|---|---|---|---|---|---|
| tanımlayıcılar | |||||||
| Sembol | NEFL | ||||||
| NCBI geni | 4747 | ||||||
| HGNC | 7739 | ||||||
| OMIM | 162280 | ||||||
| Referans Sırası | NM_006158 | ||||||
| UniProt | P07196 | ||||||
| Diğer veri | |||||||
| yer | Chr. 8 p21 | ||||||
| |||||||
| NF-M orta moleküler ağırlıklı nörofilament proteini | |||||||
|---|---|---|---|---|---|---|---|
| tanımlayıcılar | |||||||
| Sembol | NEFM | ||||||
| Alt. semboller | NEF3 | ||||||
| NCBI geni | 4741 | ||||||
| HGNC | 7734 | ||||||
| OMIM | 162250 | ||||||
| Referans Sırası | NM_005382 | ||||||
| UniProt | P07197 | ||||||
| Diğer veri | |||||||
| yer | Chr. 8 p21 | ||||||
| |||||||
| NF-H yüksek moleküler ağırlıklı nörofilament proteini | |||||||
|---|---|---|---|---|---|---|---|
| tanımlayıcılar | |||||||
| Sembol | NEFH | ||||||
| NCBI geni | 4744 | ||||||
| HGNC | 7737 | ||||||
| OMIM | 162230 | ||||||
| Referans Sırası | NM_021076 | ||||||
| UniProt | P12036 | ||||||
| Diğer veri | |||||||
| yer | Chr. 22 q12.1-13.1 | ||||||
| |||||||
| Alfa-interneksin nöronal ara filament proteini | |||||||
|---|---|---|---|---|---|---|---|
| tanımlayıcılar | |||||||
| Sembol | İÇİNDE | ||||||
| Alt. semboller | NEF5 | ||||||
| NCBI geni | 9118 | ||||||
| HGNC | 6057 | ||||||
| OMIM | 605338 | ||||||
| Referans Sırası | NM_032727 | ||||||
| UniProt | Q5SYD2 | ||||||
| Diğer veri | |||||||
| yer | Chr. 10 q24 | ||||||
| |||||||
| Periferin nöronal ara filament proteini | |||||||
|---|---|---|---|---|---|---|---|
| tanımlayıcılar | |||||||
| Sembol | PRPH | ||||||
| Alt. semboller | NEF4 | ||||||
| NCBI geni | 5630 | ||||||
| HGNC | 9461 | ||||||
| OMIM | 170710 | ||||||
| Referans Sırası | NM_006262.3 | ||||||
| UniProt | P41219 | ||||||
| Diğer veri | |||||||
| yer | Chr. 12 q13.12 | ||||||
| |||||||
| Nestin nöronal kök hücre ara filament proteini | |||||||
|---|---|---|---|---|---|---|---|
| tanımlayıcılar | |||||||
| Sembol | NES | ||||||
| NCBI geni | 10763 | ||||||
| HGNC | 7756 | ||||||
| OMIM | 600915 | ||||||
| Referans Sırası | NP_006608 | ||||||
| UniProt | P48681 | ||||||
| Diğer veri | |||||||
| yer | Chr. 1 q23.1 | ||||||
| |||||||
Nörofilamentler ( NF ) , nöronların sitoplazmasında bulunan tip IV ara filamentler olarak sınıflandırılır . 10 nm çapında ve birçok mikrometre uzunluğunda protein polimerleridir. Birlikte mikrotübül (~ 25 nm) ve mikrofilamanlar (7 nm) nöronal oluşturan hücre iskeleti . Öncelikle aksonlar için yapısal destek sağlamak ve sinir iletim hızını etkileyen akson çapını düzenlemek için işlev gördüklerine inanılmaktadır . Nörofilamentleri oluşturan proteinler, gen organizasyonlarına ve protein yapılarına göre altı tipe ayrılan ara filament protein ailesinin üyeleridir. Tip I ve II, epitelde ifade edilen keratinlerdir . Tip III, vimentin , desmin , periferin ve glial fibril asidik protein (GFAP) proteinlerini içerir . Tip IV, nörofilament proteinleri L, M, H ve internexinden oluşur . Tip V nükleer laminlerden oluşur ve tip VI nestin proteininden oluşur . Tip IV ara filament genlerinin tümü , diğer ara filament gen dizilerinde bulunmayan iki benzersiz intronu paylaşır , bu da bir ilkel tip IV geninden ortak bir evrimsel köken olduğunu düşündürür.
Bir sinir hücresinin sitoplazmasında uzanan herhangi bir proteinli filament ayrıca bir nörofibril olarak adlandırılır . Bu isim, bazı nörodejeneratif hastalıkların nörofibriler yumaklarında kullanılır .
nörofilament proteinleri
Nörofilamentlerin protein bileşimi, farklı hayvan filumları arasında büyük farklılıklar gösterir. Çoğu memeli nörofilamentleri hakkında bilinmektedir. Tarihsel olarak, memeli nörofilamentlerinin başlangıçta nörofilament protein L (düşük moleküler ağırlık; NFL ), M (orta moleküler ağırlık; NFM ) ve H (yüksek moleküler ağırlık; NFH ) olarak adlandırılan sadece üç proteinden oluştuğu düşünülüyordu . Bu proteinler aksonal taşıma çalışmalarından keşfedildi ve genellikle "nörofilament üçlüsü" olarak anılır. Bununla birlikte, nörofilamentlerin interneksin proteinini de içerdiği ve periferik sinir sistemindeki nörofilamentlerin ayrıca protein periferini de içerebileceği artık açıktır. (bu, retinada ifade edilen periferin 2'den farklıdır ). Bu nedenle memeli nörofilamentleri, beş farklı proteine kadar heteropolimerdir: NfL, NfM, NfH, interneksin-alfa ve periferin. Beş nörofilament proteini, farklı sinir hücresi tiplerinde ve farklı gelişim aşamalarında farklı kombinasyonlarda bir araya gelebilir. Herhangi bir sinir hücresindeki nörofilamentlerin kesin bileşimi, o sırada hücredeki nörofilament proteinlerinin nispi ekspresyon seviyelerine bağlıdır. Örneğin, gelişen nöronlarda NfH ekspresyonu düşüktür ve miyelinli aksonları olan nöronlarda postnatal olarak artar. Yetişkin sinir sisteminde küçük miyelinsiz aksonlardaki nörofilamentler daha fazla periferin ve daha az NfH içerirken, büyük miyelinli aksonlardaki nörofilamentler daha fazla NfH ve daha az periferin içerir. Tip III ara filaman alt-birimi, vimentin , tip ile birlikte yetişkin gibi IV proteinleri, nöronlar ve birkaç çok olağandışı gelişen sinir olarak ifade edilir yatay nöronlar arasında retina .
| Protein | Amino asitler | NCBI Referans Sırası | Öngörülen moleküler kütle | Görünür moleküler kütle (SDS-PAGE) |
|---|---|---|---|---|
| periferin | 470 | NP_006253.2 | 53,7 kDa | ~56 kDa |
| internexin | 499 | NP_116116.1 | 55.4 kDa | ~66 kDa |
| Nörofilament proteini L | 543 | NP_006149.2 | 61,5 kDa | ~70 kDa |
| Nörofilament proteini M | 916 | NP_005373,2 | 102,5 kDa | ~160 kDa |
| Nörofilament proteini H | 1020 | NP_066554.2 | 111.9 kDA | ~200 kDa |
Üçlü proteinler, göreceli boyutlarına göre (düşük, orta, yüksek) adlandırılır. SDS-PAGE tarafından belirlenen her bir proteinin görünen moleküler kütlesi , amino dizisinden tahmin edilen kütleden daha büyüktür. Bu, bu proteinlerin anormal elektroforetik göçünden kaynaklanır ve yüksek yüklü amino asit içeriği ve yoğun fosforilasyon nedeniyle nörofilament proteinleri M ve H için özellikle aşırıdır. Üç nörofilament üçlü proteinin tümü, glutamik asit ve lizin kalıntıları bakımından zengin uzun polipeptit dizilimleri içerir ve NfM ve özellikle NfH ayrıca birden fazla ardışık tekrarlanan serin fosforilasyon bölgesi içerir. Bu bölgelerin hemen hepsi peptit lizin-serin-prolin (KSP) içerir ve fosforilasyon normal olarak dendritik nörofilamentlerde değil aksonlarda bulunur. İnsan NF-H iki eksprese ederken İnsan NFM, bu KSP siteleri 13 sahiptir alelleri 44 üretir, bunlardan biri diğer 45 KSP tekrarlar.
Nörofilament düzeneği ve yapısı
Diğer ara filament proteinleri gibi, nörofilament proteinlerinin tümü , büyük ölçüde yapılandırılmamış amino terminal ve karboksi terminal alanları ile çevrili, çubuk benzeri üçüncül yapısı nedeniyle çubuk alanı olarak bilinen ortak bir merkezi alfa sarmal bölgesini paylaşır . İki nörofilament proteininin çubuk alanları, bir alfa sarmal sarmal oluşturmak üzere dimerize olur . İki dimer, bir tetramer oluşturmak için kademeli bir antiparalel şekilde birleşir. Bu tetramerin, nörofilamentin temel alt birimi (yani yapı taşı) olduğuna inanılmaktadır. Tetramer alt birimleri, birim uzunlukta filamentler oluşturmak için yan yana birleşir ve daha sonra olgun nörofilament polimeri oluşturmak için uçtan uca tavlanır, ancak bu alt birimlerin polimer içindeki kesin organizasyonu, büyük ölçüde heterojen protein nedeniyle bilinmemektedir. bileşimi ve nörofilamentleri veya nörofilament proteinlerini kristalleştirememe. Yapısal modeller genellikle bir filament kesitinde sekiz tetramer (32 nörofilament polipeptidi) varsayar, ancak doğrusal kütle yoğunluğunun ölçümleri bunun değişebileceğini düşündürür.
Nörofilament proteinlerinin amino terminal alanları, çok sayıda fosforilasyon bölgesi içerir ve filament montajı sırasında alt birim etkileşimleri için önemli görünmektedir. Karboksi terminal alanları, alfa sarmalı veya beta yaprağı olmayan, özünde düzensiz alanlar gibi görünmektedir. Nörofilament proteinlerinin farklı boyutları, büyük ölçüde karboksi terminal alanlarının uzunluğundaki farklılıklardan kaynaklanmaktadır. Bu alanlar asidik ve bazik amino asit kalıntıları bakımından zengindir. NFM ve NFH'nin karboksi terminal alanları en uzundur ve in vivo fosforilasyon ve glikosilasyon gibi translasyon sonrası modifikasyonlarla kapsamlı bir şekilde değiştirilir . Bir şişe fırçasındaki kıllara benzer şekilde yüksek oranda yüklü ve yapılandırılmamış alanlardan oluşan yoğun bir fırça sınırı oluşturmak için filament omurgasından radyal olarak çıkıntı yaparlar. Bu entropik olarak dövülen alanların, filamanları komşularından etkin bir şekilde ayırarak her bir filamanın etrafında bir dışlama bölgesi tanımlaması önerilmiştir. Bu şekilde, karboksi terminal projeksiyonları, nörofilament polimerlerin boşluk doldurma özelliklerini en üst düzeye çıkarır. Elektron mikroskobu ile bu alanlar, komşu filamentlerle temas ediyor gibi görünen yan kollar olarak adlandırılan çıkıntılar olarak görünür.

nörofilament fonksiyonu

Nörofilamentler omurgalı nöronlarında, özellikle aksonlarda yüksek konsantrasyonlarda bulunur, burada hepsi sürekli olarak örtüşen bir dizi oluşturan aksonun uzun ekseni boyunca paralel olarak hizalanır. Aksonal çapı artıran boşluk dolduran yapılar olarak işlev gördükleri öne sürülmüştür. Akson çapına katkıları, aksondaki nörofilamentlerin sayısı ve bunların paketlenme yoğunluğu ile belirlenir. Aksondaki nörofilamentlerin sayısının, nörofilament gen ekspresyonu ve aksonal taşınma ile belirlendiği düşünülmektedir. Filamentlerin paketleme yoğunluğu, komşu filamentler arasındaki boşluğu tanımlayan yan kolları tarafından belirlenir. Yan kolların fosforilasyonunun, iki değerlikli katyonların bitişik filamentlerin yan kolları arasında bağlanmasıyla komşu filamentler arasındaki boşluğu artırarak uzayabilirliklerini arttırdığı düşünülmektedir.
Gelişimin başlarında aksonlar, nispeten az sayıda nörofilament içeren dar süreçlerdir. Miyelinli hale gelen aksonlar, kalibrelerinin genişlemesini sağlayan daha fazla nörofilament biriktirir. Bir akson büyüyüp hedef hücreye bağlandıktan sonra aksonun çapı beş kata kadar artabilir. Bunun nedeni, sinir hücresi gövdesinden ihraç edilen nörofilamentlerin sayısındaki artışın yanı sıra taşıma hızlarının yavaşlamasıdır. Olgun miyelinli aksonlarda, nörofilamentler en bol bulunan tek sitoplazmik yapı olabilir ve aksonal kesit alanının çoğunu kaplayabilir. Örneğin, büyük bir miyelinli akson, bir kesitte binlerce nörofilament içerebilir.
nörofilament taşıma
Aksonlardaki yapısal rollerine ek olarak, nörofilamentler aynı zamanda aksonal taşıma kargolarıdır . Aksonlardaki nörofilament proteinlerinin çoğu, sinir hücresi gövdesinde sentezlenir ve burada yaklaşık 30 dakika içinde hızla nörofilament polimerleri halinde birleşirler. Bu birleştirilmiş nörofilament polimerler, mikrotübül motor proteinleri tarafından desteklenen mikrotübül yolları üzerinde akson boyunca taşınır . Filamentler çift yönlü, yani hem akson ucuna (anterograd) hem de hücre gövdesine (retrograd) doğru hareket eder, ancak net yön anterograddır. Filamentler, kısa zaman ölçeklerinde (saniye veya dakika) 8 µm/s'ye kadar hızlarda hareket eder ve ortalama hızlar yaklaşık 1 µm/s'dir. Bununla birlikte, daha uzun zaman ölçeklerinde (saatler veya günler) ortalama hız yavaştır çünkü hareketler çok seyrektir ve uzun duraklamalarla kesintiye uğrayan kısa sprintlerden oluşur. Böylece uzun zaman ölçeklerinde nörofilamentler aksonal taşımanın yavaş bileşeninde hareket eder.
Klinik ve araştırma uygulamaları
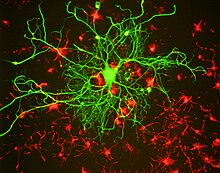
Nörofilament proteinlerine karşı çok sayıda spesifik antikor geliştirilmiştir ve ticari olarak temin edilebilir. Bu antikorlar, immünofloresan mikroskopi veya immünohistokimya kullanılarak hücreler ve dokulardaki nörofilament proteinlerini saptamak için kullanılabilir . Bu tür antikorlar, histolojik kesitlerde ve doku kültüründe nöronları ve onların işlemlerini tanımlamak için yaygın olarak kullanılmaktadır . Tip VI ara filament proteini Nestin, gelişen nöronlarda ve gliada ifade edilir. Nestin, nöronal kök hücrelerin bir belirteci olarak kabul edilir ve bu proteinin varlığı, nörojenezi tanımlamak için yaygın olarak kullanılır . Bu protein gelişme ilerledikçe kaybolur.
Nörofilament antikorları ayrıca tanısal nöropatolojide yaygın olarak kullanılmaktadır . Bu antikorlarla boyama, nöronları (nörofilament proteinleri için pozitif) glia'dan (nörofilament proteinleri için negatif ) ayırt edebilir .
Nörofilament proteinlerinin merkezi sinir sistemini etkileyen hastalıklarda aksonal hasarın biyobelirteçleri olarak kullanımına da önemli klinik ilgi vardır. Nöronlar veya aksonlar dejenere olduğunda, nörofilament proteinleri kan veya beyin omurilik sıvısına salınır. Beyin omurilik sıvısı ve plazmadaki nörofilament proteinlerinin immünoanalizleri, bu nedenle nörolojik bozukluklarda aksonal hasarın göstergeleri olarak hizmet edebilir. NfL, amyotrofik lateral skleroz , multipl skleroz ve daha yakın zamanda Huntington hastalığında hastalık izleme için yararlı bir belirteçtir . Akut iskemik inme sonrası fonksiyonel sonuç için prognostik bir belirteç olarak da değerlendirilmiştir.
Nörofilament anormallikleri olan mutant fareler, amyotrofik lateral skleroza benzeyen fenotiplere sahiptir .
