Leigh sendromu - Leigh syndrome
| Leigh sendromu | |
|---|---|
| Diğer isimler | Juvenil subakut nekrotizan ensefalomyelopati, Leigh hastalığı, infantil subakut nekrotizan ensefalomyelopati, subakut nekrotizan ensefalomyelopati (SNEM) |
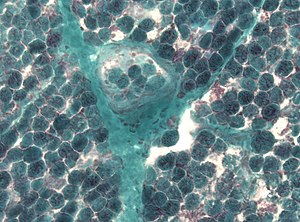 | |
| Kas biyopsisinde çok sayıda düzensiz kırmızı lifin tespiti | |
| uzmanlık |
Nöroloji |
Leigh sendromu (aynı zamanda Leigh hastalığı ve subakut nekrotizan ensefalomyelopati olarak da adlandırılır ), merkezi sinir sistemini etkileyen kalıtsal bir nörometabolik bozukluktur . Adını 1951'de durumu ilk kez tanımlayan İngiliz nöropsikiyatrist Archibald Denis Leigh'den almıştır. Normal seviyelerde tiamin , tiamin monofosfat ve tiamin difosfat yaygın olarak bulunur, ancak düşük bir tiamin trifosfat seviyesi vardır veya yoktur . Bunun tiamin-difosfat kinaz enzimindeki bir blokajdan kaynaklandığı düşünülür ve bu nedenle bazı hastalarda tedavi günlük olarak tiamin trifosfat almak olabilir.
Belirti ve bulgular
Leigh sendromunun semptomları klasik olarak bebeklik döneminde başlayıp birkaç yıl içinde ölüme yol açması olarak tanımlanır; bununla birlikte, daha fazla vaka tanındıkça, semptomların her yaşta ortaya çıkabileceği -ergenlik veya yetişkinlik dahil- ve hastaların tanıdan sonra uzun yıllar hayatta kalabileceği açıktır. Semptomlar genellikle ilk olarak enfeksiyon veya ameliyat gibi vücudun enerji üretimini zorlayan tetikleyici bir olaydan sonra görülür. Leigh sendromunun genel seyri, metabolik stres zamanlarında epizodik gelişimsel gerilemelerden biridir. Bazı hastalarda hastalık progresyonu olmadan uzun dönemler olurken, diğerleri ilerleyici düşüş gelişir.
Sendromlu bebeklerde ishal , kusma ve yutma güçlüğü (yutma veya emme güçlüğü) gibi belirtiler görülür ve bu durum gelişme geriliğine yol açar . Erken Leigh hastalığı olan çocuklar da sinirli görünebilir ve sağlıklı bebeklerden çok daha fazla ağlayabilir. Nöbetler sıklıkla görülür. Fazla laktat görülebileceği idrar , beyin omurilik sıvısı ve kan Leigh sendromu olan bir kişinin.
Hastalık ilerledikçe, beyin kasların kasılmasını kontrol edemediği için kas sistemi vücutta zayıflar. Hipotoni (düşük kas tonusu ve gücü), distoni (istemsiz, sürekli kas kasılması) ve ataksi (hareket üzerinde kontrol eksikliği) Leigh hastalığı olan kişilerde sıklıkla görülür. Gözler , özellikle etkilenir; oftalmoparezi (zayıflık veya felç) ve nistagmus (istemsiz göz hareketleri) adı verilen durumlarda gözleri kontrol eden kaslar zayıflar, felç olur veya kontrol edilemez hale gelir . Yavaş sakkadlar da bazen görülür. Kalp ve akciğerler de Leigh hastalığının bir sonucu olarak başarısız olabilir. Hipertrofik kardiyomiyopati (kalp kasının bir kısmının kalınlaşması) da bazen bulunur ve ölüme neden olabilir; asimetrik septal hipertrofi de Leigh sendromu ile ilişkilendirilmiştir. Leigh sendromu ile ilişkili ventriküler septal defektleri olan çocuklarda piruvat dehidrogenaz eksikliğinden kaynaklanan yüksek alın ve büyük kulaklar görülür; yüz anormallikleri Leigh sendromunun tipik özelliği değildir.
Bununla birlikte, solunum yetmezliği , Leigh sendromlu kişilerde en yaygın ölüm nedenidir. Diğer nörolojik semptomlar arasında periferik nöropati , periferik sinir sistemindeki hasarın neden olduğu ekstremitelerde duyu kaybı yer alır .
Hipertrikoz , nükleer gen SURF1'deki mutasyonların neden olduğu Leigh sendromunda görülür .
genomik
Mutasyonlar içinde mitokondriyal DNA (mtDNA) ve üzerinde 30 gen , nükleer DNA (gen SURF1 ve bazı COX düzeneği faktörleri) Leigh hastalığı implike edilmiştir.
Oksidatif fosforilasyon bozuklukları, hücrelerin ana enerji kaynağı olan adenozin trifosfat (ATP) üretme süreci , mtDNA veya nükleer kodlanmış genlerdeki mutasyonlardan kaynaklanabilir. Sonuncusu, Leigh hastalığının çoğunluğunu açıklar, ancak belirli bir bireydeki durumdan sorumlu spesifik mutasyonu belirlemek her zaman mümkün değildir. Oksidatif fosforilasyona dahil olan beş protein kompleksinden dördü , Leigh sendromunda, ya hatalı biçimlendirilmiş protein nedeniyle ya da bu komplekslerin montajındaki bir hata nedeniyle en yaygın olarak bozulur. Genetik temelden bağımsız olarak, mutasyondan etkilenen komplekslerin oksidatif fosforilasyondaki rollerini yerine getirememesine neden olur. Leigh hastalığında beyin sapı ve bazal ganglionlardaki önemli hücreler etkilenir. Bu, hücrelerde kronik bir enerji eksikliğine neden olur, bu da hücre ölümüne yol açar ve sırayla merkezi sinir sistemini etkiler ve motor fonksiyonları engeller. Kalp ve diğer kaslar da çok fazla enerji gerektirir ve Leigh sendromundaki kronik enerji eksikliklerinin neden olduğu hücre ölümünden etkilenir.
Mitokondriyal DNA mutasyonları
Mitokondri gerekli olan organelleri içerisinde ökaryotik hücreler. İşlevleri, glikoz , amino asitler ve yağ asitlerinin potansiyel enerjisini oksidatif fosforilasyon adı verilen bir süreçte adenozin trifosfata (ATP) dönüştürmektir . Mitokondri , mitokondriyal DNA (mtDNA) adı verilen kendi DNA'sını taşır . MtDNA'da depolanan bilgiler , ATP üretimi için gerekli olan enzimlerin birkaçını üretmek için kullanılır .
Leigh sendromu vakalarının yüzde 20 ila 25'i mitokondriyal DNA'daki mutasyonlardan kaynaklanır. Bu mutasyonların en yaygın olanı, Leigh sendromunun yüzde 10 ila 20'sinde bulunur ve oksidatif fosforilasyon zincirinin son kompleksindeki bir proteini kodlayan bir gen olan MT-ATP6'da meydana gelir , ATP sentaz , doğrudan ATP üreten bir enzim. ATP sentaz olmadan, elektron taşıma zinciri herhangi bir ATP üretmeyecektir. En yaygın MT-ATP6 mutasyonu Leigh sendromu bulunan bir nokta mutasyonu , bir değişikliği nükleotid 8993 de timin a guanin . Leigh sendromuyla ilişkili bu ve diğer nokta mutasyonları, protein kompleksini dengesizleştirir veya hatalı biçimlendirir ve etkilenen hücrelerde enerji üretimini düşük tutar. Oksidatif fosforilasyon zincirinin ilk kompleksinin yaratılmasında rol oynayan birkaç mitokondriyal gen, MT-ND2 , MT-ND3 , MT-ND5 , MT-ND6 ve MT-CO1 genleri dahil olmak üzere bir Leigh sendromu vakasında yer alabilir .
Mitokondriyal DNA, maternal kalıtım adı verilen bir modelde anasoylu olarak aktarılır - bir anne, Leigh sendromu genlerini hem erkek hem de kız çocuklarına aktarabilir, ancak babalar mitokondriyal genleri aktaramaz.
Nükleer DNA mutasyonları
Nükleer DNA , bir organizmanın genomunun çoğunu içerir ve cinsel olarak üreyen organizmalarda, mitokondriyal DNA'nın maternal kalıtım modelinin aksine, her iki ebeveynden de miras alınır. Nükleer DNA mutasyonlarının neden olduğu Leigh sendromu, otozomal resesif bir modelde kalıtsaldır . Bu, hastalığa neden olmak için mutasyona uğramış genin iki kopyasının gerekli olduğu anlamına gelir, bu nedenle, her biri bir mutant allel taşıyan etkilenmemiş iki ebeveyn, bu çocuk mutant alleli her iki ebeveynden miras alırsa, etkilenmiş bir çocuğa sahip olabilir.
Leigh sendromunun yüzde 75 ila 80'i nükleer DNA'daki mutasyonlardan kaynaklanır; Oksidatif fosforilasyonda yer alan dördüncü kompleksin, sitokrom c oksidazın (COX) işlevini veya birleşmesini etkileyen mutasyonlar , çoğu Leigh hastalığı vakasına neden olur. SURF1 (surfeit1) adı verilen bir gendeki mutasyonlar , Leigh sendromunun bu alt tipinin en yaygın nedenidir. SURF1'in kodladığı protein erken sonlandırılır ve bu nedenle işlevini yerine getiremez, COX'in alt birimlerini birlikte işlevsel bir protein kompleksine yönlendirir. Bu, mitokondri tarafından üretilen enerji miktarını azaltan bir COX proteini eksikliği ile sonuçlanır. SURF1, kromozom 9'un uzun kolunda bulunur . Leigh sendromuna neden olan bir başka nükleer DNA mutasyonu , Link reaksiyon yolundaki bir enzim olan mitokondrideki başka bir protein kompleksi olan piruvat dehidrojenazı etkiler . Bazı SURF1 mutasyon tipleri, özellikle geç başlangıçlı ancak benzer şekilde değişken klinik seyir gösteren bir Leigh sendromu alt tipine neden olur.
Leigh sendromu ile ilişkili diğer nükleer genler, kromozom 2 üzerinde yer alır ( BCS1L ve NDUFA10 ); kromozom 5 ( SDHA , NDUFS4 , NDUFAF2 ve NDUFA2 ); kromozom 8 ( NDUFAF6 ), kromozom 10 ( COX15 ); kromozom 11 ( NDUFS3 , NDUFS8 ve FOXRED1 ); kromozom 12 ( NDUFA9 ve NDUFA12 ); ve kromozom 19 ( NDUFS7 ). Bu genlerin çoğu, ilk oksidatif fosforilasyon kompleksini etkiler.
X'e bağlı Leigh sendromu

Leigh sendromuna ayrıca en yaygın olarak X'e bağlı bir gen ( OMIM 308930 ) tarafından kodlanan bir PDHC alt birimini içeren piruvat dehidrojenaz kompleksinin (PDHC) eksikliği neden olabilir . PDHC eksikliğinin neden olduğu Leigh sendromunun nörolojik özellikleri diğer formlardan ayırt edilemez. Ancak PDHC eksikliğinde nörolojik olmayan özellikler (laktik asidoz dışında) görülmez.
X'e bağlı çekinik Leigh sendromu, erkek çocukları kız çocuklarından çok daha sık etkiler çünkü onlarda X kromozomunun yalnızca bir kopyası vardır . Kız çocukların, X'e bağlı Leigh sendromundan etkilenmek için hatalı genin iki kopyasına ihtiyacı olacaktır.
Fransız Kanadalı Leigh sendromu
Leigh sendromu tip çok daha yüksek bir oranda bulunan Saguenay-Lac-Saint-Jean bir mutasyondan kaynaklanır Quebec bölge LRPPRC kromozom 2. Her iki kol küçük ( 'p') üzerinde yer alan bir gen, bileşik heterozigotluk ve homozigot mutasyonlar Fransız Kanada Leigh sendromunda gözlenmiştir. Hastalığın bu alt tipi ilk olarak 1993 yılında, mitokondriyal elektron taşıma zincirindeki dördüncü kompleks olan sitokrom c oksidazda (COX) ciddi bir eksikliği olan bölgeden 34 çocukta tanımlanmıştır . Etkilenen hücrelerde bulunan proteinin alt birimleri işlevsel olsa da, düzgün bir şekilde birleştirilmemişlerdi. Eksikliğin beyin ve karaciğer dokularında hemen hemen tam, fibroblastlarda (bağ dokusu hücreleri) ve iskelet kasında önemli (normal enzim aktivitesinin yaklaşık %50'si) olduğu bulundu . Böbrek ve kalp dokularında COX eksikliği olmadığı bulundu.
Fransız Kanadalı Leigh sendromu, diğer Leigh sendromu türlerine benzer semptomlara sahiptir. Başlangıç yaşı ortalama 5 aydır ve ortanca ölüm yaşı 1 yıl 7 aydır. Hastalığı olan çocuklar gelişimsel olarak gecikir , orta yüz hipoplazisi ve geniş burun köprüsü , kronik metabolik asidoz ve hipotoni (düşük kas gücü) dahil olmak üzere hafif dismorfik yüz özelliklerine sahiptir . Diğer semptomlar arasında takipne (olağandışı hızlı nefes alma hızı), zayıf emme yeteneği, hipoglisemi (düşük kan şekeri) ve titreme bulunur . Şiddetli, ani metabolik asidoz, yaygın bir ölüm nedenidir.
Saguenay-Lac-Saint-Jean bölgesindeki genetik taşıyıcı oranı tahminleri 23'te 1 ile 28'de 1 arasında değişmektedir; Hastalıkla doğan çocuk sayısının 2063'te 1, 2473 canlı doğumda 1 olduğu tahmin edilmektedir. Şecere çalışmaları, sorumlu mutasyonun bölgeye erken Avrupalı yerleşimciler tarafından getirildiğini gösteriyor.
patofizyoloji
Leigh sendromu karakteristik semptomları, en azından kısmen karşılıklı fokal neden olan lezyonlar içinde beyin sapı , bazal gangliyonlar , serebellum ve beynin diğer. Lezyonlar, demiyelinizasyon , spongioz , glioz , nekroz ve kılcal proliferasyon alanları dahil olmak üzere farklı biçimler alır . Demiyelinizasyon, nöronların aksonlarının etrafındaki miyelin kılıfının kaybıdır ve diğer nöronlarla iletişim kurma yeteneklerini engeller. Beyin sapı, nefes alma, yutma ve dolaşım gibi temel yaşam işlevlerinin sürdürülmesinde yer alır; bazal ganglionlar ve serebellum hareket ve dengeyi kontrol eder. Bu nedenle, bu alanlardaki hasar, Leigh sendromunun başlıca semptomlarına yol açar - bu alanlar tarafından kontrol edilen işlevler üzerindeki kontrol kaybı.
Bazen Leigh sendromu ile ilişkili laktik asidoz , belirli tipte oksidatif fosforilasyon eksiklikleri olan kişilerde işlenemeyen piruvat birikmesinden kaynaklanır . Pıruvat ya dönüştürülür alanin ile alanin aminotransferaz veya laktik asit dönüştürülür laktat dehidrojenaz ; bu maddelerin her ikisi de vücutta birikebilir.
Teşhis
Leigh sendromu klinik bulgularla öne sürülür ve laboratuvar ve genetik testlerle doğrulanır.
Klinik bulgular
Distoni, nistagmus ve otonom sinir sistemi ile ilgili problemler, potansiyel olarak Leigh sendromunun neden olduğu bazal ganglionlarda ve beyin sapında hasar olduğunu düşündürür . Diğer semptomlar ayrıca hipertrikoz ve nörolojik olarak sağırlık gibi beyin hasarının göstergesidir . Laktik asidoz veya asidemi ve hiperalaninemi ( kandaki yüksek alanin seviyeleri) laboratuvar bulguları da Leigh sendromunu düşündürebilir. İdrardaki organik asit seviyesinin değerlendirilmesi de metabolik yolda bir işlev bozukluğuna işaret edebilir .
Ayırıcı tanı
Diğer hastalıklar, Leigh sendromuna benzer bir klinik sunuma sahip olabilir; benzer klinik semptomların diğer nedenlerini dışlamak genellikle Leigh sendromunu teşhis etmenin ilk adımıdır. Leigh hastalığına benzer görünebilen durumlar arasında perinatal asfiksi , kernikterus , karbon monoksit zehirlenmesi , metanol toksisitesi , tiamin eksikliği , Wilson hastalığı , biotine duyarlı bazal ganglion hastalığı ve bazı ensefalit türleri bulunur . Perinatal asfiksi, Leigh sendromunda görülen belirtilere benzer şekilde bilateral gangliyal lezyonlara ve talamusta hasara neden olabilir . Tüm hiperbilirubinemisi ile tedavi edilmemiş olan fototerapi , bilirübin birikebilir bazal gangliyonlar ve Leigh sendromunda görülenlere benzer lezyonlara yol açar. Bu, fototerapinin ortaya çıkışından beri yaygın değildir.
tedavi
Süksinik asit çalışılmış ve hem Leigh sendromu hem de MELAS sendromu için etkili olduğu gösterilmiştir . Bireyin Leigh sendromunda X kromozomundaki bir genin rolü varsa , yüksek yağlı, düşük karbonhidratlı bir diyet izlenebilir. Tiamin (B vitamini 1 ise) verilebilir piruvat dehidrojenaz eksikliği bilinen veya şüphelenilen. Laktik asidoz semptomları, diyete sodyum bikarbonat (kabartma tozu) veya sodyum sitrat eklenerek tedavi edilir, ancak bu maddeler Leigh sendromunun nedenini tedavi etmez. Dikloroasetat ayrıca Leigh sendromuyla ilişkili laktik asidozun tedavisinde de etkili olabilir; bu madde üzerinde araştırmalar devam etmektedir. Koenzim Q10 takviyelerinin bazı durumlarda semptomları iyileştirdiği görülmüştür.
Leigh sendromu için ilaç EPI-743'ün klinik denemeleri devam etmektedir.
2016 yılında, John Zhang ve ekibi, New York, ABD'deki New Hope Doğurganlık Merkezi'nde , Meksika'da Leigh hastalığı olan bir bebek üretme riski taşıyan bir anne üzerinde bir iğ transferi mitokondriyal bağış tekniği gerçekleştirdi. 6 Nisan 2016'da sağlıklı bir erkek çocuk dünyaya geldi. Ancak tekniğin tamamen güvenilir ve güvenli olup olmadığı henüz kesin değil.
prognoz
Hepsi kötü olsa da, farklı genetik nedenler ve Leigh sendromu türleri farklı prognozlara sahiptir. Etkilenen proteinlerden birinin tam eksikliğinden kaynaklanan hastalığın en şiddetli formları, birkaç yaşında ölüme neden olur. Eksiklik tam değilse, prognoz biraz daha iyidir ve etkilenen bir çocuğun 6-7 yıl ve nadir durumlarda gençlik yıllarına kadar hayatta kalması beklenir.
epidemiyoloji
Leigh sendromu, bazı popülasyonlarda çok daha yüksek oranlara sahip olmasına rağmen, 40.000 canlı doğumdan en az birinde görülür. Gelen Saguenay-Lac-Saint-Jean merkez bölgesinde Quebec , Leigh sendromu 2000 yenidoğanlarda 1 oranında ortaya çıkar.
Tarih
Leigh sendromu ilk olarak 1951'de Denis Leigh tarafından tanımlandı ve 1954'te benzer Wernicke ensefalopatisinden ayırt edildi. 1968'de, hastalığın mitokondriyal aktivite ile bağlantısı ilk kez belirlendi, ancak sitokrom c oksidaz ve diğer elektron taşıma zinciri proteinlerindeki mutasyonlar 1977'ye kadar keşfedilmedi. .
Ayrıca bakınız
Referanslar
daha fazla okuma
- Mitokondriyal DNA ile İlişkili Leigh Sendromu ve NARP üzerine GeneReviews/NCBI/NIH/UW girişi
- Mitokondriyal DNA ile İlişkili Leigh Sendromu ve NARP ile ilgili OMIM girişleri
- Leigh sendromu; Subakut nekrotizan ensefalopati; Leigh'in hastalığı en NIH 'Dairesi'nin s Nadir Hastalıklar
- leighsdisease de NINDS
- Maternal Leigh Sendromu Kalıtsal de NIH Dairesi'nin s' Nadir Hastalıklar
Dış bağlantılar
| sınıflandırma |
|---|


