Pankreas adacıkları - Pancreatic islets
| Pankreas adacıkları/langerhans adacıkları | |
|---|---|

| |
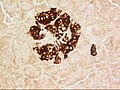
 Tipik bir pozisyonda, bir kan damarına yakın bir fareden alınan pankreas adacığı; insülin kırmızı, çekirdekler mavi.
| |
| Detaylar | |
| Parçası | Pankreas |
| sistem | Endokrin |
| tanımlayıcılar | |
| Latince | insulae pankreas |
| ağ | D007515 |
| TA98 | A05.9.01.019 |
| TA2 | 3128 |
| FMA | 16016 |
|
Mikroanatominin anatomik terimleri | |
Pankreas adacıkları veya Langerhans adacıkları bölgeleridir pankreas da içeren endokrin tarafından 1869 yılında keşfedilmiştir (hormon üreten) hücreler, Alman patolojik anatomi Paul, Langerhans . Pankreas adacıkları pankreas hacminin %1-2'sini oluşturur ve kan akışının %10-15'ini alır. Pankreas adacıkları, insan pankreası boyunca yoğunluk yollarında düzenlenir ve glikoz metabolizmasında önemlidir .
Yapı
Sağlıklı bir yetişkin insanın pankreası boyunca yoğunluk yolları şeklinde dağılmış yaklaşık 1 milyon adacık vardır ve bunların her biri ortalama 0,2 mm çapındadır. :928 Her biri çevreleyen pankreas dokusundan , pankreasın geri kalanı boyunca iç içe geçmiş fibröz bağ dokusu ile sürekli olan ince bir fibröz bağ dokusu kapsülü ile ayrılır . :928
mikroanatomi
Pankreas adacıklarında üretilen hormonlar (en az) beş hücre tipi tarafından doğrudan kan akışına salgılanır. Sıçan adacıklarında endokrin hücre tipleri şu şekilde dağılır:
- Glukagon üreten alfa hücreleri (toplam adacık hücrelerinin %20'si)
- İnsülin ve amilin üreten beta hücreleri (≈70%)
- Somatostatin üreten delta hücreleri (<%10)
- Ghrelin üreten epsilon hücreleri (<%1)
- Pankreatik polipeptid üreten PP hücreleri (gama hücreleri veya F hücreleri) (<%5)
Pankreas adacıklarının hücre mimarisinin türler arasında farklılık gösterdiği kabul edilmiştir . Özellikle, kemirgen adacıkları, kümenin merkezinde baskın bir insülin üreten beta hücreleri oranı ve periferde az sayıda alfa, delta ve PP hücreleri ile karakterize edilirken, insan adacıkları birbirleriyle yakın ilişki içinde alfa ve beta hücreleri sergiler. küme boyunca.
Adacıklardaki beta hücrelerinin oranı türe göre değişir, insanlarda yaklaşık %40-50'dir. Endokrin hücrelere ek olarak stromal hücreler (fibroblastlar), vasküler hücreler (endotel hücreleri, perisitler), bağışıklık hücreleri (granülositler, lenfositler, makrofajlar, dendritik hücreler) ve sinir hücreleri vardır.
Adacıklardan büyük miktarda kan akar, 1 g adacık başına 5-6 mL/dk. Pankreasın ekzokrin dokusundan 15 kat daha fazladır.
Adacıklar, parakrin ve otokrin iletişim yoluyla birbirlerini etkileyebilir ve beta hücreleri, elektriksel olarak altı ila yedi diğer beta hücresine bağlanır, ancak diğer hücre tiplerine değil.
İşlev
Parakrin pankreatik adacıkların geri besleme sistemi, aşağıdaki yapıya sahiptir:
- Glikoz/İnsülin: beta hücrelerini aktive eder ve alfa hücrelerini inhibe eder
- Glikojen/Glukagon: beta hücrelerini ve delta hücrelerini aktive eden alfa hücrelerini aktive eder
- Somatostatin: alfa hücrelerini ve beta hücrelerini inhibe eder
Çok sayıda G proteinine bağlı reseptör (GPCR'ler), pankreas adacıklarından insülin, glukagon ve somatostatin salgılanmasını düzenler ve bu GPCR'lerin bazıları, tip 2 diyabeti tedavi etmek için kullanılan ilaçların hedefleridir (ref GLP-1 reseptör agonistleri, DPPIV inhibitörleri).
elektriksel aktivite
Pankreas adacıklarının elektriksel aktivitesi, yama klemp teknikleri kullanılarak incelenmiştir . Bozulmamış adacıklardaki hücrelerin davranışının, dağılmış hücrelerin davranışından önemli ölçüde farklı olduğu ortaya çıktı.
Klinik önemi
Şeker hastalığı
Beta hücreleri pankreatik adacıklar secrete insülin ve böylece de önemli bir rol oynamaktadır diyabet . Bağışıklık saldırıları ile yok edildikleri düşünülmektedir. Bununla birlikte, beta hücrelerinin yok edilmediğine, sadece işlevsiz hale geldiğine dair göstergeler de var.
Transplantasyon
Pankreas adacıklarının beta hücreleri seçici bir otoimmün süreci ile tahrip olduğu için , tip 1 diyabet , klinisyenler ve araştırmacılar aktif tam bir alternatif sunacaktır fizyolojik beta hücresi fonksiyonunu geri bir araç olarak doku adacığı transplantasyonu devam ediyor pankreas nakli ya da yapay pankreas . Adacık transplantasyonu, 1970'lerin başında diyabet gerektiren insülin tedavisi için uygun bir seçenek olarak ortaya çıktı ve takip eden otuz yıl boyunca istikrarlı bir ilerleme kaydedildi. Son klinik deneyler, kadavra donör adacıklarının stabil olmayan tip 1 diyabetli hastalara transplantasyonundan sonra insülin bağımsızlığının ve gelişmiş metabolik kontrolün tekrarlanabilir bir şekilde elde edilebileceğini göstermiştir .
Vücut kitle indeksi (BMI) yüksek olan kişiler, transplantasyon sırasında daha büyük teknik komplikasyonlar nedeniyle uygun olmayan pankreatik donörlerdir. Bununla birlikte, daha büyük pankreasları nedeniyle daha fazla sayıda adacık izole etmek mümkündür ve bu nedenle daha uygun adacık vericileridir.
Adacık nakli sadece bu hastalığın tedavisi için gerekli olan beta hücrelerinden oluşan doku transferini içerir. Bu nedenle, teknik olarak daha zahmetli olan ve örneğin organ kaybına yol açan pankreatit riski taşıyan tüm pankreas transplantasyonuna göre bir avantajı temsil eder. Diğer bir avantajı ise hastaların genel anestezi gerektirmemesidir.
Tip 1 diyabet için adacık transplantasyonu , donör adacıklarının konakçı tarafından reddedilmesini önlemek için şu anda güçlü immünosupresyon gerektirir .
Adacıklar , daha sonra karaciğere implante edilen bir portal vene nakledilir. Portal ven dal trombozu riski ve transplantasyondan birkaç dakika sonra adacık sağkalımının düşük değeri vardır, çünkü bu bölgedeki vasküler yoğunluk, endojen adacıklara göre ameliyattan birkaç ay sonra daha düşüktür. Bu nedenle, neovaskülarizasyon, örneğin adacıklar ve vasküler endotelyal hücreler tarafından üretilen VEGF tarafından desteklenen, adacık sağkalımının anahtarıdır. Bununla birlikte, intraportal transplantasyonun başka eksiklikleri vardır ve bu nedenle adacık implantasyonu için daha iyi mikro-ortam sağlayacak diğer alternatif alanlar incelenmektedir. Adacık nakli araştırmaları ayrıca adacık enkapsülasyonu, CNI içermeyen (kalsinörin inhibitörü) immünosupresyon, adacık hasarının biyobelirteçleri veya adacık donörü eksikliğine odaklanır.
Alternatif bir beta hücresi kaynağı, yetişkin kök hücrelerden veya progenitör hücrelerden türetilen insülin üreten hücreler , transplantasyon için donör organ eksikliğinin üstesinden gelmeye katkıda bulunacaktır. Rejeneratif tıp alanı hızla gelişmektedir ve yakın gelecek için büyük umutlar sunmaktadır. Bununla birlikte, tip 1 diyabet, pankreastaki beta hücrelerinin otoimmün yıkımının bir sonucudur. Bu nedenle, etkili bir tedavi, yeterli ve güvenli bağışıklık müdahalelerini beta hücre yenileyici yaklaşımlarla birleştiren sıralı, entegre bir yaklaşım gerektirecektir. Ayrıca, alfa hücrelerinin, hem sağlıklı hem de diyabetik insan ve fare pankreas adacıklarında, beta hücresi rejenerasyonu için gelecekteki olası bir kaynak olan, kendiliğinden kaderi değiştirebildiği ve beta hücrelerine farklılaşabildiği de gösterilmiştir. Aslında, adacık morfolojisi ve endokrin farklılaşmasının doğrudan ilişkili olduğu bulunmuştur. Endokrin progenitör hücreler, uyum içinde göç ederek ve tomurcuk benzeri adacık öncüleri veya alfa hücrelerinin yarımadanın dış katmanını oluşturduğu ve beta hücrelerinin daha sonra altlarında oluştuğu "yarımadalar" oluşturarak farklılaşır.
Ek resimler
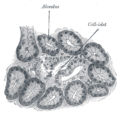
Sıçan adacıkları (üstte) ve insan adacıkları (altta) ile pankreasın ventral kısmı (solda) ve dorsal kısmı (sağda) arasındaki yapısal farklılıklar . Farklı hücre tipleri renk kodludur. Kemirgen adacıkları, insan adacıklarından farklı olarak, karakteristik insülin çekirdeğini gösterir.
Ayrıca bakınız
- betatrofin
- nöroendokrin tümör
- Pankreas nöroendokrin tümörü
- Langerhans Adacıklarının Hemen Dışında Adrift , Harlan Ellison'ın bir romanı