Bosentan - Bosentan
 | |
| Klinik veriler | |
|---|---|
| Ticari isimler | Tracleer, Bekçi |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a605001 |
| Lisans verileri | |
| Hamilelik kategorisi |
|
Yönetim yolları |
Ağızla |
| ATC kodu | |
| Hukuki durum | |
| Hukuki durum | |
| Farmakokinetik veriler | |
| biyoyararlanım | %50 |
| Protein bağlama | >98% |
| Metabolizma | Karaciğer |
| Eliminasyon yarı ömrü | 5 saat |
| tanımlayıcılar | |
| |
| CAS numarası | |
| PubChem Müşteri Kimliği | |
| IUPHAR/BPS | |
| İlaç Bankası | |
| Kimyasal Örümcek | |
| ÜNİİ | |
| fıçı | |
| chebi | |
| CHEMBL | |
| CompTox Panosu ( EPA ) | |
| ECHA Bilgi Kartı |
100.171.206 |
| Kimyasal ve fiziksel veriler | |
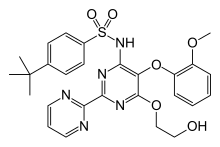
| formül | C 27 H 29 N 5 O 6 S |
| Molar kütle | 551,62 g·mol -1 |
| 3B model ( JSmol ) | |
| |
| |
|
| |
Diğerleri arasında Tracleer markası altında satılan Bosentan , pulmoner arter hipertansiyonunun (PAH) tedavisinde kullanılan çift endotelin reseptör antagonisti bir ilaçtır .
Bosentan, film kaplı tabletler (62.5 mg veya 125 mg) veya oral süspansiyon (32 mg) için dağılabilir tabletler olarak mevcuttur.
Tıbbi kullanımlar
Bosentan, orta derecede pulmoner arter hipertansiyonu olan kişileri tedavi etmek ve sistemik sklerodermalı kişilerde dijital ülserlerin (özellikle parmak uçlarında ve daha az sıklıkla eklemlerde açık yaralar) sayısını azaltmak için kullanılır .
Bosentan fetüslere zarar verir ve hamileler almamalı ve alırken hamile kalmamalıdır (Gebelik Kategorisi X). Hormonal kontraseptifleri etkisiz hale getirebilir, bu nedenle diğer doğum kontrol yöntemleri kullanılmalıdır.
ABD'de yalnızca fetüslere yönelik riskler ve karaciğer hasarına neden olma riskleri açısından FDA tarafından zorunlu kılınan bir risk değerlendirme ve azaltma stratejisini (REMS) izleyen doktorlar tarafından kullanılabilir . Doktor, ilacı reçete etmeden önce kadınlar için negatif bir gebelik testi belgelemeli, doğum kontrolü konusunda tavsiyede bulunmalı ve düzenli gebelik testleri yapmalıdır. Bosentanın karaciğer hasarına neden olma riski yüksek olduğundan , REMS planı ayrıca yüksek transaminazlar için ön test ve ilaç alınırken düzenli testler gerektirir . Bosentan ayrıca , bu iki ajan birlikte alındığında artan karaciğer enzimleri ve karaciğer hasarı riski nedeniyle gliburid alan hastalarda kontrendikedir .
Yan etkiler
Doğum kusurlarına neden olma ve karaciğer hasarına neden olma riskine ek olarak, bosentan ödem, pulmoner veno-tıkayıcı hastalık , sperm sayısında azalma, hemoglobin ve hematokritte azalmaya neden olma riski yüksektir .
Çok yaygın yan etkiler (insanların %10'undan fazlasında görülür) baş ağrısı, transaminazlarda yükselme ve ödemdir. Yaygın yan etkiler (insanların %1 ila %10'u arasında) anemi, hemoglobin azalması, aşırı duyarlılık reaksiyonları, cilt iltihabı, kaşıntı, döküntü, kırmızı cilt, kızarma, bayılma, kalp çarpıntısı, düşük tansiyon, burun tıkanıklığı, mide-yemek borusu reflü içerir. hastalık ve ishal.
Hareket mekanizması
Bosentan, endotelin-A (ET-A) ve endotelin-B (ET-B) reseptörlerinde endotelin -1'in rekabetçi bir antagonistidir . Normal koşullar altında, ET-A reseptörlerinin endotelin-1 bağlanması , pulmoner kan damarlarının daralmasına neden olur . Tersine, endotelin-1'in ET-B reseptörlerine bağlanması, ET-B alt tipine (ET-B1 veya ET-B2) ve dokuya bağlı olarak vasküler düz kasın hem vazodilatasyonu hem de vazokonstriksiyonu ile ilişkilendirilmiştir. Bosentan, hem ET-A hem de ET-B reseptörlerini bloke eder, ancak ET-A reseptörleri üzerinde daha büyük bir etki yarattığı ve pulmoner vasküler dirençte tam bir azalmaya neden olduğu düşünülmektedir.
farmakokinetik
Sağlıklı kişilerde bosentanın mutlak biyoyararlanımı yaklaşık %50'dir. Oral süspansiyon için dağılabilir tabletlerle bosentanın doruk plazma konsantrasyonu, oral tabletlerin doruk konsantrasyonuna kıyasla ortalama olarak %14 daha azdır.
Bosentan, CYP3A4 ve CYP2C9'un bir substratıdır . CYP2C19 ayrıca metabolizmasında da rol oynayabilir. Aynı zamanda hepatik alım taşıyıcı organik anyon taşıyan polipeptitlerin ( OATP'ler ) OATP1B1, OATP1B3 ve OATP2B1'in bir substratıdır.
Bosentanın eliminasyonu çoğunlukla hepatiktir ve renal ve fekal atılımın minimum katkısı vardır.
Bosentan ile siklosporin kullanımı kontrendikedir çünkü siklosporin A'nın bosentan serum konsantrasyonunu belirgin şekilde arttırdığı gösterilmiştir.
Tarih
Bosentan, üzerinde çalışılan dozdaki toksisite nedeniyle 1997'nin başlarında sonlandırılan REACH-1 adlı bir çalışmada kalp yetmezliği üzerinde çalışıldı; 2001 itibariyle, bu denemenin sonuçları yayınlanmamıştı.
Pulmoner arter hipertansiyonu için ABD'de Kasım 2001'de ve Avrupa Birliği'nde Mayıs 2002'de onaylanmıştır.
Toplum ve kültür
ekonomi
2013 itibariyle, dünya çapında bosentan satışları 1.57 milyar dolardı. Bosentan üzerindeki patentler 2015 yılında sona ermeye başladı.
Ayrıca bakınız
Referanslar
Dış bağlantılar
- "Bosentan" . İlaç Bilgi Portalı . ABD Ulusal Tıp Kütüphanesi.
