Ortosilikat - Orthosilicate
Kimyada, ortosilikat olduğu anyonu SiO 4−
4 veya tuzlarından ve esterlerinden herhangi biri . Bu biridir silikat anyonları. Bazen silikon tetroksit anyonu veya grubu olarak adlandırılır .
Sodyum ortosilikat gibi ortosilikat tuzları stabildir ve doğada silikat mineralleri olarak yaygın şekilde bulunur, nesosilikatların tanımlayıcı özelliği olarak . Bir magnezyum veya demir (II) ortosilikat olan olivin , üst mantoda en bol bulunan mineraldir .
Ortosilikat anyon güçlü baz , konjuge baz son derece zayıf bir ortosilisik asit H
4 SiO
4 ( 25 ° C'de p K a2 = 13,2). Bu dengenin incelenmesi zordur çünkü asit hidratlı bir silika yoğunlaşmasına ayrışma eğilimindedir .
Yapısı
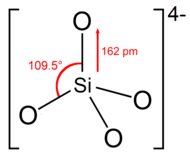
Ortosilikat iyon veya grup, dört oksijen atomu ile çevrili bir silikon atomu ile tetrahedral şekle sahiptir .
Anyonda her oksijen bir birim negatif yük taşır. Si – O bağı 162 pm uzunluğundadır.
Tetrametil ortosilikat gibi organik bileşiklerde , her oksijen resmi olarak nötrdür ve molekülün geri kalanına tek bir kovalent bağ ile bağlanır .
Kullanımlar
Evropiyum takviyeli baryum ortosilikat (Ba 2 SiO 4 ) ortak olan fosfor yeşil kullanılan ışık yayan diyotlar (LED). Mavi LED'ler için fosfor, stronsiyum katkılı baryum ortosilikat ile yapılabilir. Baryum ortosilikat önemli bir nedeni olan katot zehirlenmesi içinde vakum tüpleri .
Organik Kimya
İnorganik kimyada ve jeokimyada çok önemli olmasına rağmen, ortosilikat iyonu organik kimyada nadiren görülür. Bununla birlikte, organik sentezde iki silikat bileşiği kullanılır : tetraetil ortosilikat veya TEOS , polimerleri bağlamak için kullanılır ve özellikle aerojellerin üretiminde önemlidir. Tetrametil ortosilikat veya TMOS , TEOS'a alternatif olarak kullanılır ve ayrıca bir reaktif olarak başka birçok kullanıma sahiptir. TMOS, yüksek konsantrasyonlarda toksik metanol üretmek için ayrıştığı için TEOS, TMOS'a göre tercih edilir . TMOS'u solumak, akciğerlerde toksik silika birikmesine neden olabilir.