antrasiklin - Anthracycline
Antrasiklinler , Streptomyces bakterisinden elde edilen kanser kemoterapisinde kullanılan bir ilaç sınıfıdır . Bu bileşikler, lösemiler , lenfomalar , meme , mide , rahim , yumurtalık , mesane kanseri ve akciğer kanserleri dahil olmak üzere birçok kanseri tedavi etmek için kullanılır . Keşfedilen ilk antrasiklin , bir aktinobakteri türü olan Streptomyces peucetius tarafından doğal olarak üretilen daunorubisindir (ticari adı Daunomycin) . Klinik olarak en önemli antrasiklinler doksorubisin , daunorubisin , epirubisin ve idarubisindir .
Antrasiklinler şimdiye kadar geliştirilmiş en etkili antikanser tedavileri arasındadır ve diğer herhangi bir kemoterapötik ajan sınıfından daha fazla kanser türüne karşı etkilidir. Ana olumsuz etkileri , yararlılıklarını önemli ölçüde sınırlayan kardiyotoksisitedir . Antrasiklin kullanımının ayrıca, döngü 1 şiddetli veya ateşli nötropeni ile önemli ölçüde ilişkili olduğu gösterilmiştir . Diğer olumsuz etkiler arasında kusma sayılabilir.
İlaçlar esas olarak DNA ile araya girerek ve DNA metabolizmasına ve RNA üretimine müdahale ederek etki eder. Sitotoksisite, esas olarak , enzim DNA'da bir kırılmayı indükledikten sonra topoizomeraz II'nin inhibisyonundan kaynaklanır , bu da kırılmanın yeniden ligasyonunu önleyerek hücre ölümüne yol açar. Antrasiklinlerin temel yapısı, bir şeker parçasına glikozidik bir bağlantı ile bağlı bir antrakinon omurgasına sahip bir tetrasiklik molekülün yapısıdır . Bir hücre tarafından alındığında, dört halka yapısı DNA baz çiftleri arasına girerken şeker küçük oluk içinde oturur ve bitişik baz çiftleri ile etkileşime girer.
Tarih
Daunorubisin , 1960'ların başında keşfedilen kırmızı pigmentli bir ilaçtır. Di Marco ve İtalya'daki Farmitalia Araştırma Laboratuvarlarında çalışan ve buna daunomycin adını veren iş arkadaşları tarafından Streptomyces peucetius'un bir türünden izole edildi . Aynı zamanda Dubost ve Fransa'daki iş arkadaşları da bileşiği keşfetti ve ona rubidomisin adını verdi. Daunorubisin uluslararası isim olarak kabul edilmiştir. Başlangıçta murin tümörlerine karşı aktiviteye sahip olduğu görüldü ve daha sonra klinik deneylerde lösemi ve lenfomalara karşı aktif olduğu bulundu .
Doksorubisin, mutasyona uğramış bir S. peucetius varyantından (var. caesius ) izole edildi . Daunorubisinden sadece karbon 14 pozisyonunda bir hidroksil grubunun eklenmesiyle farklıdır. Bu modifikasyon, ilacın aktivitesini büyük ölçüde değiştirerek onu çok çeşitli katı tümörler, lösemi ve lenfomalara karşı oldukça etkili hale getirir. Yeni antrasiklinlerin yargılandığı standarttır.
İlk antrasiklinler o kadar başarılıydı ki , geliştirilmiş terapötik uygulamalara sahip bileşikleri bulma girişimlerinde binlerce analog üretildi. Dünya çapında kullanım için sadece epirubisin ve idarubisin benimsenmiştir. Epirubisin, doksorubisine benzer aktiviteye sahiptir, ancak kardiyotoksik yan etkileri azaltmıştır. İdarubisin, daunorubisinin yağda çözünen bir çeşididir ve oral olarak biyoyararlıdır.
Birkaç araştırmacı grubu, antrasiklinlerin polisiklik aromatik kromoforunu koruyan (DNA'ya karışmayı destekleyen) ve şeker kalıntısını basit yan zincirlerle değiştiren bileşikler tasarlamaya odaklandı. Bu, bir antrasenedion bileşiği olarak sınıflandırılan ve klinikte çeşitli kanserlerin tedavisi için kullanılan mitoksantronun tanımlanmasına yol açmıştır. Disakkarit analoglarının antikanser aktivitesini koruduğu gösterilmiştir ve etki mekanizmalarına göre daha fazla araştırılmaktadır.
Antrasiklinlerin keşfinin üzerinden 50 yıl geçmesine ve kanserler için hedefe yönelik tedavilerin geliştirilmesindeki son gelişmelere rağmen, meme kanseri hastalarının yaklaşık %32'si, yaşlı lenfoma hastalarının %57-70'i ve çocukluk çağı kanserlerinin %50-60'ı Hastalar antrasiklinlerle tedavi edilir. Bazı kanserler neoadjuvan antrasiklin bazlı rejimlerden yararlanır ve bunlar, hedeflenebilecek mevcut reseptörlerin olmaması nedeniyle hedefe yönelik tedavilere iyi yanıt vermeyen üçlü negatif meme kanserlerini içerir. Üçlü negatif olmayan meme kanseri hastalarıyla karşılaştırıldığında, üçlü negatif meme kanseri hastaları, iyileştirilmiş uzun vadeli sonuçları öngörmek için kullanılan bir gösterge olan antrasiklin kullanımıyla daha iyi yanıt oranı ve daha yüksek patolojik yanıt oranı göstermiştir.
Klinik denemeler
Antrasiklinler, en yaygın kullanılan kemoterapötik ajanlardan bazıları olmaya devam etmektedir, ancak potansiyelleri, doz sınırlayıcı toksisiteleri ile sınırlıdır. Halihazırda, daha iyi anti-tümör etkinliği olan veya farklı nanoteknoloji tabanlı ilaç dağıtım sistemleri kullanılarak yan etkileri azaltılmış antrasiklinlerin araştırılmasında yürütülen birçok çalışma bulunmaktadır.
Hareket mekanizması

Antrasiklinler, hücresel bileşenlerle etkileşimleri ve hücresel süreçler üzerindeki etkileri nedeniyle geniş çapta incelenmiştir. Bu, kültürlenmiş hücrelerde ve tüm hayvan sistemlerinde yapılan çalışmaları içerir. Bilimsel literatürde sayısız ilaç-hücresel etkileşim belgelenmiştir ve bunlar hedef hücrelerin özelliklerine, ilaç dozuna ve üretilen ilaç ara maddelerine göre değişiklik gösterir. Yapay etki mekanizmaları gözlemlenebildiğinden, klinik olarak ilgili ilaç konsantrasyonlarında meydana gelen aşağıdaki mekanizmalar en önemlileridir.
DNA Interkalasyonu
Antrasiklinler hücreler tarafından kolayca alınır ve çekirdeğe yerleşir . Antrasiklinlerin kromofor kısmı, aralayıcı fonksiyona sahiptir ve bitişik DNA baz çifti arasına girer. Araya girme işlevi, yüksek oranda replike olan hücrelerde DNA ve RNA sentezini inhibe eder, ardından transkripsiyon ve replikasyon işlemlerini bloke eder.
Topoizomeraz II zehiri
Bu, topoizomeraz-II aracılı toksisite klinik olarak ilgili ilaç konsantrasyonlarında belirgin olduğundan, antrasiklinlerin etkisini açıklamak için açık ara en çok kabul edilen mekanizmadır. Topoizomeraz-II, geçici çift sarmallı DNA (dsDNA) kırılmaları yaratan ve DNA süper bobinlerinin burulmasını yönettikten sonra bunları yeniden kapatan bir enzimdir . DNA'ya eklenen antrasiklinler, kararlı bir antrasiklin-DNA-topoizomeraz II üçlü kompleksi oluşturur, böylece enzimi "zehirler" ve çift sarmallı DNA kırılmalarının yeniden bağlanmasını engeller. Bu topoizomeraz-II aracılı DNA hasarı, daha sonra büyümenin durdurulmasını teşvik eder ve DNA onarım makinelerini çalıştırır. Onarım işlemi başarısız olduğunda, lezyonlar programlanmış hücre ölümünü başlatır .
Reaktif oksijen türleri
Antrasiklinlerin kinon kısmı, sitokrom P450 redüktaz , NADH dehidrojenaz ve ksantin oksidaz gibi oksidoredüktif enzimlerin varlığında aşırı reaktif oksijen türleri (ROS) oluşturmak için redoks reaksiyonlarına girebilir . Dönüştürme kinon semikuinonun aktif oluşturmak üzere oksijen ile reaksiyona giren serbest radikaller ürettiğini süperoksitlerin , hidroksil radikalleri ve peroksitler. Ek olarak, hücresel demirin mevcudiyeti redoks reaksiyonlarını katalize eder ve ayrıca ROS üretir. Detoksifiye edilemeyen aşırı ROS, oksidatif stres, DNA hasarı ve lipid peroksidasyonu ile sonuçlanarak apoptozu tetikler.
DNA eklenti oluşumu
Antrasiklinler ayrıca daunosaminin 3'-amino'sundan guaninin ekzosiklik aminosuna bir aminal bağlantı yoluyla tek bir kovalent bağ ile DNA ile eklentiler oluşturabilir. Formaldehit salan ön ilaçlar kullanılarak hücre dışı formaldehit temini, kovalent DNA eklenti oluşumunu destekleyebilir. Bu tür eklentilerin GpC'ye özgü transkripsiyon faktörlerini bloke ettiği ve apoptotik tepkileri indüklediği gösterilmiştir.
Klinik etkileri
Yakın tarihli bir meta-analizden elde edilen sonuçlar, ya sentromer 17 kopyalanması ya da topoizomeraz-IIa'yı kodlayan gen olan TOP2A'da aberasyonları olan meme kanseri hastalarının antrasiklinleri içeren adjuvan kemoterapiden yararlandığına dair kanıt sağlar. Bu, HER2 amplifikasyonunu barındıran hasta alt gruplarını içermez. Bu çalışmadan elde edilen gözlemler, aynı zamanda, antrasiklinlerin tedavi stratejilerinden güvenli bir şekilde çıkarılabileceği hastaların belirlenmesine de olanak tanır.
Yan etkiler
Antrasiklin uygulamasına sıklıkla kliniklerde antrasiklin kullanımını sınırlayan advers ilaç reaksiyonları eşlik eder. Antrasiklinlerin iki ana doz sınırlayıcı toksisitesi, miyelosupresyon ve kardiyotoksisiteyi içerir . Neyse ki, terapötik sitokinlerin tanıtımı, miyelosupresyonun yönetimine izin verir. Bu nedenle, kardiyak yaralanma, antrasiklin bazlı anti-kanser ajanlarının en büyük dezavantajı olmaya devam etmektedir.
Antrasiklin aracılı kardiyotoksisite doza bağımlıdır ve kümülatiftir, kalbe verilen hasar ilk dozda meydana gelir ve ardından her antrasiklin döngüsünde birikir. Tanımlanmış dört tip antrasiklin ile ilişkili kardiyotoksisite vardır.
| Kardiyotoksisite türleri | sunum zamanı | Belirtiler |
|---|---|---|
| Akut | İlaç uygulaması sırasında ve hemen sonrasında | Vazodilatasyon, hipotansiyon, geçici kalp ritmi bozuklukları |
| subkronik | 1-3 gün ilaç uygulamasından sonra | perikardit-miyokardit |
| Erken kronik | Antrasiklin tedavisini tamamladıktan sonra 1 yıldan az | Dilate kardiyomiyopati, kısıtlayıcı kardiyomiyopati (yaygın olmayan), sol ventrikül kontraktil disfonksiyonu, konjestif kalp yetmezliği |
| Gecikmeli/geç başlangıçlı kronik | Antrasiklin tedavisini tamamladıktan sonra 1 yıldan fazla | Kısıtlayıcı kardiyomiyopati, dilate kardiyomiyopati, konjestif kalp yetmezliği |
Klinikte, konjestif kalp yetmezliğinin gelişmesini önlemek için antrasiklinler için önerilen maksimum kümülatif doz belirlenir . Hastalar 400 mg / m doksorubisin alındığında Bir örnek olarak konjestif kalp yetmezliği insidansı% 4.7,% 26 ve% 48 sırasıyla 2 , 550 mg / m 2 ve mg / 700 m 2 . Bu nedenle, kullanım süresi kümülatif doksorubisin maruz 400-450 mg / m ile sınırlıdır 2 doksorubisin toleransın bakımından değişkenlik bireyler arasında var olmasına rağmen,% 5'ten daha az konjestif kalp yetmezliği sıklığını azaltmak için. Antrasiklinlerin neden olduğu kardiyak hasarın derecesini etkileyen risk faktörleri arasında genetik değişkenlik, yaş (düşük veya yüksek yaş grupları), kardiyotoksik ilaçlarla önceki tedaviler ve kalp hastalıkları öyküsü bulunur. Çocuklar, olgunlaşmamış kalbin gelişimini tehlikeye atabilecek antrasiklin aktivitesi nedeniyle özellikle risk altındadır.
Başlangıç antrasiklin dozlarına yanıt olarak meydana gelen kalp hasarı, uygulamadan hemen sonra troponin seviyesindeki bir artış ile tespit edilebilir . Biyopsi ayrıca, kalp ultrastrüktür değişikliklerini değerlendirerek kardiyak hasarın erken tespit edilmesini sağlar. Kümülatif antrasiklin dozları almak, sol ventrikül disfonksiyonuna neden olur ve sürekli doz ile 2D ekokardiyografi ve zorlanma hızı görüntüleme gibi invaziv olmayan tekniklerle klinik olarak tespit edilebilen belirli bir eşiğe ulaşır . Daha hassas görüntüleme teknikleri ve biyobelirteçler geliştirmedeki ilerlemeler , kardiyotoksisitenin erken saptanmasına olanak tanır ve antrasiklin aracılı kardiyotoksisiteyi önlemek için kardiyoprotektif müdahaleye izin verir.
Kalbin antrasiklinlere baskın duyarlılığı, kısmen antrasiklinlerin tercihli mitokondriyal yerleşiminden kaynaklanmaktadır. Bu, kalp dokusu hücre başına nispeten yüksek sayıda mitokondri içerdiğinden, kalp mitokondriyal zarında bulunan bir fosfolipid olan antrasiklinler ve kardiyolipin arasındaki yüksek afinite etkileşimine atfedilir. Kalp dokusu ayrıca, antrasiklin aracılı ROS'u detoksifiye etmek için katalaz ve süperoksit dismutaz gibi düşük düzeyde antioksidan enzimler sergileyerek oksidatif strese karşı bozulmuş bir savunmaya sahiptir.
Antrasiklin kaynaklı kardiyak hasarı açıklayan mekanizmalar karmaşık ve birbiriyle ilişkilidir. İlk önce antrasiklinlerin neden olduğu oksidatif stresle ilişkili olduğu kabul edildi. Antrasiklin aracılı kardiyotoksisitenin antrasiklin-topoizomeraz IIb zehirlenmesinden kaynaklandığı ve aşağı yönde oksidatif strese yol açtığı daha yeni bir açıklama ortaya çıkmıştır.
Antrasiklinlere yanıt olarak kardiyak hasarın etkisini azaltmak için birkaç kardiyoprotektif strateji araştırılmıştır. Antrasiklinlerin lipozomal formülasyonları (aşağıda tartışılmıştır) kardiyak hasarı azaltmak için geliştirilmiş ve kullanılmıştır. Epirubisin ve idarubisin gibi diğer yeni antrasiklin analogları da olumsuz kardiyak olayları azaltmak için seçenekler sunar; bu analoglar, ana bileşiklere karşı üstün anti-kanser aktivitesi göstermede başarısız olmuştur. Bolus uygulamaya kıyasla 72 saat boyunca sürekli infüzyonu içeren alternatif bir ilaç uygulama yöntemi , bir miktar koruma sağlar ve yüksek kümülatif dozlar beklendiğinde kullanılabilir.
Antrasiklinler intravenöz olarak verildiğinde, enjeksiyon bölgelerinde kazara ekstravazasyona neden olabilir. Ekstravazasyon insidansının %0.1 ile %6 arasında değiştiği tahmin edilmektedir . Ekstravazasyon, doku nekrozu ve cilt ülserasyonu semptomları ile çevre dokularda ciddi komplikasyonlara neden olur. Deksrazoksan öncelikle antrasiklinlerin neden olduğu oksidatif stresi azaltmak için bir topoizomeraz II inhibitörü ve ayrıca bir şelatlama maddesi olarak hareket ederek ekstravazasyon sonrası antrasiklinleri tedavi etmek için kullanılır. Deksrazoksan da daha fazla 300 mg / m ile muamele edilmiştir metastatik meme kanserli hastalarda doksorubisin ile bir arada bir kardiyo-koruyucu bileşim olarak bir başarı ile kullanılan 2 Yüksek bir birleştirici ile ilgili yararlı bir etkiye sahip olacak şekilde de beklenen hastalarda doksorubisin doksorubisin dozları.
Kardiyoprotektif tedavilerin etkili olup olmadığını doğrulamak için yüksek kalitede kanıt yoktur. Deksrazoksanın kardiyoprotektif doğası üzerine yapılan çalışmalar, antrasiklin tedavisinin anti-tümör etkilerine müdahale etmeden kalp hasarını önleyebildiğine dair kanıtlar sunmaktadır. Antrasiklin tedavisi ile birlikte deksrazoksan verilen hastaların kalp yetmezliği riskleri, deksrazoksan içermeyen antrasiklinlerle tedavi edilenlere kıyasla azalmıştır. Yine de hayatta kalma üzerinde hiçbir etkisi yoktu.
Radyoetiketli doksorubisin, bir pilot çalışmada meme kanseri lezyon görüntüleme ajanı olarak kullanılmıştır. Bu radyokimyasal, 99m Tc-doksorubisin, kadın hastalarda meme tümörü lezyonlarına lokalizedir ve meme tümörlerinin görüntülenmesi için potansiyel bir radyofarmasötiktir.
Bazı durumlarda, antrasiklinler ilaç direncinin gelişmesi nedeniyle etkisiz olabilir . Birincil direnç (ilk tedaviye duyarsız yanıt) veya edinilmiş direnç (tedaviye tam veya kısmi yanıt gösterdikten sonra mevcut) olabilir. Antrasiklinlere direnç birçok faktörü içerir, ancak genellikle antrasiklinleri kanser hücrelerinden uzaklaştıran transmembran ilaç akış proteini P-glikoprotein (P-gp) veya çoklu ilaç direnç proteini 1'in ( MRP1 ) aşırı ekspresyonu ile ilgilidir . Büyük bir araştırma çabası, antrasikline dirençli hücreleri yeniden duyarlı hale getirmek için MRP1'e karşı inhibitörlerin tasarlanmasına odaklanmıştır, ancak bu tür ilaçların çoğu klinik deneyler sırasında başarısız olmuştur.
Lipozom bazlı klinik formülasyonlar
Lipozomlar , fosfolipidler veya kolesteroller ile bir veya daha fazla lipid çift tabakası ile oluşturulabilen küresel şekilli, fosfolipid veziküllerdir. Lipozomların hem hidrofobik hem de hidrofilik ilaç bileşiklerini kapsülleme yeteneği, lipozomların bu nano taşıyıcılarda bir dizi ilaç iletmek için etkili bir ilaç dağıtım sistemi (DDS) olmasına izin verdi.
Antrasiklinlerin lipozomal formülasyonları, antrasiklinlerin terapötik etkinliğini muhafaza etmek ve hatta geliştirmek için geliştirilmiştir ve aynı zamanda sağlıklı dokulara, özellikle kardiyotoksisiteye karşı sınırlayıcı toksisitelerini azaltır. Şu anda kliniklerde doksorubisinin iki lipozomal formülasyonu mevcuttur.
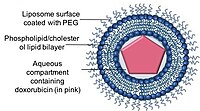
Doxil/Caelyx, FDA onaylı ilk lipozomal DDS'dir ve ilk olarak 1995 yılında AIDS ile ilişkili Kaposi sarkomunu tedavi etmek için kullanılmıştır ve şu anda tekrarlayan yumurtalık kanseri , artmış kardiyak riski olan metastatik meme kanseri ve multipl miyelom tedavisinde kullanılmaktadır . Doksorubisin, lipozom fosfolipidlerine kovalent olarak bağlı hidrofilik polimer polietilen glikol (PEG) ile kaplanmış tek lamelli lipozomlardan oluşan Stealth veya sterik olarak stabilize edilmiş lipozomlar olarak bilinen bir nano-taşıyıcı içinde kapsüllenir . PEG kaplama , ilaç bir amonyum sülfat kimyasal gradyan yoluyla nano-taşıyıcılar içinde stabil bir şekilde tutulurken opsonizasyona , hızlı temizlemeye karşı bir bariyer görevi görür . Nano taşıyıcıları bir ilaç dağıtım sistemi olarak kullanmanın büyük bir avantajı, nano taşıyıcıların, EPR etkisi yoluyla tümörlerin sızdıran damar sistemini ve onların bozulmuş lenfatik drenajını kullanma yeteneğidir.
Doxil uygulamasından sonra serbest doksorubisinin maksimum plazma konsantrasyonu, geleneksel doksorubisine kıyasla önemli ölçüde daha düşüktür ve düşük kardiyotoksisite profili için bir açıklama sağlar. Ancak Doxil , deride birikmesi nedeniyle Palmar-plantar eritrodisesteziye (PPE, el ve ayak sendromu) neden olabilir. Doxil 50 mg / m alt tolere edilebilir maksimum dozu (MTD) sahip olmasıdır 2 60 mg / m serbest doksorubisine göre her 4 haftada bir 2 her 3 haftada. Buna rağmen, kardiyoprotektif özelliklerinden dolayı Doxil için maksimum kümülatif doz, doksorubisine kıyasla hala daha yüksektir.
Myocet , Avrupa ve Kanada'da birinci basamak tedavi olarak metastatik meme kanseri hastalarında siklofosfamid ile kombinasyon halinde kullanım için onaylanmış başka bir pegile olmayan lipozom kapsüllü doksorubisin sitrat kompleksidir. Doksorubisin, 75 mg / m'lik bir maksimum tek bir doz olan hastalara verilmesinden hemen önce, lipozomlar içine yüklenen 2 her 3 haftada. Myocet, kardiyak toksisiteyi önemli ölçüde azaltırken, geleneksel doksorubisin ile benzer etkinliğe sahiptir.
| doksil | miyosit | Referanslar | |
|---|---|---|---|
| Lipozomların bileşimi | PEG-fosfolipid
fosfolipit Kolesterol |
fosfolipit
Kolesterol |
|
| Boy | 80 nm – 100 nm | 150 nm - 250 nm | |
| İlaç yükleme yöntemi | Amonyum tuzu gradyanı | sitrik asit gradyanı | |
| farmakokinetik | Doz: 10 mg / m tek doz 2 - 20 mg / m 2 pik plazma konsantrasyonu 7.4 uM - 15.3 uM
Eliminasyon yarı ömrü: 50,2 saat – 54,5 saat |
Doz: Tek 60 mg / m doza 2
Pik plazma konsantrasyonu: 16 μM Eliminasyon yarı ömrü: 16.4 saat |
|
| Klinik endikasyon | AIDS ile ilişkili Kaposi sarkomu, tekrarlayan yumurtalık kanseri ve metastatik meme kanseri | Metastatik meme kanseri |
Olumsuz ilaç etkileşimleri
Antrasiklinlerle ilaç etkileşimleri karmaşık olabilir ve antrasiklin etkisine, yan etkilerine veya metabolizmasına bağlı olabilir. Sitokrom P450 veya diğer oksidazları inhibe eden ilaçlar, antrasiklinlerin klirensini azaltabilir, dolaşımdaki yarı ömürlerini uzatabilir, bu da kardiyotoksisiteyi ve diğer yan etkileri artırabilir. Antrasiklinler antibiyotik görevi görerek mesane kanseri için Bacillus Calmette-Guerin tedavisi gibi canlı kültür tedavilerinin etkinliğini azaltabilir . Antrasiklinler miyelosupresör olarak hareket ettikleri için bağışıklık sistemini inhibe ederek aşıların etkinliğini azaltabilirler.
Birkaç etkileşim özellikle klinik öneme sahiptir. Deksrazoksan, antrasiklinlerin kardiyotoksisitesini veya ekstravazasyon hasarını hafifletmek için kullanılabilse de, etkinliklerini de azaltabilir ve tavsiye, ilk antrasiklin tedavisinden sonra deksrazoksan tedavisine başlanmamasıdır. Trastuzumab (meme kanserini tedavi etmek için kullanılan bir HER2 antikoru), antrasiklin ile trastuzumab uygulaması arasında bir zaman aralığı uygulanarak etkileşim en aza indirilebilse de, antrasiklinlerin kardiyotoksisitesini artırabilir . Taksanlar (dosetaksel hariç) antrasiklin metabolizmasını azaltarak antrasiklinlerin serum konsantrasyonlarını artırabilir. Tavsiye, taksanlarla kombinasyon tedavisi gerekiyorsa, önce antrasiklinlerle tedavi etmektir.
Ayrıca bakınız
Referanslar
![]() Bu makale, CC BY 4.0 lisansı ( 2019 ) ( inceleme raporları ) kapsamında aşağıdaki kaynaktan uyarlanmıştır :
Alison Cheong; Sean McGrath; Suzanne Cutts (6 Aralık 2018). "Antrasiklinler". WikiJournal of Medicine . 5 (1): 1. doi : 10.15347/WJM/2018.001 . ISSN 2002-4436 . Vikiveri Q60638523 .
Bu makale, CC BY 4.0 lisansı ( 2019 ) ( inceleme raporları ) kapsamında aşağıdaki kaynaktan uyarlanmıştır :
Alison Cheong; Sean McGrath; Suzanne Cutts (6 Aralık 2018). "Antrasiklinler". WikiJournal of Medicine . 5 (1): 1. doi : 10.15347/WJM/2018.001 . ISSN 2002-4436 . Vikiveri Q60638523 .
Notlar
Dış bağlantılar
-
 Medya ile ilgili Antrasiklinler Wikimedia Commons
Medya ile ilgili Antrasiklinler Wikimedia Commons