amfetamin - Amphetamine
 | |
 | |
| Klinik veriler | |
|---|---|
| Telaffuz |
/ Æ m f ɛ t ə m Ben bir n / ( dinleme ) |
| Ticari isimler | Evekeo, Adderall , diğerleri |
| Diğer isimler | a-metilfenetilamin |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a616004 |
| Lisans verileri | |
| Bağımlılık sorumluluğu |
Ilıman |
| Bağımlılık sorumluluğu |
Ilıman |
Yönetim yolları |
Tıbbi: oral , intravenöz Rekreasyonel: oral , insuflasyon , rektal , intravenöz , intramüsküler |
| İlaç sınıfı | CNS uyarıcı , anorektik |
| ATC kodu | |
| Hukuki durum | |
| Hukuki durum | |
| Farmakokinetik veriler | |
| biyoyararlanım | Ağızdan: %75-100 |
| Protein bağlama | %20 |
| Metabolizma | CYP2D6 , DBH , FMO3 |
| metabolitler | 4-hidroksiamfetamin , 4-hidroksinorefedrin , 4-hidroksifenilaseton , benzoik asit , hippurik asit , norefedrin , fenilaseton |
| Etki başlangıcı |
IR dozlama: 30–60 dakika XR dozlama: 1,5–2 saat |
| Eliminasyon yarı ömrü |
D-amph : 9–11 saat L-amph : 11–14 saat pH'a bağlı: 7–34 saat |
| Hareket süresi |
IR dozlama: 3–6 saat XR dozlama: 8–12 saat |
| Boşaltım | Öncelikle böbrek ; pH'a bağlı aralık: %1–75 |
| tanımlayıcılar | |
| |
| CAS numarası | |
| PubChem Müşteri Kimliği | |
| IUPHAR/BPS | |
| İlaç Bankası | |
| Kimyasal Örümcek | |
| ÜNİİ | |
| fıçı | |
| chebi | |
| CHEMBL | |
| NIAID ChemDB | |
| CompTox Panosu ( EPA ) | |
| ECHA Bilgi Kartı |
100.005.543 |
| Kimyasal ve fiziksel veriler | |
| formül | Cı- 9 H 13 N |
| Molar kütle | 135.210 g·mol -1 |
| 3B model ( JSmol ) | |
| kiralite | Rasemik karışım |
| Yoğunluk | 0,936 g / cc 3. 25 ° C'de |
| Erime noktası | 11,3 °C (52,3 °F) (tahmin edilen) |
| Kaynama noktası | 760 mmHg'de 203 °C (397 °F) |
| |
| |
| (Doğrulayın) | |
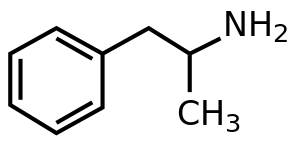
Amfetamin (sözleşmeli bir lfa - m etil pH en ve hyl amin ) a, merkezi sinir sistemi (MSS) uyarıcı tedavisinde kullanılan , dikkat eksikliği hiperaktivite bozukluğu (ADHD), narkolepsi ve obezite . Amfetamin 1887'de keşfedildi ve iki enantiyomer olarak var : levoamfetamin ve dekstroamfetamin . Amfetamin , iki enantiyomerin, levoamfetamin ve dekstroamfetamin'in saf amin formlarında eşit parçaları olan spesifik bir kimyasal olan rasemik serbest bazı ifade eder . Terim, enantiyomerlerin herhangi bir kombinasyonunu veya tek başına herhangi birini belirtmek için sıklıkla gayri resmi olarak kullanılır. Tarihsel olarak, burun tıkanıklığı ve depresyonu tedavi etmek için kullanılmıştır. Amfetamin ayrıca atletik bir performans arttırıcı ve bilişsel güçlendirici olarak ve eğlence amaçlı olarak afrodizyak ve coşku verici olarak kullanılır . Bu bir olan reçeteli ilaç birçok ülkede ve yetkisiz bulundurmak ve amfetamin dağılımı genellikle sıkı önemli sağlık ile ilişkili riski nedeniyle kontrol edilir eğlence amaçlı kullanımıyla .
İlk amfetamin ilacı, çeşitli koşulları tedavi etmek için kullanılan bir marka olan Benzedrine idi. Şu anda farmasötik amfetamin , rasemik amfetamin, Adderall , dekstroamfetamin veya aktif olmayan ön ilaç lisdexamfetamin olarak reçete edilmektedir . Amfetamin , norepinefrin ve dopamin nörotransmitter sistemlerini hedef alan en belirgin etkileri ile beyindeki monoamin ve uyarıcı sinir iletimini arttırır .
Terapötik dozlarda, amfetamin öfori , cinsel istekte değişiklik , artan uyanıklık ve gelişmiş bilişsel kontrol gibi duygusal ve bilişsel etkilere neden olur . İyileştirilmiş reaksiyon süresi, yorgunluk direnci ve artan kas gücü gibi fiziksel etkilere neden olur. Daha yüksek dozlarda amfetamin bilişsel işlevi bozabilir ve hızlı kas yıkımına neden olabilir . Bağımlılık , yoğun eğlence amaçlı amfetamin kullanımıyla ciddi bir risktir, ancak terapötik dozlarda uzun süreli tıbbi kullanımdan kaynaklanması olası değildir. Çok yüksek dozlar, uzun süreli kullanımlarda bile terapötik dozlarda nadiren ortaya çıkan psikoza (örn., sanrılar ve paranoya ) neden olabilir. Rekreasyonel dozlar genellikle reçete edilen terapötik dozlardan çok daha fazladır ve çok daha büyük ciddi yan etki riski taşır.
Amfetamin, fenetilamin sınıfına aittir . Aynı zamanda, bupropion , katinon , MDMA ve metamfetamin gibi önde gelen maddeleri içeren ikame edilmiş amfetaminler olan kendi yapısal sınıfının ana bileşiğidir . Fenetilamin sınıfının bir üyesi olarak amfetamin, doğal olarak oluşan eser amin nöromodülatörleri, özellikle de her ikisi de insan vücudunda üretilen fenetilamin ve N- metilfenetilamin ile kimyasal olarak ilişkilidir . Fenetilamin, amfetaminin ana bileşiği iken, N- metilfenetilamin , yalnızca metil grubunun yerleşiminde farklılık gösteren, amfetaminin konumsal bir izomeridir .
kullanır
Tıbbi
Amfetamin, dikkat eksikliği hiperaktivite bozukluğu (DEHB), narkolepsi (bir uyku bozukluğu) ve obeziteyi tedavi etmek için kullanılır ve bazen geçmiş tıbbi endikasyonları , özellikle depresyon ve kronik ağrı için etiket dışı olarak reçete edilir . Bazı hayvan türlerinde yeterince yüksek dozlarda uzun süreli amfetamin maruziyetinin anormal dopamin sistemi gelişimi veya sinir hasarı ürettiği bilinmektedir , ancak DEHB'li insanlarda terapötik dozlarda farmasötik amfetaminlerin beyin gelişimini ve sinir büyümesini iyileştirdiği görülmektedir. Yorumlar , manyetik rezonans görüntüleme (MRI) çalışmalar amfetamin ile uzun süreli tedavi beyin yapısı ve işlevi anormallikler DEHB öznelerdeki azalır ve sağ gibi beynin çeşitli bölümlerinde bölgesi işlevini artırır göstermektedir kuyruk çekirdeği arasında bazal ganglion .
Klinik uyarıcı araştırmaların incelemeleri, DEHB tedavisi için uzun süreli sürekli amfetamin kullanımının güvenliğini ve etkinliğini ortaya koymuştur. DEHB tedavisine yönelik sürekli uyarıcı tedavinin 2 yılı kapsayan randomize kontrollü çalışmaları , tedavinin etkinliğini ve güvenliğini göstermiştir. İki inceleme, DEHB için uzun süreli sürekli uyarıcı tedavinin, DEHB'nin temel semptomlarını (yani, hiperaktivite, dikkatsizlik ve dürtüsellik) azaltmak, yaşam kalitesini ve akademik başarıyı arttırmak ve çok sayıda işlevsellikte iyileştirmeler üretmek için etkili olduğunu göstermiştir. akademisyenler, antisosyal davranış, araba kullanma, tıbbi olmayan uyuşturucu kullanımı, obezite, meslek, benlik saygısı, hizmet kullanımı (yani, akademik, mesleki, sağlık, finansal ve yasal hizmetler) ve sosyal işlevle ilgili 9 sonuç kategorisindeki sonuçlar . Bir inceleme, DEHB için ortalama 4.5 IQ puanı artışı, dikkatte devam eden artışlar ve yıkıcı davranışlarda ve hiperaktivitede devam eden düşüşler bulan, DEHB için dokuz aylık randomize kontrollü bir amfetamin tedavisi denemesinin altını çizdi . Başka bir inceleme, bugüne kadar yapılmış en uzun takip çalışmalarına dayanarak, çocukluk döneminde başlayan yaşam boyu uyarıcı tedavinin DEHB belirtilerini kontrol etmede sürekli olarak etkili olduğunu ve yetişkinlikte madde kullanım bozukluğu geliştirme riskini azalttığını göstermiştir .
Mevcut DEHB modelleri, beynin bazı nörotransmitter sistemlerindeki fonksiyonel bozukluklarla ilişkili olduğunu ileri sürmektedir ; Bu fonksiyonel bozuklukları bozulmuş dahil dopamin nörotransmisyonu mezokortikolimbik çıkıntı ve norepinefrin ile ilgili noradrenerjik çıkıntılar nörotransmisyon locus coeruleus için prefrontal kortekste . Metilfenidat ve amfetamin gibi psikostimulanlar , bu sistemlerdeki nörotransmitter aktivitesini artırdıkları için DEHB tedavisinde etkilidir. Bu uyarıcıları kullananların yaklaşık %80'i DEHB semptomlarında iyileşme görüyor. Uyarıcı ilaçlar kullanan DEHB'li çocuklar genellikle akranları ve aile üyeleriyle daha iyi ilişkilere sahiptir, okulda daha iyi performans gösterir, daha az dikkati dağılabilir ve dürtüseldir ve daha uzun dikkat süreleri vardır. Cochrane nedeniyle olumsuz kısa vadeli çalışmalar bunlar olmayan uyarıcı ilaçlar daha yüksek bırakma oranları var bu ilaçların şiddetini azaltmak olduğunu göstermiştir, fakat belirtti ilaç amfetamin olan çocuklarda, ergenlerde DEHB tedavisinde ilgili incelemeler ve yetişkinler yan etkiler . Tourette sendromu gibi tik bozuklukları olan çocuklarda DEHB tedavisine ilişkin bir Cochrane incelemesi, uyarıcıların genel olarak tikleri daha da kötüleştirmediğini, ancak yüksek dozlarda dekstroamfetamin bazı kişilerde tikleri şiddetlendirebileceğini göstermiştir.
Performansı artırma
Bilişsel performans
2015 yılında, sistematik bir inceleme ve yüksek kaliteli klinik çalışmaların bir meta-analizi , düşük (terapötik) dozlarda kullanıldığında, amfetaminin, çalışma belleği , uzun süreli epizodik bellek , engelleyici kontrol , ve normal sağlıklı yetişkinlerde dikkatin bazı yönleri ; amfetamin, bu biliş arttırıcı etkilerinin kısmen aracılık ettiği bilinmektedir dolaylı aktivasyonu hem de D dopamin reseptörü 1 ve adrenoseptör a 2 olarak prefrontal kortekste . 2014'te yapılan sistematik bir inceleme, düşük dozlarda amfetaminin aynı zamanda bellek sağlamlaştırmayı iyileştirdiğini ve bunun sonucunda bilginin daha iyi hatırlanmasına yol açtığını buldu . Terapötik amfetamin dozları, aynı zamanda, tüm bireylerde çalışma belleğindeki gelişmelere aracılık eden bir etki olan kortikal ağ verimliliğini de arttırır. Amfetamin ve diğer DEHB uyarıcıları ayrıca görev belirginliğini (bir görevi gerçekleştirme motivasyonu) iyileştirir ve uyarılmayı (uyanıklığı) artırır , dolayısıyla hedefe yönelik davranışı teşvik eder. Amfetamin gibi uyarıcılar, zor ve sıkıcı görevlerde performansı artırabilir ve bazı öğrenciler tarafından bir çalışma ve test çözme yardımı olarak kullanılır. Kendileri tarafından bildirilen yasadışı uyarıcı kullanımına ilişkin çalışmalara dayanarak , üniversite öğrencilerinin % 5-35'i, eğlence amaçlı uyuşturuculardan ziyade öncelikle akademik performansı artırmak için kullanılan yönlendirilmiş DEHB uyarıcıları kullanmaktadır. Bununla birlikte, terapötik aralığın üzerindeki yüksek amfetamin dozları, işleyen hafızayı ve bilişsel kontrolün diğer yönlerini etkileyebilir.
Fiziksel performans
Amfetamin, bazı sporcular tarafından, artan dayanıklılık ve uyanıklık gibi psikolojik ve atletik performansı arttırıcı etkileri için kullanılır ; ancak, üniversite, ulusal ve uluslararası dopingle mücadele kuruluşları tarafından düzenlenen spor etkinliklerinde tıbbi olmayan amfetamin kullanımı yasaktır. Sağlıklı insanlarda oral terapötik dozlarda, amfetaminin, reaksiyon süresini iyileştirirken kas gücünü , hızlanmasını, anaerobik koşullarda atletik performansı ve dayanıklılığı (yani yorgunluğun başlamasını geciktirdiği ) arttırdığı gösterilmiştir . Amfetamin, esas olarak merkezi sinir sisteminde dopaminin geri alımının engellenmesi ve salınması yoluyla dayanıklılığı ve reaksiyon süresini iyileştirir . Amfetamin ve diğer dopaminerjik ilaçlar ayrıca, bir "güvenlik anahtarını" geçersiz kılarak algılanan eforun sabit seviyelerinde güç çıkışını arttırır ve normalde limit dışı olan bir rezerv kapasitesine erişmek için çekirdek sıcaklık limitinin artmasına izin verir . Terapötik dozlarda amfetaminin yan etkileri atletik performansı engellemez; bununla birlikte, çok daha yüksek dozlarda amfetamin, hızlı kas yıkımı ve yüksek vücut ısısı gibi performansı ciddi şekilde bozan etkilere neden olabilir .
Kontrendikasyonlar
Göre Uluslararası Kimyasal Güvenlik Programı (IPCS) ve Amerika Birleşik Devletleri Gıda ve İlaç Dairesi (USFDA), amfetamin olduğu kontrendike öyküsü olan kişilerde uyuşturucu bağımlılığı , kardiyovasküler hastalıklar , şiddetli ajitasyon veya şiddetli anksiyete. Ayrıca ilerlemiş arterioskleroz (atardamarların sertleşmesi), glokom (artan göz basıncı), hipertiroidizm (aşırı tiroid hormonu üretimi) veya orta ila şiddetli hipertansiyonu olan kişilerde kontrendikedir . Bu kurumlar, diğer uyarıcılara karşı alerjik reaksiyonlar yaşayan veya monoamin oksidaz inhibitörleri (MAOI'ler) alan kişilerin, amfetamin ve monoamin oksidaz inhibitörlerinin güvenli bir şekilde eşzamanlı kullanımı belgelenmiş olmasına rağmen, amfetamin almamaları gerektiğini belirtmektedir. Bu kurumlar ayrıca anoreksiya nervoza , bipolar bozukluk , depresyon, hipertansiyon, karaciğer veya böbrek sorunları, mani , psikoz , Raynaud fenomeni , nöbetler , tiroid sorunları, tikler veya Tourette sendromu olan herkesin amfetamin alırken semptomlarını izlemesi gerektiğini belirtmektedir. İnsan çalışmalarından elde edilen kanıtlar, terapötik amfetamin kullanımının fetüs veya yenidoğanlarda gelişimsel anormalliklere neden olmadığını (yani, bir insan teratojeni olmadığını ), ancak amfetamin kötüye kullanımının fetüs için risk oluşturduğunu göstermektedir. Amfetaminin anne sütüne geçtiği de gösterilmiştir, bu nedenle IPCS ve USFDA, annelere bu ilacı kullanırken emzirmekten kaçınmalarını tavsiye eder. Geri dönüşümlü büyüme bozuklukları potansiyeli nedeniyle, USFDA, bir amfetamin ilacı reçete edilen çocukların ve ergenlerin boy ve kilosunun izlenmesini tavsiye eder.
Yan etkiler
Olumsuz yan etkiler amfetaminin çok ve çeşitlidir ve kullanılan amfetamin miktarı yan etkilerin ihtimalini ve şiddetinin belirlenmesi birincil faktör olmaktadır. Adderall , Dexedrine ve bunların jenerik eşdeğerleri gibi amfetamin ürünleri , şu anda uzun süreli terapötik kullanım için USFDA tarafından onaylanmıştır. Amfetaminin eğlence amaçlı kullanımı genellikle çok daha büyük dozları içerir ve tedavi amaçlı kullanılan dozlara göre ciddi yan etki riski daha fazladır.
Fiziksel
Kardiyovasküler yan etkiler, vazovagal yanıttan kaynaklanan hipertansiyon veya hipotansiyon , Raynaud fenomeni (ellere ve ayaklara kan akışının azalması) ve taşikardi (artmış kalp hızı) içerebilir . Erkeklerde cinsel yan etkiler, erektil disfonksiyon , sık ereksiyonlar veya uzun süreli ereksiyonları içerebilir . Gastrointestinal yan etkiler karın ağrısı , kabızlık , ishal ve mide bulantısını içerebilir . Diğer potansiyel fiziksel yan etkiler arasında iştah kaybı , bulanık görme , ağız kuruluğu , dişlerin aşırı gıcırdaması , burun kanaması, aşırı terleme, rinitis medicamentosa (ilaca bağlı burun tıkanıklığı), düşük nöbet eşiği , tikler (bir tür hareket bozukluğu) ve kilo kaybı . Tipik farmasötik dozlarda tehlikeli fiziksel yan etkiler nadirdir.
Amfetamin medüller solunum merkezlerini uyarır, daha hızlı ve daha derin nefesler üretir. Normal bir insanda terapötik dozlarda bu etki genellikle fark edilmez, ancak solunum zaten tehlikeye girdiğinde belirgin olabilir. Amfetamin ayrıca idrara çıkmayı kontrol eden kas olan idrar kesesi sfinkterinde kasılmaya neden olur ve bu da idrar yapma zorluğuna neden olabilir. Bu etki, yatak ıslatma ve mesane kontrolünün kaybının tedavisinde faydalı olabilir . Amfetaminin gastrointestinal sistem üzerindeki etkileri tahmin edilemez. Bağırsak aktivitesi yüksekse, amfetamin gastrointestinal motiliteyi (içeriğin sindirim sisteminde hareket etme hızı) azaltabilir ; bununla birlikte amfetamin , yolun düz kası gevşediğinde motiliteyi artırabilir . Amfetamin ayrıca hafif bir analjezik etkiye sahiptir ve opioidlerin ağrı giderici etkilerini artırabilir .
2011 yılında USFDA tarafından yaptırılan araştırmalar, çocuklarda, genç yetişkinlerde ve yetişkinlerde ciddi olumsuz kardiyovasküler olaylar ( ani ölüm , kalp krizi ve felç ) ile amfetamin veya diğer DEHB uyarıcılarının tıbbi kullanımı arasında bir ilişki olmadığını göstermektedir. Bununla birlikte, amfetamin ilaçları, kardiyovasküler hastalığı olan kişilerde kontrendikedir .
Psikolojik
Normal terapötik dozlarda, amfetamin en yaygın psikolojik yan etkiler arasında artmış uyanıklık , endişe, konsantrasyon , inisiyatif, kendine güven ve sosyallik, dalgalanmalara ( sevinçli ruh hafif takiben depresif ruh hali ), uykusuzluk ya da uyanıklığı ve yorgunluk hissi azalmıştır . Daha az görülen yan etkiler arasında kaygı , libidoda değişiklik , büyüklenme , sinirlilik , tekrarlayan veya takıntılı davranışlar ve huzursuzluk yer alır; bu etkiler kullanıcının kişiliğine ve mevcut zihinsel durumuna bağlıdır. Ağır kullanıcılarda amfetamin psikozu (örneğin, sanrılar ve paranoya ) ortaya çıkabilir. Çok nadir olmakla birlikte, bu psikoz, uzun süreli tedavi sırasında terapötik dozlarda da ortaya çıkabilir. USFDA'ya göre, uyarıcıların saldırgan davranış veya düşmanlık ürettiğine dair "sistematik bir kanıt yoktur".
Amfetaminin, terapötik dozlar alan insanlarda koşullu bir yer tercihi ürettiği de gösterilmiştir ; bu, bireylerin daha önce amfetamin kullandıkları yerlerde zaman geçirme tercihi edindikleri anlamına gelir.
Pekiştirme bozuklukları
Bağımlılık
| Bağımlılık ve bağımlılık sözlüğü | |
|---|---|
| |
| Transkripsiyon faktörü sözlüğü | |
|---|---|
| |
|
|
Bağımlılık , eğlence amaçlı yoğun amfetamin kullanımıyla ciddi bir risktir, ancak terapötik dozlarda uzun süreli tıbbi kullanımdan kaynaklanma olasılığı düşüktür; aslında, DEHB için çocuklukta başlayan yaşam boyu uyarıcı tedavi, yetişkinlikte madde kullanım bozuklukları geliştirme riskini azaltır . Patolojik aşırı aktivasyonu mezolimbik yolu , bir dopamin yolunun bağlayan ventral tegmental alan için nucleus accumbens'inde , amfetamin bağımlılığı merkezi bir rol oynar. Sık sık Bireyler kendilerine uygulamalarına yüksek dozlarda amfetamin yüksek dozlarda kronik kullanım için, bir amfetamin bağımlılığı yakalanma riski yüksek olan kademeli düzeyini artırmak accumbal ΔFosB , bağımlılığı için bir "moleküler anahtar" ve "ana kontrol proteini". Çekirdek ΔFosB'yi yeterince aşırı eksprese ettiğinde, ekspresyonunda daha fazla artışla bağımlılık davranışının (yani kompulsif uyuşturucu arama) şiddetini artırmaya başlar. Şu anda amfetamin bağımlılığını tedavi etmek için etkili ilaçlar bulunmamakla birlikte, düzenli olarak sürekli aerobik egzersiz yapmak, böyle bir bağımlılık geliştirme riskini azaltıyor gibi görünmektedir. Düzenli olarak sürekli aerobik egzersizi de amfetamin bağımlılığı için etkili bir tedavi gibi görünmektedir; egzersiz terapisi klinik tedavi sonuçlarını iyileştirir ve bağımlılık için davranışsal terapilerle birlikte yardımcı bir terapi olarak kullanılabilir .
biyomoleküler mekanizmalar
Aşırı dozlarda amfetamin kronik kullanımı içinde değişikliklere neden olmakta, gen ekspresyonu içinde mezokortikolimbik projeksiyon aracılığıyla ortaya çıkan, transkripsiyonel ve epigenetik mekanizmalar. Bu değişiklikleri üreten en önemli transkripsiyon faktörleri Delta FBJ murin osteosarkom viral onkogen homolog B ( ΔFosB ), cAMP yanıt elemanı bağlayıcı protein ( CREB ) ve nükleer faktör-kappa B'dir ( NF-κB ). ΔFosB için ΔFosB bağımlılığı en önemli biyomoleküler bir mekanizma olduğu aşırı (yani, belirgin bir gen ile ilgili üreten gen ekspresyonunun anormal derecede yüksek düzeyde fenotipi ) içinde D1 tipi orta spinal nöronların içinde nucleus accumbens olan gerekli ve yeterli bir çoğu için sinirsel adaptasyonlar ve bağımlılıkla ilgili çoklu davranışsal etkileri (örneğin, ödül duyarlılığı ve artan ilaç kendi kendine tatbikat) düzenler . ΔFosB yeterince aşırı ifade edildiğinde, ΔFosB ifadesinde daha fazla artışla giderek daha şiddetli hale gelen bir bağımlılık durumunu indükler. Alkol , kannabinoidler , kokain , metilfenidat , nikotin , opioidler , fensiklidin , propofol ve ikameli amfetaminlere bağımlılıkla ilişkilendirilmiştir .
ΔJunD , bir transkripsiyon faktörü ve G9A bir, histon metil transferaz enzimi, hem ifade ΔFosB fonksiyonunu ve inhibe artar karşı. Viral vektörlerle accumbens çekirdeğindeki ΔJunD'yi yeterince aşırı eksprese etmek, kronik ilaç kötüye kullanımında görülen nöral ve davranışsal değişikliklerin çoğunu tamamen bloke edebilir (yani, ΔFosB'nin aracılık ettiği değişiklikler). Benzer bir şekilde, belirgin bir artış olarak accumbal G9A hiper sonuçları histon 3 lizin Tortu, 9 dimetilasyon ( H3K9me2 arasında) ve bloklar indüksiyon ΔFosB aracılı nöral ve davranışsal plastisite ile meydana gelen bir kronik ilaç kullanımı ile, H3K9me2 aracılı baskı ait transkripsiyon faktörleri ΔFosB ve H3K9me2- için çeşitli ΔFosB transkripsiyonel hedeflerinin aracılı baskısı (örneğin, CDK5 ). ΔFosB ayrıca lezzetli yiyecekler, seks ve egzersiz gibi doğal ödüllere davranışsal tepkileri düzenlemede önemli bir rol oynar . Hem doğal ödüller hem de bağımlılık yapan ilaçlar ΔFosB ifadesini indüklediğinden (yani beynin daha fazlasını üretmesine neden olurlar), bu ödüllerin kronik olarak edinilmesi benzer patolojik bir bağımlılık durumuna neden olabilir. Sonuç olarak, ΔFosB, hem amfetamin bağımlılığında hem de aşırı cinsel aktivite ve amfetamin kullanımından kaynaklanan zorlayıcı cinsel davranışlar olan amfetamin kaynaklı cinsel bağımlılıklarda rol oynayan en önemli faktördür . Bu cinsel bağımlılıklar, dopaminerjik ilaçlar alan bazı hastalarda ortaya çıkan bir dopamin düzensizliği sendromu ile ilişkilidir .
Amfetaminin gen regülasyonu üzerindeki etkileri hem doza hem de yola bağlıdır. Gen regülasyonu ve bağımlılığı üzerine yapılan araştırmaların çoğu, çok yüksek dozlarda intravenöz amfetamin uygulaması ile hayvan çalışmalarına dayanmaktadır. Eşdeğer (ağırlığa göre ayarlanmış) insan terapötik dozlarını ve oral uygulamayı kullanan az sayıda çalışma, bu değişikliklerin meydana gelmesi durumunda nispeten küçük olduğunu göstermektedir. Bu, amfetaminin tıbbi kullanımının gen düzenlemesini önemli ölçüde etkilemediğini göstermektedir.
farmakolojik tedaviler
Aralık 2019 itibariyle amfetamin bağımlılığı için etkili bir farmakoterapi bulunmamaktadır . 2015 ve 2016'daki incelemeler, TAAR1 seçici agonistlerinin psikostimulan bağımlılıkları için bir tedavi olarak önemli terapötik potansiyele sahip olduğunu göstermiştir ; ancak, Şubat 2016 itibariyle, TAAR1 seçici agonistleri olarak işlev gördüğü bilinen tek bileşikler deneysel ilaçlardır . Amfetamin bağımlılığı, büyük ölçüde artmış aktivasyonu aracılık etmektedir dopamin reseptörlerine ve ko-lokalize NMDA reseptörleri nucleus accumbens içinde; magnezyum iyonları , reseptör kalsiyum kanalını bloke ederek NMDA reseptörlerini inhibe eder . Bir inceleme, hayvan testlerine dayanarak, patolojik (bağımlılığa neden olan) psikostimulan kullanımının beyindeki hücre içi magnezyum seviyesini önemli ölçüde azalttığını ileri sürdü. Ek magnezyum tedavisinin insanlarda kendi kendine amfetamin uygulamasını (yani kişinin kendisine verilen dozları) azalttığı gösterilmiştir , ancak amfetamin bağımlılığı için etkili bir monoterapi değildir .
2019'dan sistematik bir inceleme ve meta-analiz, RCT'lerde amfetamin ve metamfetamin bağımlılığı için kullanılan 17 farklı farmakoterapinin etkinliğini değerlendirdi; sadece metilfenidatın amfetamin veya metamfetamin kendi kendine tatbikatını azaltabileceğine dair düşük güçte kanıt bulmuştur. Antidepresanlar (bupropion, mirtazapin , sertralin ), antipsikotikler ( aripiprazol ), antikonvülsanlar ( topiramat , baklofen , gabapentin ), naltrekson , vareniklin dahil olmak üzere, RKÇ'lerde kullanılan diğer ilaçların çoğu için düşük ila orta güçte hiçbir yarar sağlamadığına dair kanıt vardı. , sitikolin , ondansetron , prometa , riluzol , atomoksetin , dekstroamfetamin ve modafinil .
davranışsal tedaviler
Bir 2018 sistematik gözden geçirilmesi ve ağ meta-analiz amfetamin, metamfetamin veya kokain bağımlılığı için 12 farklı psikososyal müdahaleler kapsayan 50 çalışmanın bulundu kombinasyon tedavisinin hem de risk yönetimi ve Topluluk Güçlendirme Yaklaşımı en yüksek etkinliği (yani perhiz oranı) ve kabul edilebilirliğini vardı ( yani, en düşük bırakma oranı). Analizde incelenen diğer tedavi yöntemleri , beklenmedik durum yönetimi veya topluluk güçlendirme yaklaşımı ile monoterapi , bilişsel davranışçı terapi , 12 adımlı programlar , koşulsuz ödül temelli terapiler, psikodinamik terapi ve bunları içeren diğer kombinasyon terapilerini içeriyordu.
Ek olarak, fiziksel egzersizin nörobiyolojik etkileri üzerine yapılan araştırmalar, günlük aerobik egzersizin, özellikle dayanıklılık egzersizinin (örneğin, maraton koşusu ) uyuşturucu bağımlılığının gelişmesini engellediğini ve amfetamin bağımlılığı için etkili bir yardımcı tedavi (yani ek bir tedavi) olduğunu göstermektedir. Egzersiz, özellikle psikostimulan bağımlılıkları için ek tedavi olarak kullanıldığında daha iyi tedavi sonuçlarına yol açar. Özellikle, aerobik egzersiz , psikostimülan kendini idare azaltmakta eski haline ilaç arayışı (diğer bir deyişle, relaps) ve indükler artan dopamin reseptör D'yi 2 içinde (DRD2) yoğunluğu striatum . Bu, striatal DRD2 yoğunluğunun azalmasına neden olan patolojik uyarıcı kullanımının tersidir. Bir inceleme, egzersizin , striatumda veya ödül sisteminin diğer bölümlerinde ΔFosB veya c-Fos immünoreaktivitesini değiştirerek bir uyuşturucu bağımlılığının gelişmesini de önleyebileceğini kaydetti .
| Şekli nöroplastisitesi veya davranışsal plastisite |
pekiştireç türü | Kaynaklar | |||||
|---|---|---|---|---|---|---|---|
| afyonlar | Psikostimulanlar | Yüksek yağlı veya şekerli yiyecekler | cinsel ilişki |
Fiziksel egzersiz (aerobik) |
Çevresel zenginleştirme |
||
|
ΔFosB ekspresyon nucleus accumbens D1 tipi MSNs |
↑ | ↑ | ↑ | ↑ | ↑ | ↑ | |
| davranışsal plastisite | |||||||
| alımın artırılması | Evet | Evet | Evet | ||||
| Psikostimulan çapraz duyarlılık |
Evet | Uygulanamaz | Evet | Evet | zayıflatılmış | zayıflatılmış | |
| Psikostimulan kendi kendine uygulama |
↑ | ↑ | ↓ | ↓ | ↓ | ||
| Psikostimulan koşullu yer tercihi |
↑ | ↑ | ↓ | ↑ | ↓ | ↑ | |
| Uyuşturucu arama davranışının eski haline döndürülmesi | ↑ | ↑ | ↓ | ↓ | |||
| nörokimyasal plastisite | |||||||
|
CREB fosforilasyon içinde nukleus accumbens'de |
↓ | ↓ | ↓ | ↓ | ↓ | ||
| Hassas dopamin yanıt olarak nucleus accumbens'inde |
Numara | Evet | Numara | Evet | |||
| Değiştirilmiş striatal dopamin sinyali | ↓ DRD2 , ↑ DRD3 | ↑ DRD1 , ↓ DRD2 , ↑ DRD3 | ↑ DRD1 , ↓ DRD2 , ↑ DRD3 | ↑ DRD2 | ↑ DRD2 | ||
| Değiştirilmiş striatal opioid sinyali | Değişiklik yok veya ↑ μ-opioid reseptörleri |
↑ μ-opioid reseptörleri ↑ κ-opioid reseptörleri |
↑ μ-opioid reseptörleri | ↑ μ-opioid reseptörleri | Değişiklik yok | Değişiklik yok | |
| Striatal opioid peptitlerindeki değişiklikler | ↑ dynorphin Değişiklik yok: enkefalin |
↑ dinorfin | ↓ enkefalin | ↑ dinorfin | ↑ dinorfin | ||
| Mezokortikolimbik sinaptik plastisite | |||||||
| Sayısı dendritler de nukleus accumbens'de | ↓ | ↑ | ↑ | ||||
|
Dendritik omurga içinde yoğunluk nukleus akkumbenlere |
↓ | ↑ | ↑ | ||||
Bağımlılık ve geri çekilme
Amfetamin kötüye kullanımında (yani eğlence amaçlı amfetamin kullanımında) uyuşturucu toleransı hızla gelişir, bu nedenle uzun süreli kötüye kullanım süreleri, aynı etkiyi elde etmek için ilacın giderek daha yüksek dozlarını gerektirir. Amfetamin ve metamfetamin'i zorunlu olarak kullanan bireylerde yoksunlukla ilgili bir Cochrane incelemesine göre , "kronik ağır kullanıcılar amfetamin kullanımını aniden bıraktığında, çoğu kişi son dozlarından sonraki 24 saat içinde meydana gelen zaman sınırlı bir yoksunluk sendromu bildirir." Bu derleme, kronik, yüksek doz kullananlarda yoksunluk semptomlarının sık olduğunu, vakaların kabaca %88'inde meydana geldiğini ve ilk haftada belirgin bir "çarpma" evresi ile 3-4 hafta boyunca devam ettiğini kaydetti. Amfetamin yoksunluk belirtileri arasında anksiyete, uyuşturucuya aşerme , depresif ruh hali , yorgunluk , iştah artışı , artan hareket veya azalan hareket , motivasyon eksikliği, uykusuzluk veya uyku hali ve berrak rüyalar sayılabilir . İnceleme, yoksunluk semptomlarının ciddiyetinin, bireyin yaşı ve bağımlılığının derecesi ile pozitif olarak ilişkili olduğunu göstermiştir. Terapötik dozlarda amfetamin tedavisinin kesilmesinden kaynaklanan hafif yoksunluk semptomları, doz azaltılarak önlenebilir.
aşırı doz
Bir amfetamin doz aşımı birçok farklı semptoma yol açabilir, ancak uygun bakım ile nadiren ölümcüldür. Doz aşımı semptomlarının şiddeti dozla artar ve amfetamine karşı ilaç toleransı ile azalır . Toleranslı bireylerin, günde maksimum günlük terapötik dozun yaklaşık 100 katı olan, günde 5 gram kadar amfetamin aldıkları bilinmektedir. Orta ve aşırı büyük doz aşımı belirtileri aşağıda listelenmiştir; ölümcül amfetamin zehirlenmesi genellikle konvülsiyonları ve komayı da içerir . 2013 yılında, amfetamin, metamfetamin ve " amfetamin kullanım bozukluğu " ile ilişkilendirilen diğer bileşiklere aşırı doz verilmesi, dünya çapında tahmini 3.788 ölümle sonuçlandı ( 3.425-4.145 ölüm, %95 güven ).
| sistem | Küçük veya orta doz aşımı | Şiddetli doz aşımı |
|---|---|---|
| kardiyovasküler |
|
|
|
Merkezi sinir sistemi |
|
|
| kas-iskelet sistemi |
|
|
| Solunum |
|
|
| İdrar |
|
|
| Başka |
|
|
toksisite
Kemirgenlerde ve primatlarda, yeterince yüksek dozlarda amfetamin , dopaminerjik nörotoksisiteye veya dopamin terminal dejenerasyonu ve azaltılmış taşıyıcı ve reseptör işlevi ile karakterize edilen dopamin nöronlarında hasara neden olur . Amfetaminin insanlarda doğrudan nörotoksik olduğuna dair bir kanıt yoktur. Bununla birlikte, yüksek dozlarda amfetamin, hiperpireksi , aşırı reaktif oksijen türlerinin oluşumu ve dopaminin artan otooksidasyonunun bir sonucu olarak dolaylı olarak dopaminerjik nörotoksisiteye neden olabilir . Yüksek dozda amfetamin maruziyetinden kaynaklanan nörotoksisitenin hayvan modelleri , amfetamin kaynaklı nörotoksisitenin gelişimi için hiperpireksi oluşumunun (yani çekirdek vücut sıcaklığı ≥ 40 °C) gerekli olduğunu göstermektedir. 40 °C'nin üzerindeki uzun süreli beyin sıcaklığı yükselmeleri, reaktif oksijen türlerinin üretimini kolaylaştırarak, hücresel protein fonksiyonunu bozarak ve geçici olarak kan-beyin bariyeri geçirgenliğini artırarak laboratuvar hayvanlarında amfetamin kaynaklı nörotoksisitenin gelişmesini teşvik eder .
Psikoz
Bir amfetamin doz aşımı, sanrılar ve paranoya gibi çeşitli semptomları içerebilen uyarıcı bir psikoza neden olabilir. Amfetamin, dekstroamfetamin ve metamfetamin psikozu tedavisine ilişkin bir Cochrane incelemesi, kullanıcıların yaklaşık % 5-15'inin tamamen iyileşmediğini belirtmektedir. Aynı incelemeye göre, antipsikotik ilaçların akut amfetamin psikozunun semptomlarını etkili bir şekilde çözdüğünü gösteren en az bir çalışma var . Psikoz nadiren terapötik kullanımdan kaynaklanır.
İlaç etkileşimleri
Birçok madde türünün amfetamin ile etkileşime girdiği ve bunun , amfetaminin, etkileşime giren maddenin veya her ikisinin de değişen ilaç etkisi veya metabolizması ile sonuçlandığı bilinmektedir . Amfetamini metabolize eden enzimlerin inhibitörleri (örneğin, CYP2D6 ve FMO3 ) eliminasyon yarı ömrünü uzatacak , yani etkileri daha uzun sürecek. Amfetamin ayrıca MAOI'ler , özellikle monoamin oksidaz A inhibitörleri ile etkileşime girer , çünkü hem MAOI'ler hem de amfetamin plazma katekolaminlerini (yani, norepinefrin ve dopamin) arttırır; bu nedenle, her ikisinin birlikte kullanımı tehlikelidir. Amfetamin çoğu psikoaktif ilacın aktivitesini modüle eder. Özellikle amfetamin, sakinleştirici ve depresanların etkilerini azaltabilir ve uyarıcı ve antidepresanların etkilerini artırabilir . Amfetamin, sırasıyla kan basıncı ve dopamin üzerindeki etkilerinden dolayı antihipertansiflerin ve antipsikotiklerin etkilerini de azaltabilir . Çinko takviyesi , DEHB tedavisi için kullanıldığında minimum etkili amfetamin dozunu azaltabilir .
Genel olarak, amfetamin gıda ile tüketildiğinde önemli bir etkileşim yoktur, ancak gastrointestinal içeriğin ve idrarın pH'ı sırasıyla amfetaminin emilimini ve atılımını etkiler . Asidik maddeler amfetamin emilimini azaltır ve idrarla atılımı artırır, alkali maddeler ise tam tersini yapar. Etki pH emilimini sahiptir, örneğin, mide asidi azaltıcı maddeler ile amfetamin etkileşime bağlı proton pompa inhibitörleri ve H 2 antihistaminler mide pH değerini (yani, daha az asidik hale).
Farmakoloji
farmakodinamik
|
Bir dopamin nöronunda amfetaminin farmakodinamiği
|
Amfetamin, davranışsal etkilerini beyindeki nöronal sinyaller olarak monoaminlerin kullanımını değiştirerek , özellikle de beynin ödül ve yürütücü işlev yollarındaki katekolamin nöronlarında gösterir. Ödül devresi ve yürütme işlevinde yer alan ana nörotransmitterlerin konsantrasyonları, dopamin ve norepinefrin, monoamin taşıyıcıları üzerindeki etkilerinden dolayı amfetamin tarafından doza bağlı bir şekilde çarpıcı biçimde artar . Takviye edici ve motivasyon çıkıntı amfetamin -promoting etkileri nedeniyle çok gelişmiş dopaminerjik aktiviteye olan mezolimbik yolu . Öforik amfetamin ve lokomotor uyarıcı etkileri sinaptik dopamin ve norepinefrin konsantrasyonları artar göre büyüklüğü ve hızı bağlıdır striatum .
Amfetamin güçlü bir şekilde tespit edilmiştir tam agonist ve iz amin bağlantılı reseptörün 1 (TAAR1), bir G s -coupled ve G q -coupled G-protein kenetli reseptör beyin monoaminler düzenlenmesi için önemli 2001 yılında keşfedilmiştir (GPCR), . TAAR1'in aktivasyonu, adenilil siklaz aktivasyonu yoluyla cAMP üretimini arttırır ve monoamin taşıyıcı fonksiyonunu inhibe eder . Monoamin oto- (örneğin, D 2 kısa , presinaptik α 2 ve presinaptik 5-HT 1A ) TAAR1 ters bir etki ve birlikte bu reseptörler monoaminler için düzenleyici bir sistem sağlar. Özellikle, amfetamin ve eser aminler , TAAR1 için yüksek bağlanma afinitelerine sahiptir, ancak monoamin otoreseptörleri için değildir. Görüntüleme çalışmaları, amfetamin ve eser aminler tarafından monoamin geri alım inhibisyonunun bölgeye özgü olduğunu ve ilişkili monoamin nöronlarında TAAR1 ortak lokalizasyonunun varlığına bağlı olduğunu göstermektedir .
Nöronal monoamin taşıyıcılarına ek olarak , amfetamin ayrıca hem veziküler monoamin taşıyıcıları , VMAT1 ve VMAT2'yi hem de SLC1A1 , SLC22A3 ve SLC22A5'i inhibe eder . SLC1A1, nöronlarda bulunan bir glutamat taşıyıcısı olan uyarıcı amino asit taşıyıcısı 3'tür (EAAT3), SLC22A3, astrositlerde bulunan ekstranöronal bir monoamin taşıyıcısıdır ve SLC22A5, yüksek afiniteli bir karnitin taşıyıcısıdır. Amfetaminin, nöronal gelişimde ve in vitro hayatta kalmada gözlemlenebilir artışlara neden olan beslenme davranışı, stres ve ödülle ilgili bir nöropeptid olan kokain ve amfetaminle düzenlenen transkript (CART) gen ekspresyonunu güçlü bir şekilde indüklediği bilinmektedir . Sepete reseptörü henüz tespit edilmesi, ancak önemli kanıtlar vardır benzersiz bir Sepete bağlandığı , G ı / G O -coupled GPCR . Amfetamin ayrıca monoamin oksidazları çok yüksek dozlarda inhibe ederek daha az monoamin ve eser amin metabolizmasına ve sonuç olarak daha yüksek sinaptik monoamin konsantrasyonlarına neden olur. İnsanlarda, amfetaminin bağlandığı bilinen tek post-sinaptik reseptör, düşük mikromolar afiniteye sahip bir agonist olarak hareket ettiği 5-HT1A reseptörüdür .
Amfetaminin insanlarda kısa vadeli ilaç etkilerinin tam profili, çoğunlukla artan hücresel iletişim veya dopamin , serotonin , norepinefrin , epinefrin , histamin , CART peptidleri , endojen opioidler , adrenokortikotropik hormon , kortikosteroidler ve glutamatın nörotransmisyonuyla elde edilir. ile etkileşimleri CART , 5-HT1A , EAAT3 , TAAR1 , VMAT1 , VMAT2 ve muhtemelen diğer biyolojik hedefler . Amfetamin ayrıca , birçoğu insan beyninde ifade edilen yedi insan karbonik anhidraz enzimini aktive eder.
Dekstroamfetamin, levoamfetaminden daha güçlü bir TAAR1 agonistidir . Sonuç olarak, dekstroamfetamin, levoamfetaminden daha fazla, kabaca üç ila dört kat daha fazla CNS uyarımı üretir , ancak levoamfetaminin biraz daha güçlü kardiyovasküler ve periferik etkileri vardır.
dopamin
Bazı beyin bölgelerinde, amfetamin sinaptik yarıkta dopamin konsantrasyonunu arttırır . Amfetamin presinaptik nörona ya DAT yoluyla ya da nöronal membrandan doğrudan difüze olarak girebilir . DAT alımının bir sonucu olarak, amfetamin taşıyıcıda rekabetçi geri alım inhibisyonu üretir. Presinaptik nörona girdikten sonra amfetamin , protein kinaz A (PKA) ve protein kinaz C (PKC) sinyallemesi yoluyla DAT fosforilasyonuna neden olan TAAR1'i aktive eder . Her iki protein kinaz tarafından fosforilasyon, DAT içselleştirmesi ( rekabetçi olmayan geri alım inhibisyonu) ile sonuçlanabilir , ancak tek başına PKC aracılı fosforilasyon , DAT yoluyla dopamin taşınmasının tersine çevrilmesine neden olur (yani, dopamin akışı ). Amfetaminin, tanımlanamayan bir Ca2+/kalmodulin bağımlı protein kinaza (CAMK) bağımlı yol aracılığıyla DAT fosforilasyonu ile ilişkili bir etki olan hücre içi kalsiyumu arttırdığı ve bunun sonucunda dopamin akışı ürettiği bilinmektedir. Doğrudan aktivasyonu yoluyla G-protein-bağlanmış içeri doğru rektifiye potasyum kanallarının , TAAR1 azaltır ateşleme hızı , bir hiper-dopaminerjik önlemek, dopamin nöronlarının.
Amfetamin, ön-sinaptik için bir substrat olan vesiküler monoamin taşıyıcı , VMAT2 . VMAT2'de amfetamin alımını takiben, amfetamin veziküler pH gradyanının çökmesini indükler, bu da dopamin moleküllerinin sinaptik veziküllerden VMAT2 yoluyla dopamin akışı yoluyla sitozole salınmasıyla sonuçlanır. Daha sonra, sitosolik dopamin molekülleri ters taşıma araçları ile sinir hücreleri arasındaki boşluğa presinaptik nöron salınır DAT .
norepinefrin
Dopamine benzer şekilde, amfetamin doza bağlı olarak epinefrinin doğrudan öncüsü olan sinaptik norepinefrin seviyesini arttırır . Nöronal TAAR1 mRNA ekspresyonuna dayanarak , amfetaminin norepinefrini dopamine benzer şekilde etkilediği düşünülmektedir. Başka bir deyişle, amfetamin , fosforile edilmiş NET'te TAAR1 aracılı akış ve rekabetçi olmayan geri alım inhibisyonunu , rekabetçi NET geri alım inhibisyonunu ve VMAT2'den norepinefrin salınımını indükler .
serotonin
Amfetamin, dopamin ve norepinefrinde olduğu gibi serotonin üzerinde benzer, ancak daha az belirgin etkiler gösterir. Amfetamin aracılığıyla serotonini etkileyen VMAT2 norepinefrin gibi fosforile düşünülmektedir ve SERT yoluyla TAAR1 . Dopamin gibi, amfetamin de insan 5-HT1A reseptöründe düşük, mikromolar afiniteye sahiptir .
Diğer nörotransmitterler, peptitler, hormonlar ve enzimler
| Enzim | K bir ( nM ) | Kaynaklar |
|---|---|---|
| hCA4 | 94 | |
| hCA5A | 810 | |
| hCA5B | 2560 | |
| hCA7 | 910 | |
| hCA12 | 640 | |
| hCA13 | 24100 | |
| hCA14 | 9150 |
İnsanlarda akut amfetamin uygulaması , ödül sistemindeki çeşitli beyin yapılarında endojen opioid salınımını arttırır . Beyindeki birincil uyarıcı nörotransmitter olan glutamatın hücre dışı seviyelerinin, amfetamine maruz kalmayı takiben striatumda arttığı gösterilmiştir. Hücre dışı glutamattaki bu artış, muhtemelen dopamin nöronlarında bir glutamat geri alım taşıyıcısı olan EAAT3'ün amfetamin kaynaklı içselleştirilmesi yoluyla gerçekleşir . Amfetamin, aynı zamanda, seçici bir salımına sebep olmaktadır histamin gelen mast hücreleri ile ilgili ve dışa akımı histaminerjik nöronlar aracılığıyla VMAT2 . Akut amfetamin uygulaması , hipotalamik-hipofiz-adrenal ekseni uyararak kan plazmasındaki adrenokortikotropik hormon ve kortikosteroid seviyelerini de artırabilir .
Aralık 2017'de amfetamin ve insan karbonik anhidraz enzimleri arasındaki etkileşimi değerlendiren ilk çalışma yayınlandı; İncelediği on bir karbonik anhidraz enziminden, amfetaminin, dördü insan beyninde yüksek oranda eksprese edilen yedi tanesini, düşük mikromolar aktive edici etkiler yoluyla düşük nanomolar ile güçlü bir şekilde aktive ettiğini buldu . Klinik öncesi araştırmalara dayanarak, serebral karbonik anhidraz aktivasyonunun bilişi geliştirici etkileri vardır; ancak, karbonik anhidraz inhibitörlerinin klinik kullanımına bağlı olarak, diğer dokulardaki karbonik anhidraz aktivasyonu, glokomu şiddetlendiren oküler aktivasyon gibi olumsuz etkilerle ilişkilendirilebilir .
farmakokinetik
Amfetaminin oral biyoyararlanımı gastrointestinal pH'a göre değişir; bağırsaktan iyi emilir ve dekstroamfetamin için biyoyararlanım tipik olarak %75'in üzerindedir. Amfetamin bir ile zayıf bir baz olan p K a 9.9; pH bazik olduğunda sonuç olarak, daha fazla ilacın onun içinde lipit çözünür serbest baz formu ve daha lipid bakımından zengin emilir hücre zarları gut epiteli . Tersine, asidik bir pH, ilacın ağırlıklı olarak suda çözünür bir katyonik (tuz) formda olduğu ve daha az emildiği anlamına gelir. Kan dolaşımında dolaşan amfetaminin yaklaşık %20'si plazma proteinlerine bağlanır . Emilimi takiben amfetamin , beyin omurilik sıvısı ve beyin dokusunda yüksek konsantrasyonlarda meydana gelen vücuttaki çoğu dokuya kolayca dağılır .
Yarı ömürleri amfetamin enantiyomerlerin farklıdır ve idrar pH değişir. Normal idrar pH'ında dekstroamfetamin ve levoamfetaminin yarı ömürleri sırasıyla 9-11 saat ve 11-14 saattir. Yüksek asidik idrar, enantiyomerin yarı ömrünü 7 saate düşürür; yüksek alkali idrar, yarılanma ömrünü 34 saate kadar uzatacaktır. Her iki izomerin tuzlarının hemen salınan ve uzun süreli salınan varyantları, dozdan sırasıyla 3 saat ve 7 saat sonra doruk plazma konsantrasyonlarına ulaşır . Amfetamin edilir ortadan yoluyla böbrek ile, % 30-40 , ilacın normal üriner pH değişmeden atılır edilir. İdrar pH'ı bazik olduğunda, amfetamin serbest baz formundadır, dolayısıyla daha az atılır. İdrar pH'ı anormal olduğunda, amfetaminin idrarda geri kazanımı, çoğunlukla idrarın sırasıyla çok bazik veya asidik olmasına bağlı olarak %1 gibi düşük bir değerden %75 gibi yüksek bir değere kadar değişebilir. Oral uygulamayı takiben, amfetamin 3 saat içinde idrarda görülür. Yutulan amfetaminin kabaca %90'ı, son oral dozdan 3 gün sonra elimine edilir.
Ön ilaç lisdexamfetamin, mide-bağırsak yolunda emildiğinde pH'a amfetamin kadar duyarlı değildir; kan dolaşımına emildikten sonra, kırmızı kan hücresi ile ilişkili enzimler tarafından hidroliz yoluyla dekstroamfetamine dönüştürülür . Lisdexamfetaminin eliminasyon yarı ömrü genellikle 1 saatten azdır.
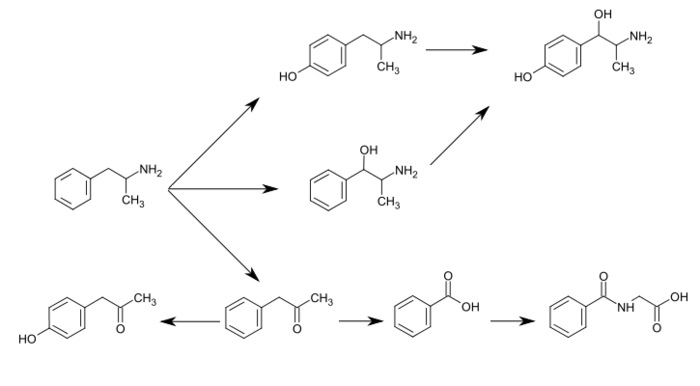
CYP2D6 , dopamin β-hidroksilaz (DBH), flavin içeren monooksijenaz 3 (FMO3), butirat-CoA ligaz (XM-ligaz) ve glisin N- asiltransferaz (GLYAT), insanlarda amfetamin veya metabolitlerini metabolize ettiği bilinen enzimlerdir . Amfetamin, 4-hidroksiamfetamin , 4-hidroksinorefedrin , 4-hidroksifenilaseton , benzoik asit , hippurik asit , norefedrin ve fenilaseton dahil olmak üzere çeşitli atılan metabolik ürünlere sahiptir . Bu metabolitlerin arasında, aktif sempatomimetikler olarak 4-hidroksiamfetamin , 4-hydroxynorephedrine ve norefedrin. Ana metabolik yollar, aromatik para-hidroksilasyon, alifatik alfa- ve beta-hidroksilasyon, N- oksidasyon, N- dealkilasyon ve deaminasyonu içerir. İnsanlarda bilinen metabolik yollar, saptanabilir metabolitler ve metabolize edici enzimler şunları içerir:
|
İnsanlarda amfetaminin metabolik yolları
|
farmakomikrobiyomik
İnsan metagenome (yani, tek bir genetik kompozisyonu ve bireyin vücut üzerindeki ya da içindeki bulunan tüm mikroorganizmalar) bireyler arasında önemli farklılık gösterir. Kompozisyonunu değiştirerek ilaçlar: insan vücudunda mikrobik ve virüs hücrelerin toplam sayısı yana (100 trilyon) üzerinden büyük ölçüde insan hücreleri (trilyon onlarca) outnumbers, dahil olmak üzere önemli ilaçlar arasındaki etkileşimler için bir potansiyel ve bireyin mikrobiyomları vardır, insan mikrobiyom , ilacın farmakokinetik profilini değiştiren mikrobiyal enzimler tarafından ilaç metabolizması ve bir ilacın klinik etkinliğini ve toksisite profilini etkileyen mikrobiyal ilaç metabolizması . Bu etkileşimleri inceleyen alan olarak bilinir pharmacomicrobiomics .
Çoğu biyomolekül ve diğer oral yoldan uygulanan ksenobiyotiklere (yani ilaçlar) benzer şekilde, amfetaminin kan dolaşımına emilmeden önce insan gastrointestinal mikrobiyotası (öncelikle bakteriler) tarafından rastgele metabolizmaya uğradığı tahmin edilmektedir . İlk amfetamin metabolize eden mikrobiyal enzim, insan bağırsağında yaygın olarak bulunan bir E. coli türünden tiramin oksidaz , 2019'da tanımlandı. Bu enzimin amfetamin, tiramin ve fenetilamini, üçü için de kabaca aynı bağlanma afinitesi ile metabolize ettiği bulundu. Bileşikler.
İlgili endojen bileşikler
Amfetamin, insan vücudunda ve beyninde üretilen doğal olarak oluşan nöromodülatör moleküller olan endojen eser aminlere çok benzer bir yapıya ve işleve sahiptir . Bu grup arasında en yakından ilişkili bileşikler, amfetaminin ana bileşiği olan fenetilamin ve amfetaminin bir izomeri olan N- metilfenetilamindir (yani, aynı moleküler formüle sahiptir). İnsanlarda fenetilamin, L-DOPA'yı da dopamine dönüştüren aromatik amino asit dekarboksilaz (AADC) enzimi tarafından doğrudan L-fenilalaninden üretilir . Sırasıyla, N- metilfenetilamin , fenetilaminden feniletanolamin N- metiltransferaz tarafından metabolize edilir , bu enzim norepinefrini epinefrine metabolize eden aynı enzimdir. Amfetamin gibi, hem fenetilamin hem de N- metilfenetilamin , TAAR1 yoluyla monoamin sinir iletimini düzenler ; amfetaminden farklı olarak, bu maddelerin her ikisi de monoamin oksidaz B tarafından parçalanır ve bu nedenle amfetaminden daha kısa bir yarı ömre sahiptir.
Kimya
|
rasemik amfetamin
|
Fenil-2-nitropropen (sağ kaplar)
Amfetamin, C 9 H 13 N kimyasal formülüne sahip memeli nörotransmitter fenetilaminin bir metil homologudur .. Birincil amine bitişik karbon atomu bir stereojenik merkezdir ve amfetamin, iki enantiyomerin rasemik 1:1 karışımından oluşur . Bu rasemik karışım optik izomerlerine ayrılabilir : levoamfetamin ve dekstroamfetamin . Oda sıcaklığında, amfetaminin saf serbest bazı, karakteristik olarak güçlü bir amin kokusu ve buruk, yanık tadı olan hareketli, renksiz ve uçucu bir sıvıdır . Amfetaminin sıklıkla hazırlanan katı tuzları arasında amfetamin adipat, aspartat, hidroklorür, fosfat, sakarat, sülfat ve tanat bulunur. Dekstroamfetamin sülfat en yaygın enantiopür tuzudur. Amfetamin aynı zamanda bir dizi psikoaktif türev içeren kendi yapısal sınıfının ana bileşiğidir . Organik kimyada, amfetamin mükemmel bir kiral ligandı için stereo-seçici sentez ve 1,1'-bi-2-naftol .
ikame edilmiş türevler
Amfetaminin ikameli türevleri veya "ikame edilmiş amfetaminler", bir "omurga" olarak amfetamin içeren çok çeşitli kimyasallardır; özellikle, bu kimyasal sınıf , amfetamin çekirdek yapısındaki bir veya daha fazla hidrojen atomunun ikame edicilerle değiştirilmesiyle oluşturulan türev bileşikleri içerir . Sınıf, diğer alt grupların yanı sıra amfetaminin kendisini, metamfetamin gibi uyarıcıları, MDMA gibi serotonerjik empatojenleri ve efedrin gibi dekonjestanları içerir .
sentez
İlk preparasyonun 1887'de bildirilmesinden bu yana, amfetamin için çok sayıda sentetik yol geliştirilmiştir. Hem yasal hem de yasadışı amfetamin sentezinin en yaygın yolu, Leuckart reaksiyonu (yöntem 1) olarak bilinen metal olmayan bir indirgeme kullanır . İlk adımda, fenilaseton ve formamid arasında , ek formik asit veya indirgeyici ajan olarak formamidin kendisi kullanılarak bir reaksiyon, N- formilamfetamin verir . Bu ara madde daha sonra hidroklorik asit kullanılarak hidrolize edilir ve ardından bazlaştırılır, organik çözücü ile özütlenir, konsantre edilir ve serbest baz verecek şekilde damıtılır. Serbest baz daha sonra organik bir çözücü içinde çözülür, sülfürik asit eklenir ve amfetamin sülfat tuzu olarak çökelir.
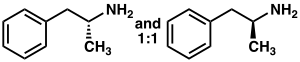
Amfetaminin iki enantiyomerini ayırmak için bir dizi kiral çözünürlük geliştirilmiştir. Örneğin, rasemik amfetamin, dekstroamfetamin verecek şekilde fraksiyonel olarak kristalize edilen bir diastereoizomerik tuz oluşturmak üzere d- tartarik asit ile işlenebilir . Kiral çözünürlük, büyük ölçekte optik olarak saf amfetamin elde etmek için en ekonomik yöntem olmaya devam etmektedir. Ek olarak, amfetaminin birkaç enantioselektif sentezi geliştirilmiştir. Bir örnekte, optik olarak saf ( R )-1-fenil-etanamin , bir kiral Schiff bazı verecek şekilde fenilaseton ile yoğunlaştırılır . Anahtar aşamada, bu ara madde, amino grubuna alfa karbon atomuna kiralite transferi ile katalitik hidrojenasyon ile indirgenir . Benzilik amin bağının hidrojenasyon ile bölünmesi, optik olarak saf dekstroamfetamin verir.
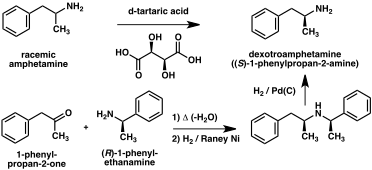
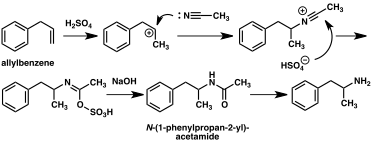
Klasik organik reaksiyonlara dayalı olarak amfetamin için çok sayıda alternatif sentetik yol geliştirilmiştir. Bir örnek , Friedel-Crafts alkilasyonu benzen ile alil klorür daha sonra rasemik amfetamin (yöntem 2) üretmek üzere amonyak ile reaksiyona sokulur, beta chloropropylbenzene elde edilir. Başka bir örnek, Ritter reaksiyonunu kullanır (yöntem 3). Bu yolda allilbenzen , sülfürik asit içinde asetonitril ile reaksiyona sokularak bir organosülfat elde edilir, bu da bir asetamid ara maddesi aracılığıyla amfetamin verecek şekilde sodyum hidroksit ile işlenir . Üçüncü bir yol , metil iyodür ve ardından benzil klorür ile bir çift alkilasyon yoluyla 2-metil-3-fenil-propanoik aside dönüştürülebilen etil 3-oksobutanoat ile başlar . Bu sentetik ara madde, bir Hofmann veya Curtius yeniden düzenlemesi (yöntem 4) kullanılarak amfetamine dönüştürülebilir .
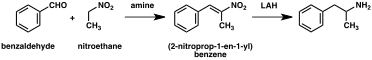
Önemli sayıda amfetamin sentezi , bir nitro , imin , oksim veya diğer nitrojen içeren fonksiyonel gruplarda bir azalma özelliğine sahiptir . Böyle bir örnekte, bir Knoevenagel kondansasyonu içinde benzaldehid ile nitroetan verir fenil-2-nitropropene . Bu ara ikili bağı ve nitro grubunun, bir indirgenir ya da katalitik kullanılarak hidrojenasyon ile işlenerek veya lityum alüminyum hidrür (yöntem 5). Diğer bir yöntem, fenilasetonun amonyak ile reaksiyonu, bir paladyum katalizörü veya lityum alüminyum hidrit üzerinde hidrojen kullanılarak birincil amine indirgenen bir imin ara ürünü üretilmesidir (yöntem 6).
|
|
|
Vücut sıvılarında algılama
Amfetamin, spor, istihdam, zehirlenme teşhisi ve adli tıp için bir uyuşturucu testinin parçası olarak sıklıkla idrar veya kanda ölçülür . Amfetamin testinin en yaygın şekli olan immunoassay gibi teknikler , bir takım sempatomimetik ilaçlarla çapraz reaksiyona girebilir. Yanlış pozitif sonuçları önlemek için amfetamine özgü kromatografik yöntemler kullanılır. Reçeteli amfetamin, reçeteli amfetamin ön ilaçları (örneğin selegilin ), levometamfetamin içeren reçetesiz satılan ilaç ürünleri veya yasa dışı olarak elde edilen ikameli amfetaminler olsun, ilacın kaynağını ayırt etmeye yardımcı olmak için kiral ayırma teknikleri kullanılabilir . Bazı reçeteli ilaçlar , diğerleri arasında benzfetamin , klobenzorex , famprofazon , fenproporex , lisdexamfetamin , mezokarb , metamfetamin, prenilamin ve selegilin dahil olmak üzere bir metabolit olarak amfetamin üretir . Bu bileşikler, ilaç testlerinde amfetamin için pozitif sonuçlar üretebilir. Amfetamin genellikle sadece standart bir ilaç testi ile yaklaşık 24 saat boyunca saptanabilir, ancak yüksek doz 2-4 gün boyunca saptanabilir .
Tahliller için, bir çalışma, amfetamin ve metamfetamin için bir enzimle çoğaltılmış bağışıklık tahlili tekniği (EMIT) tahlilinin, sıvı kromatografi-tandem kütle spektrometrisinden daha fazla yanlış pozitif üretebileceğini kaydetti . Amfetamin ve metamfetaminin türevlendirme maddesi ( S )-(-)-trifloroasetilprolil klorür ile gaz kromatografisi-kütle spektrometrisi (GC-MS), idrarda metamfetaminin saptanmasına izin verir. Kiral türevlendirme maddesi Mosher asit klorürü ile amfetamin ve metamfetaminin GC- MS'si, idrarda hem dekstroamfetamin hem de dekstrometamfetaminin saptanmasına izin verir. Bu nedenle, ikinci yöntem, ilacın çeşitli kaynakları arasında ayrım yapılmasına yardımcı olmak için diğer yöntemler kullanılarak pozitif test edilen numunelerde kullanılabilir.
Tarih, toplum ve kültür
| Madde | En iyi tahmin |
Düşük tahmin |
Yüksek tahmin |
|---|---|---|---|
| Amfetamin tipi uyarıcılar |
34.16 | 13.42 | 55.24 |
| esrar | 192.15 | 165,76 | 234.06 |
| Kokain | 18.20 | 13.87 | 22.85 |
| ecstasy | 20.57 | 8.99 | 32.34 |
| afyonlar | 19.38 | 13.80 | 26.15 |
| opioidler | 34.26 | 27.01 | 44.54 |
Amfetamin ilk Romen kimyager tarafından Almanya'da 1887 yılında sentezlendi Lazăr Edeleanu o adında phenylisopropylamine ; uyarıcı etkileri, Gordon Alles tarafından bağımsız olarak yeniden sentezlendiği ve sempatomimetik özelliklere sahip olduğu bildirildiği 1927 yılına kadar bilinmiyordu . Amfetamin, Smith, Kline ve French'in Benzedrine markası altında bir dekonjestan olarak bir inhaler olarak satmaya başladığı 1933'ün sonlarına kadar tıbbi bir kullanımı yoktu . Benzedrin sülfat 3 yıl sonra piyasaya sürüldü ve diğerleri arasında narkolepsi , obezite , düşük tansiyon , düşük libido ve kronik ağrı dahil olmak üzere çok çeşitli tıbbi durumları tedavi etmek için kullanıldı . İkinci Dünya Savaşı sırasında, amfetamin ve metamfetamin, uyarıcı ve performans arttırıcı etkileri nedeniyle hem Müttefik hem de Mihver kuvvetleri tarafından yoğun bir şekilde kullanıldı. İlacın bağımlılık yapan özellikleri bilinmeye başladıkça, hükümetler amfetamin satışına sıkı denetimler uygulamaya başladı. Örneğin, Amerika Birleşik Devletleri'nde 1970'lerin başlarında, amfetamin , Kontrollü Maddeler Yasası kapsamında program II kontrollü bir madde haline geldi . Sıkı hükümet kontrollerine rağmen, amfetamin, yazarlar, müzisyenler, matematikçiler ve sporcular dahil olmak üzere çeşitli geçmişlerden insanlar tarafından yasal veya yasadışı olarak kullanılmıştır.
Amfetamin bugün hala yasadışı olarak gizli laboratuvarlarda sentezlenmekte ve başta Avrupa ülkeleri olmak üzere karaborsada satılmaktadır . 2018 yılında Avrupa Birliği (AB) üye ülkeleri arasında, 15-64 yaş arası 11,9 milyon yetişkin, yaşamlarında en az bir kez amfetamin veya metamfetamin kullanmış ve 1,7 milyonu da son bir yılda her ikisini de kullanmıştır. 2012 yılında, AB üye ülkelerinde yaklaşık 5,9 metrik ton yasadışı amfetamin ele geçirildi; AB içinde yasa dışı amfetaminin "sokak fiyatı" aynı dönemde gram başına 6-38 € arasında değişiyordu . Avrupa dışında, amfetamin için yasa dışı pazar, metamfetamin ve MDMA pazarından çok daha küçüktür.
Hukuki durum
Birleşmiş Milletler 1971 Psikotrop Maddeler Sözleşmesi'nin bir sonucu olarak , amfetamin, anlaşmada tanımlandığı gibi, 183 devletin tümünde program II kontrollü bir madde haline geldi. Sonuç olarak, çoğu ülkede sıkı bir şekilde düzenlenmiştir. Güney Kore ve Japonya gibi bazı ülkeler, tıbbi kullanım için bile ikame edilmiş amfetaminleri yasakladı. Kanada ( program I uyuşturucu ), Hollanda ( Liste I uyuşturucu ), Amerika Birleşik Devletleri ( program II uyuşturucu ), Avustralya ( program 8 ), Tayland ( kategori 1 narkotik ) ve Birleşik Krallık ( sınıf B uyuşturucu ) gibi diğer ülkelerde ), amfetamin, tıbbi tedavi olarak kullanılmasına izin veren kısıtlayıcı bir ulusal ilaç programındadır.
Eczacılıkla ilgili ürünler
Şu anda pazarlanan birkaç amfetamin formülasyonu, Adderall, Adderall XR, Mydayis, Adzenys ER, Adzenys XR-ODT , Dyanavel XR, Evekeo ve Evekeo ODT markaları altında pazarlananlar da dahil olmak üzere her iki enantiyomeri içerir . Bunlardan Evekeo (Evekeo ODT dahil), yalnızca rasemik amfetamin (amfetamin sülfat olarak) içeren tek üründür ve bu nedenle aktif kısmı doğru bir şekilde "amfetamin" olarak adlandırılabilen tek üründür . Dekstroamfetamin, marka adları Dexedrine ve Zenzedi altında pazarlanan, sadece enantiyosaf mevcut amfetamin ürünü. Bir ön-ilaç dekstroamfetamin şekli lisdexamfetamine de mevcuttur ve markası Vyvanse altında pazarlanmaktadır. Bir ön ilaç olduğu için lisdexamfetamin yapısal olarak dekstroamfetaminden farklıdır ve dekstroamfetamine metabolize olana kadar inaktiftir. Rasemik amfetaminin serbest bazı daha önce Benzedrine, Psychedrine ve Sympatedrine olarak mevcuttu. Levoamfetamin daha önce Cydril olarak mevcuttu. Mevcut amfetamin ilaçlarının çoğu , serbest bazın nispeten yüksek uçuculuğu nedeniyle tuzlardır . Bununla birlikte, serbest bazdan oluşan oral süspansiyon ve ağızda dağılan tablet (ODT) dozaj formları sırasıyla 2015 ve 2016 yıllarında piyasaya sürülmüştür. Mevcut markalardan bazıları ve jenerik eşdeğerleri aşağıda listelenmiştir.
| Marka adı |
Amerika Birleşik Devletleri Kabul Edilen Ad |
(D:L) oranı |
Dozaj formu |
Pazarlama başlangıç tarihi |
ABD tüketici fiyat verileri |
Kaynaklar |
|---|---|---|---|---|---|---|
| zerdeçal | - | 3:1 (tuz) | tablet | 1996 | iyiRx | |
| Adderall XR | - | 3:1 (tuz) | kapsül | 2001 | iyiRx | |
| Mydayiler | - | 3:1 (tuz) | kapsül | 2017 | iyiRx | |
| Adzenys Acil Servis | amfetamin | 3:1 (taban) | süspansiyon | 2017 | iyiRx | |
| Adzenys XR-ODT | amfetamin | 3:1 (taban) | ODT | 2016 | iyiRx | |
| Dyanavel XR | amfetamin | 3,2:1 (taban) | süspansiyon | 2015 | iyiRx | |
| evekeo | amfetamin sülfat | 1:1 (tuz) | tablet | 2012 | iyiRx | |
| Evekeo ODT | amfetamin sülfat | 1:1 (tuz) | ODT | 2019 | iyiRx | |
| deksedrin | dekstroamfetamin sülfat | 1:0 (tuz) | kapsül | 1976 | iyiRx | |
| Zenzedi | dekstroamfetamin sülfat | 1:0 (tuz) | tablet | 2013 | iyiRx | |
| Vyvanse | lisdexamfetamin dimisilat | 1:0 (ön ilaç) | kapsül | 2007 | iyiRx | |
| tablet |
| ilaç | formül |
moleküler kütle |
amfetamin baz |
eşit dozlarda amfetamin bazı |
eşit baz içerikli dozlar |
|||||
|---|---|---|---|---|---|---|---|---|---|---|
| (g/mol) | (yüzde) | (30 mg doz) | ||||||||
| Toplam | temel | Toplam | dekstro- | levo- | dekstro- | levo- | ||||
| dekstroamfetamin sülfat | (C 9 H 13 N) 2 •H 2 SO 4 |
368.49
|
270.41
|
%73,38
|
%73,38
|
-
|
22.0 mg
|
-
|
30.0 mg
|
|
| amfetamin sülfat | (C 9 H 13 N) 2 •H 2 SO 4 |
368.49
|
270.41
|
%73,38
|
%36.69
|
%36.69
|
11.0 mg
|
11.0 mg
|
30.0 mg
|
|
| zerdeçal |
%62.57
|
%47,49
|
%15.08
|
14,2 mg
|
4,5 mg
|
35.2 mg
|
||||
| %25 | dekstroamfetamin sülfat | (C 9 H 13 N) 2 •H 2 SO 4 |
368.49
|
270.41
|
%73,38
|
%73,38
|
-
|
|||
| %25 | amfetamin sülfat | (C 9 H 13 N) 2 •H 2 SO 4 |
368.49
|
270.41
|
%73,38
|
%36.69
|
%36.69
|
|||
| %25 | dekstroamfetamin sakarat | (C 9 H 13 N) 2 •C 6 H 10 O 8 |
480.55
|
270.41
|
%56.27
|
%56.27
|
-
|
|||
| %25 | amfetamin aspartat monohidrat | (C 9 H 13 N)•C 4 H 7 NO 4 •H 2 O |
286,32
|
135.21
|
%47.22
|
%23.61
|
%23.61
|
|||
| lisdexamfetamin dimisilat | C 15 H 25 N 3 O•(CH 4 O 3 S) 2 |
455.49
|
135.21
|
%29.68
|
%29.68
|
-
|
8,9 mg
|
-
|
74,2 mg
|
|
| amfetamin bazlı süspansiyon | Cı- 9 H 13 N |
135.21
|
135.21
|
100%
|
%76.19
|
%23.81
|
22.9 mg
|
7,1 mg
|
22.0 mg
|
|
Notlar
- Görüntü efsanesi
Referans notları
Referanslar
Dış bağlantılar
- "Amfetamin" . İlaç Bilgi Portalı . Amerika Birleşik Devletleri Ulusal Tıp Kütüphanesi.
- CID 5826 den pubchem - Dekstroamfetamin
- CID 32893 den pubchem - Levoamphetamine
- Karşılaştırmalı Toksikogenomik Veritabanı girişi: Amfetamin
- Karşılaştırmalı Toksikogenomik Veritabanı girişi: CARTPT